Clear Sky Science · de
Reduziertes YTHDF2 hemmt PD-L1-Expression durch Stabilisierung von m6A-enthaltender SPOP-mRNA bei kolorektalem Krebs
Warum diese Forschung wichtig ist
Kolorektales Karzinom gehört zu den weltweit häufigsten und tödlichsten Krebsarten. Viele moderne Therapien versuchen, das körpereigene Immunsystem gegen Tumore zu mobilisieren, indem sie eine Bremse namens PD-1/PD-L1 blockieren. Dennoch profitieren die meisten Patientinnen und Patienten mit kolorektalem Krebs weiterhin nicht von diesen Medikamenten. Diese Studie enthüllt eine verborgene molekulare Kettenreaktion in Krebszellen, die ihnen hilft, diese Immun‑„Bremse“ gedrückt zu halten. Das Verständnis dieser Kette bietet einen neuen Ansatz, um die Wirksamkeit der Immuntherapie für deutlich mehr Menschen zu verbessern.
Ein verborgenes Markenzeichen auf Tumor‑RNA
Unsere Zellen lesen und bauen ständig RNA-Stränge ab, die kurzlebigen Nachrichten, die vorgeben, welche Proteine hergestellt werden sollen. In den letzten Jahren entdeckten Forschende, dass viele RNA‑Nachrichten winzige chemische Markierungen tragen, darunter eine namens m6A, die wie Bearbeitungszeichen in einem Manuskript wirken: Sie bestimmen, wie lange eine Nachricht erhalten bleibt und wie stark sie gelesen wird. Ein Protein namens YTHDF2 ist darauf spezialisiert, diese m6A‑Marken zu erkennen und hilft normalerweise dabei, markierte RNA abzubauen, wodurch die Proteinproduktion einer Zelle feinjustiert wird. In Tumorproben von Patientinnen und Patienten sowie in umfangreichen öffentlichen Datenbanken fanden die Autorinnen und Autoren, dass die YTHDF2‑Spiegel in Tumoren deutlich höher waren als im normalen Dickdarmgewebe und dass Patientinnen und Patienten mit höheren YTHDF2‑Werten tendenziell eine schlechtere Überlebensrate hatten, was auf eine krebsfördernde Rolle dieses RNA‑„Lesers“ hindeutet.
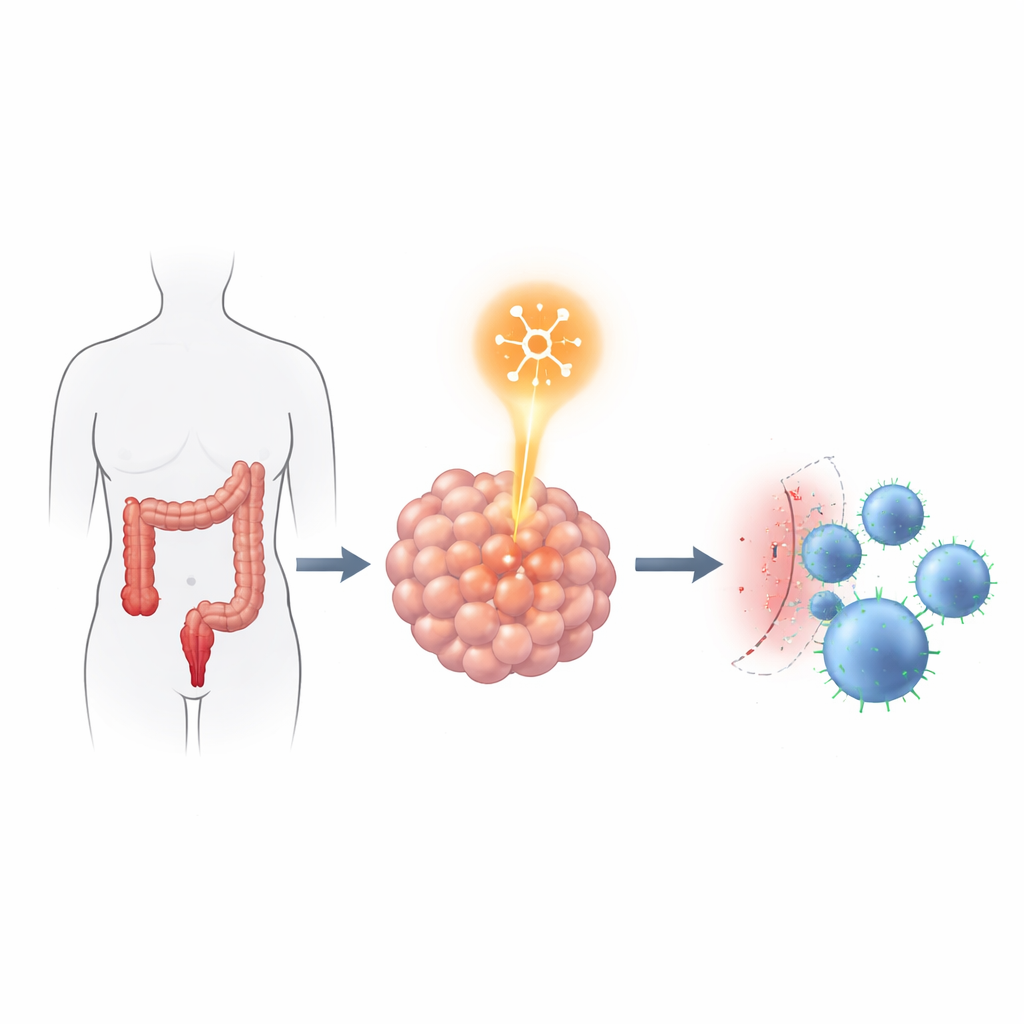
Die Verbindung des RNA‑Lesers zur Immunbremse
Als Nächstes fragten die Forschenden, wie YTHDF2 Tumoren dabei helfen könnte, Angriffen durch Immunzellen zu widerstehen. Sie transplantierten menschliche kolorektale Krebszellen mit oder ohne YTHDF2 in spezielle Mäuse, die zudem menschliche Immunzellen erhielten. Tumoren mit normalem YTHDF2 wuchsen schneller und zeigten weniger krebsabtötende T‑Zellen im Inneren. Wenn YTHDF2 reduziert wurde, schrumpften die Tumore, und mehr CD4‑ und CD8‑T‑Zellen infiltrierten den Krebs. Auffällig war, dass die Reduktion von YTHDF2 das Wachstum, die Bewegung oder das Invasionsverhalten der Krebszellen in Zellkultur kaum veränderte, was darauf hindeutet, dass seine hauptsächliche Wirkung auf die Interaktion des Tumors mit dem Immunsystem und nicht auf die rohe Tumoraggressivität gerichtet ist.
Wie Krebszellen PD-L1 hochhalten
PD-L1 ist ein Protein auf der Oberfläche von Tumorzellen, das an PD-1 auf T‑Zellen bindet und ihnen signalisiert, sich zurückzuziehen. Die Forschenden beobachteten, dass bei Herunterregulierung von YTHDF2 die Menge an PD-L1‑Protein auf Krebszellen und in ihren abgegebenen Vesikeln (Exosomen) stark abnahm, obwohl die PD-L1‑RNA‑Spiegel etwa gleich blieben. Das deutete darauf hin, dass YTHDF2 PD-L1 indirekt nach dem RNA‑Stadium beeinflusst. Detaillierte Untersuchungen zeigten, dass der Verlust von YTHDF2 das PD-L1‑Protein weniger stabil und leichter durch die zelluläre Proteinabbau‑Maschinerie zerstörbar machte und die Bindung zwischen PD‑1 und PD-L1 schwächte. Infolgedessen töteten T‑Zellen in gemeinsamen Kulturversuchen mehr Krebszellen, wenn YTHDF2 gering war, was einen funktionalen Zuwachs der Immunantwort zeigte.
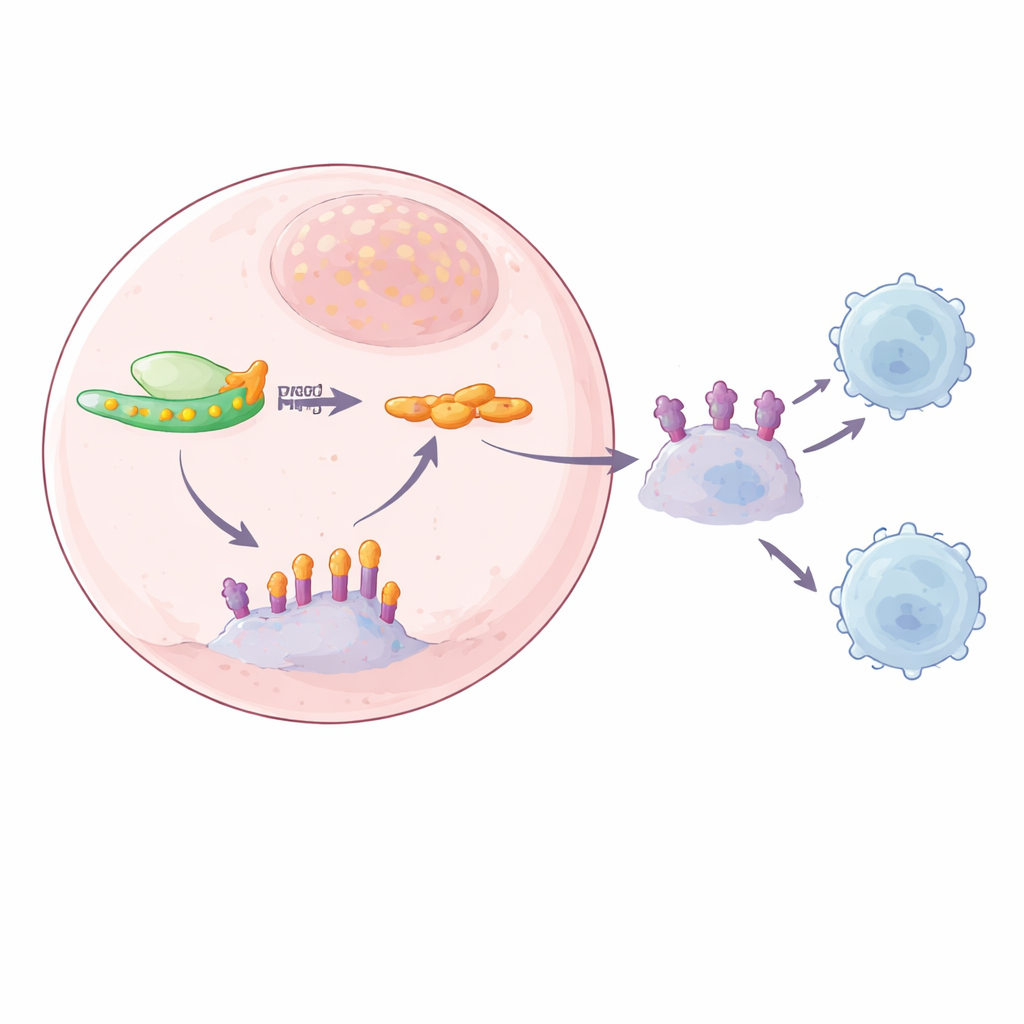
Die SPOP‑Verbindung: eine gestörte Aufräumcrew
Um die fehlende Verbindung zwischen YTHDF2 und PD-L1 aufzuspüren, kombinierten die Forschenden mehrere Sequenzier‑Ansätze, um nach RNA‑Nachrichten zu suchen, die sowohl mit m6A markiert als auch von YTHDF2 gebunden waren. Ein starker Kandidat war SPOP, Teil eines Proteinkomplexes, der normalerweise PD-L1 zur Zerstörung markiert und als Aufräumcrew verhindert, dass PD-L1 sich anhäuft. Die Autorinnen und Autoren fanden m6A‑Marken in der 3'‑Region der SPOP‑RNA und zeigten, dass YTHDF2 genau dort bindet. Wenn YTHDF2 in hoher Menge vorhanden war, wurde die SPOP‑RNA schneller abgebaut, was zu niedrigeren SPOP‑Proteinspiegeln und weniger Entfernung von PD-L1 führte. Bei Reduktion von YTHDF2 wurde die SPOP‑RNA stabiler, das SPOP‑Protein stieg an und die PD-L1‑Proteinspiegel fielen, sowohl an der Zelloberfläche als auch in Exosomen. Durch Mutation der m6A‑Stellen in der SPOP‑RNA oder durch Entfernen von SPOP selbst ließ sich diese Kette unterbrechen, was bestätigte, dass ein m6A‑abhängiger YTHDF2–SPOP‑Weg die PD-L1‑Menge kontrolliert.
Was das für künftige Therapien bedeutet
Kurz gesagt zeigt diese Arbeit ein dreistufiges Staffellauf‑System innerhalb kolorektaler Krebszellen: Das RNA‑Tag m6A erlaubt es YTHDF2, SPOP‑Spiegel zu verringern; geschwächtes SPOP kann PD-L1 nicht mehr ausreichend entfernen; die daraus resultierende Übermenge an PD-L1 schützt den Tumor vor T‑Zellen. Indem man diese Kette unterbricht — entweder durch Blockade von YTHDF2 oder durch Stärkung von SPOP — könnte man PD-L1 auf Tumoren senken und die Wirksamkeit bestehender PD-1/PD-L1‑Medikamente erhöhen, insbesondere bei Patientinnen und Patienten, die derzeit kaum profitieren. Die YTHDF2–SPOP–PD-L1‑Achse tritt damit als vielversprechendes neues Ziel hervor, um das Immunsystem zu befähigen, kolorektalen Krebs besser zu erkennen und zu zerstören.
Zitation: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Schlüsselwörter: kolorektales Karzinom, Immuntherapie, PD-L1, RNA-Modifikation, tumorbedingte Immunflucht