Clear Sky Science · fr
La réduction de YTHDF2 inhibe l'expression de PD-L1 en stabilisant l'ARNm SPOP contenant m6A dans le cancer colorectal
Pourquoi cette recherche compte
Le cancer colorectal est l'un des cancers les plus fréquents et meurtriers dans le monde. De nombreux traitements modernes cherchent à libérer le système immunitaire pour qu'il attaque les tumeurs en bloquant un frein appelé PD-1/PD-L1. Pourtant, la plupart des patients atteints de cancer colorectal ne tirent toujours pas bénéfice de ces médicaments. Cette étude met au jour une chaîne d'événements moléculaires cachée à l'intérieur des cellules cancéreuses qui les aide à maintenir ce « frein » immunitaire activé. Comprendre cette chaîne offre une nouvelle voie pour rendre l'immunothérapie efficace pour beaucoup plus de patients.
Une marque cachée sur l'ARN tumoral
Nos cellules lisent et détruisent en permanence des brins d'ARN, ces messages éphémères qui indiquent quelles protéines produire. Ces dernières années, les scientifiques ont découvert que de nombreux ARN portent de petites marques chimiques, dont une appelée m6A, qui fonctionnent comme des annotations dans un manuscrit : elles déterminent la durée de vie d'un message et l'intensité de sa traduction. Une protéine nommée YTHDF2 reconnaît ces marques m6A et aide généralement à dégrader l'ARN marqué, ajustant ainsi les protéines produites par la cellule. Dans des échantillons de cancer colorectal de patients et dans de larges bases de données publiques, les auteurs ont constaté que le niveau de YTHDF2 était nettement plus élevé dans les tumeurs que dans le tissu colique normal, et que les patients présentant plus de YTHDF2 avaient tendance à avoir une survie moindre, suggérant un rôle pro‑tumoral pour ce « lecteur » d'ARN.
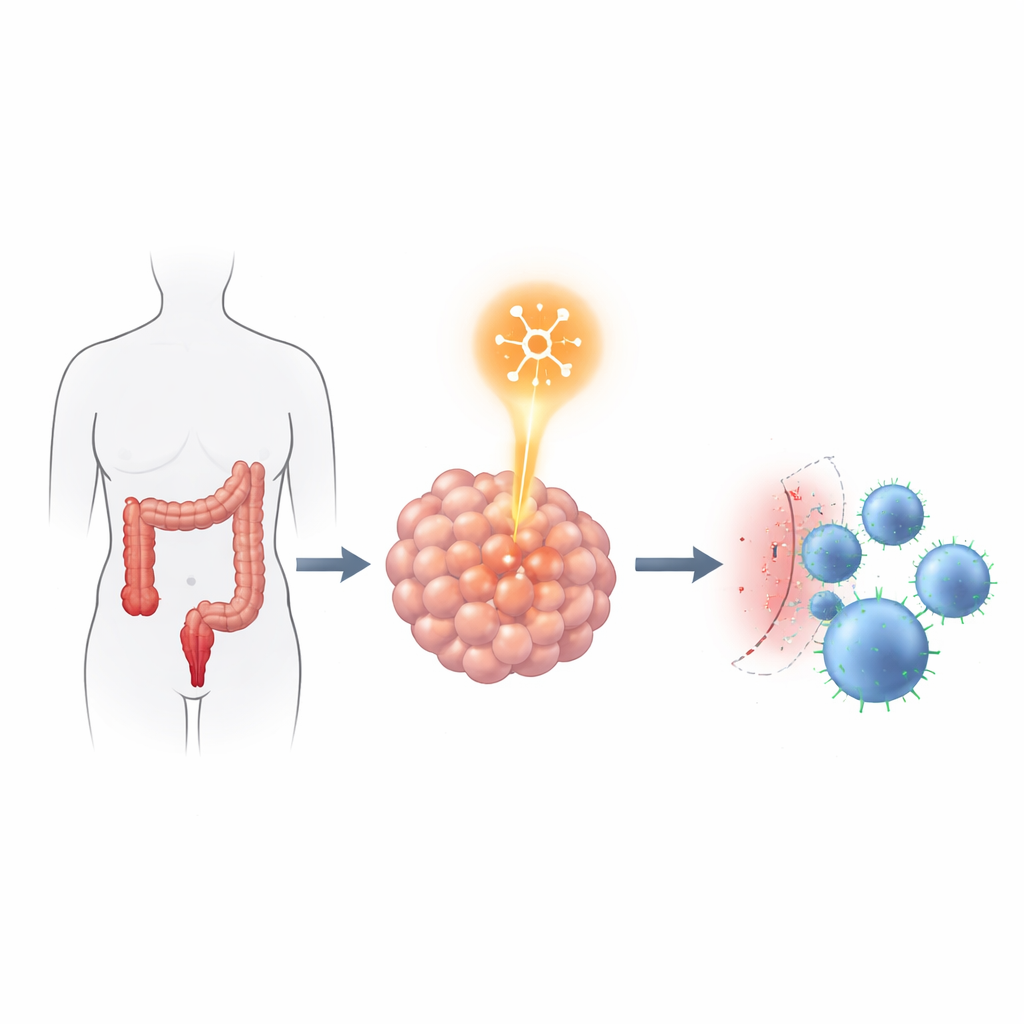
Relier le lecteur d'ARN au frein immunitaire
L'équipe a ensuite cherché comment YTHDF2 pourrait aider les tumeurs à résister aux attaques des cellules immunitaires. Ils ont implanté des cellules de cancer colorectal humain avec ou sans YTHDF2 dans des souris spéciales qui recevaient aussi des cellules immunitaires humaines. Les tumeurs avec un YTHDF2 normal ont grandi plus rapidement et présentaient moins de lymphocytes T tueurs à l'intérieur. Lorsque YTHDF2 était réduit, les tumeurs ont régressé et davantage de lymphocytes T CD4 et CD8 ont infiltré la tumeur. Fait notable, l'abaissement de YTHDF2 n'a pas modifié la vitesse de prolifération, de migration ou d'invasion des cellules cancéreuses en culture, ce qui suggère que son impact principal portait sur l'interaction tumeur‑système immunitaire plutôt que sur l'agressivité intrinsèque de la tumeur.
Comment les cellules cancéreuses maintiennent PD-L1 élevé
PD-L1 est une protéine à la surface des cellules tumorales qui se lie à PD-1 sur les lymphocytes T et les neutralise. Les chercheurs ont observé que lorsque YTHDF2 était réduit, la quantité de protéine PD-L1 à la surface des cellules cancéreuses et dans leurs vésicules sécrétées (exosomes) diminuait fortement, alors que les niveaux d'ARN de PD-L1 restaient à peu près identiques. Cela suggérait que YTHDF2 affecte PD-L1 de façon indirecte, après l'étape de l'ARN. Des tests détaillés ont montré que la perte de YTHDF2 rendait la protéine PD-L1 moins stable et plus susceptible d'être dégradée par le système protéolytique de la cellule, et affaiblissait la liaison entre PD-1 et PD-L1. En conséquence, dans des expériences de co‑culture, les lymphocytes T tuaient davantage de cellules cancéreuses lorsque YTHDF2 était bas, montrant une augmentation fonctionnelle de l'attaque immunitaire.
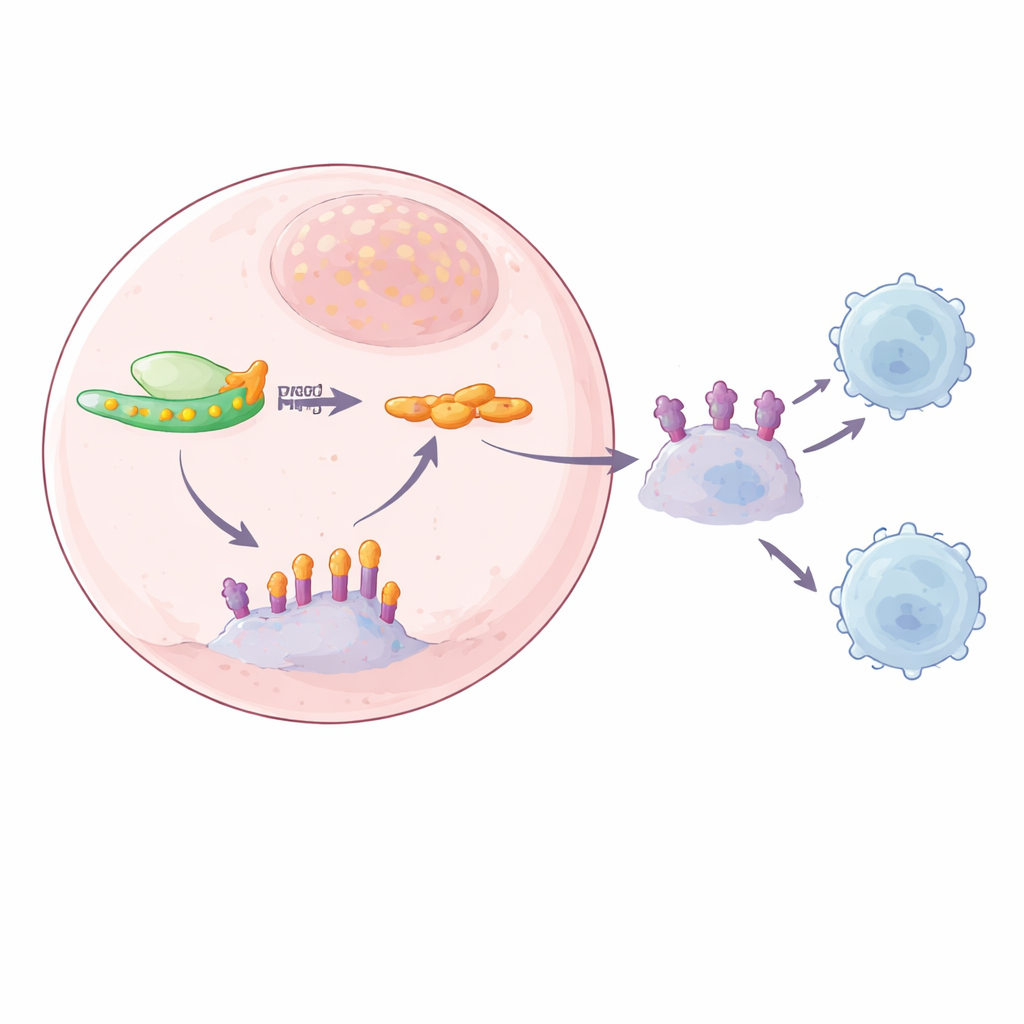
Le lien SPOP : une équipe de nettoyage défaillante
Pour retrouver le maillon manquant entre YTHDF2 et PD-L1, l'équipe a combiné plusieurs approches de séquençage pour chercher des ARN à la fois marqués par m6A et liés par YTHDF2. Un candidat solide était SPOP, composant d'un complexe protéique qui étiquette normalement PD-L1 pour sa destruction, agissant comme une équipe de nettoyage qui empêche l'accumulation de PD-L1. Les auteurs ont trouvé des marques m6A dans la région terminale de l'ARNm de SPOP et ont montré que YTHDF2 s'y lie précisément. Lorsque YTHDF2 est présent en forte quantité, l'ARNm de SPOP est dégradé plus rapidement, entraînant une baisse de la protéine SPOP et donc moins d'élimination de PD-L1. Lorsque YTHDF2 est réduit, l'ARNm de SPOP devient plus stable, la protéine SPOP augmente et les niveaux de PD-L1 diminuent, tant à la surface cellulaire que dans les exosomes. La mutation des sites m6A sur l'ARNm de SPOP ou la suppression de SPOP elle‑même rompaient cette chaîne, confirmant qu'une voie dépendante de m6A YTHDF2–SPOP contrôle l'abondance de PD-L1.
Ce que cela signifie pour les traitements futurs
En termes simples, ce travail révèle une relais en trois étapes à l'intérieur des cellules du cancer colorectal : la marque d'ARN m6A permet à YTHDF2 de réduire les niveaux de SPOP ; un SPOP affaibli ne peut pas correctement éliminer PD-L1 ; et l'excès de PD-L1 qui en résulte protège la tumeur des lymphocytes T. En interrompant ce relais — soit en bloquant YTHDF2, soit en renforçant SPOP — il pourrait être possible d'abaisser PD-L1 sur les tumeurs et d'améliorer l'efficacité des traitements anti‑PD-1/PD-L1 existants, en particulier pour les patients qui en bénéficient actuellement peu. L'axe YTHDF2–SPOP–PD-L1 émerge ainsi comme une nouvelle cible prometteuse pour aider le système immunitaire à mieux reconnaître et détruire le cancer colorectal.
Citation: Xu, X., Chen, H., Zhao, R. et al. Reduced YTHDF2 inhibits PD-L1 expression by stabilizing m6A-containing SPOP mRNA in colorectal cancer. Cell Death Dis 17, 351 (2026). https://doi.org/10.1038/s41419-026-08615-2
Mots-clés: cancer colorectal, immunothérapie, PD-L1, modification de l'ARN, évasion immunitaire tumorale