Clear Sky Science · tr
TSP-1'in RANK ve OPG ile Etkileşimi: Kemik Yenilenmesi ve Osteolitik Kemik Metastazı Üzerine Sonuçlar
Neden Kemik Parçalayan Kanserler Önemli?
Meme kanseri gibi bazı kanserler iskelete yayıldığında, kırıklar, güçsüzlük ve yaşam kalitesinde düşüşe yol açan ağrılı kemik “delikleri” oluşturabilir. Bu lezyonlar, normalde kemiği yeniden şekillendiren hücrelerin aşırı aktifleşip çok fazla doku yıkmasından kaynaklanır. Burada özetlenen çalışma, bu sistem içinde doğal bir fren olduğunu ortaya koyuyor: yaygın bir bağ dokusu proteininden türeyen bir fragman, kemik yıkımını azaltabiliyor ve farelerde kanser kaynaklı kemik hasarını yavaşlatabiliyor.
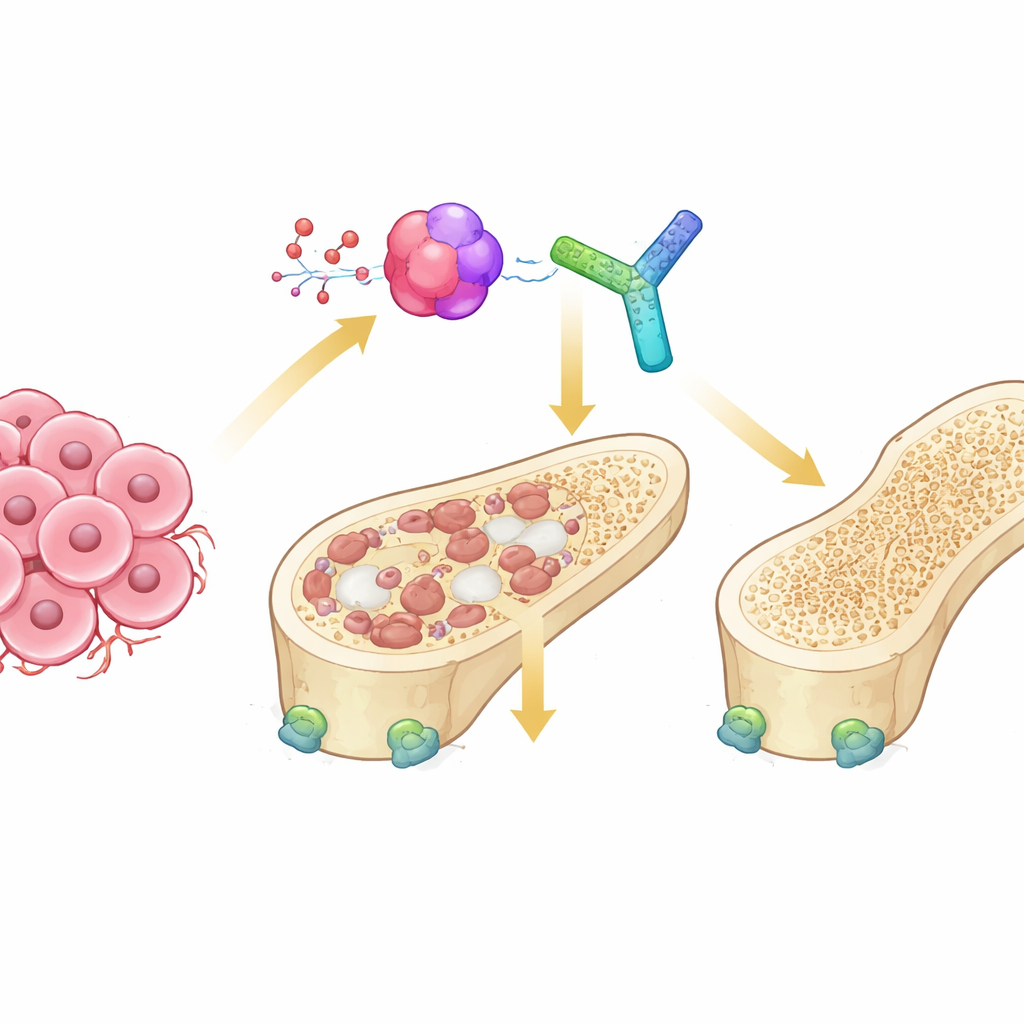
Kemiklerimizdeki Çekişme
Sağlıklı kemikler iki karşıt hücre tipi tarafından sürekli yenilenir. Osteoklastlar eski kemiği yıkar, osteoblastlar ise yeni kemik yapar. Kemiklere yayılan kanserlerde bu denge bozulur: tümör hücreleri osteoklastları aşırı uyarır ve kemikte oyulmaya yol açan “osteolitik” lezyonlar oluşur. Bu süreçteki ana iletişim hatlarından biri, osteoklastların olgunlaşmasını başlatan RANK–RANKL sistemidir. Üçüncü bir ortak oyuncu olan osteoprotegerin (OPG) normalde bir emniyet mekanizması gibi davranır; RANKL’ye bağlanarak kemik yiyen hücrelerin aşırı aktifleştirilmesini önler. Bu üçlünün kemik metastazlarının sert ortamında nasıl ince ayarlandığı belirsizdi.
Daha Büyük Bir Proteinde Saklı Sürpriz Bir Yardımcı
Araştırmacılar, doku mimarisini ve kanser mikroçevresini şekillendirdiği bilinen büyük bir ekstraselüler protein olan trombospondin‑1 (TSP‑1) üzerinde yoğunlaştı. Önceki çalışmalar, tam boy TSP‑1’in bazı koşullarda aslında kemik yıkımını teşvik edebileceğini düşündürmüştü. Bu çalışmada ekip, osteoklastları uyaran bazı alanlardan yoksun olan TSP‑1’in C‑terminal bölümüne, E123CaG adını verdikleri belirli bir parçaya odaklandı. Hücre kültürlerinde, bütün TSP‑1’in RANKL kaynaklı osteoklast oluşumunu değiştirmediğini, oysa E123CaG fragmanının olgun osteoklastların sayısını ve boyutunu güçlü şekilde azalttığını ve bu hücrelerin kemik rezorpsiyonu için ihtiyaç duyduğu aktin halka yapısını bozduğunu buldular. Önemli olarak, olgun osteoklastların kendileri proteazlar, özellikle HTRA1 adlı bir enzim salgılar; bu enzimler TSP‑1’i keserek E123CaG’ye benzer bir fragman oluşturuyor—bu da inhibitörün yerleşik bir geri besleme kontrolü olarak üretilebileceğini düşündürüyor.
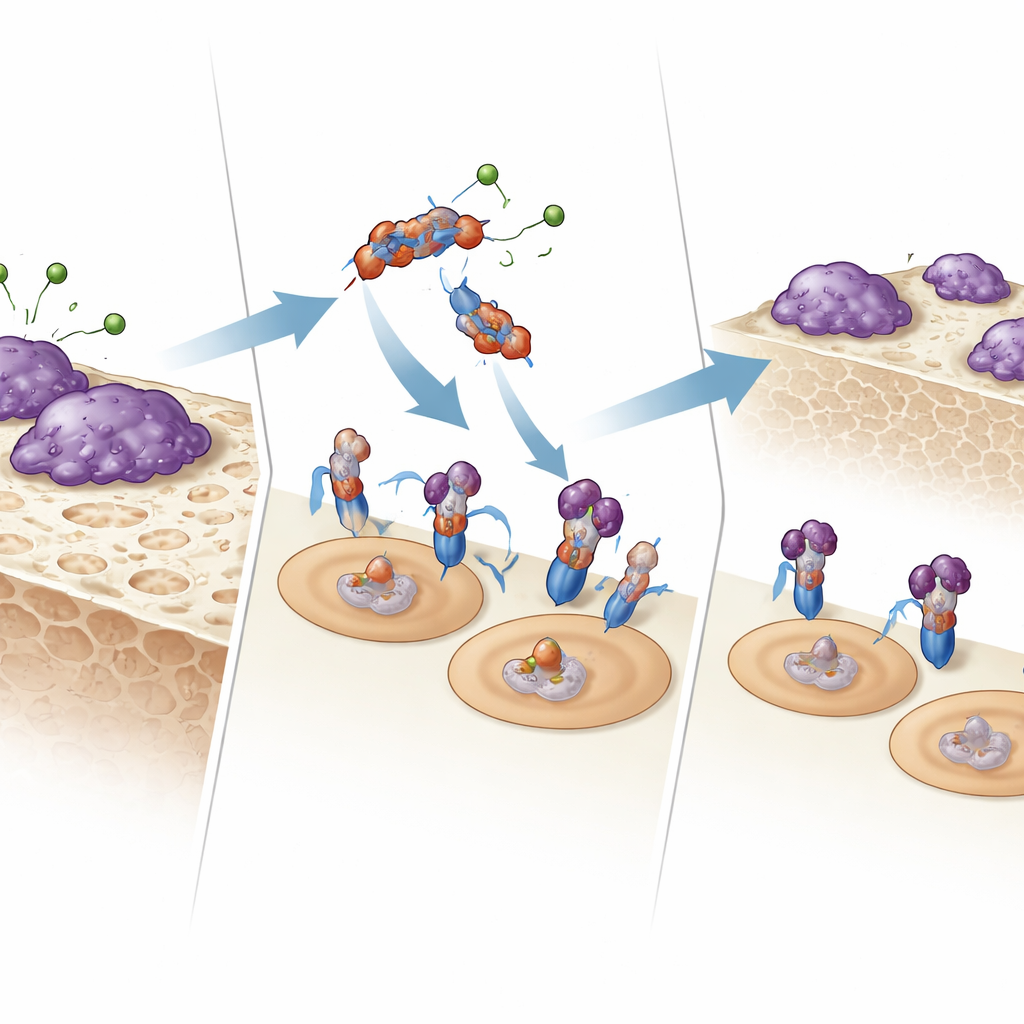
Fragman Kemik‑Yiyen Hücrelerle Nasıl Konuşuyor?
E123CaG’nin nasıl işlediğini anlamak için ekip, bunun osteoklastları kontrol eden reseptörlere doğrudan bağlanıp bağlanmadığını test etti. Yüzey plazmon rezonansı ve katı faz bağlanma deneyleri kullanarak E123CaG’nin osteoklast öncüllerindeki RANK reseptörüne tutunduğunu gösterdiler. Bu bağlanma RANKL’nin yerleşmesini engellemiyor, ama aşağı akış sinyalini zayıflatıyor: erken sinyal proteinleri (MAPK’ler p38 ve JNK) daha az kuvvetle aktifleşiyor ve anahtar transkripsiyon faktörü NFATc1 çekirdeğe daha az etkin taşınıyor. Bu değişiklikler birlikte, öncülleri tam olarak aktif kemik‑rezorbe edici hücrelere dönüştüren olgunlaşma programını köreltir.
Kemik Kaybı Üzerindeki Doğal Freni Korumak
Fragman sadece RANK sinyalini bozmakla kalmıyor; aynı zamanda RANKL’yi bağlayıp onu tutan vücudun sahte reseptörü OPG’ye de bağlanıyor. Kültürde E123CaG, OPG’nin RANKL’yi yakalamasını engellemedi; bunun yerine OPG’nin osteoklast oluşumunu engelleme yeteneğini artırdı. Araştırmacılar bunun nedenini keşfettiler: osteoklast olgunlaşması sırasında olgun osteoklastlardan salgılanan proteazlar, HTRA1 dahil, OPG’yi parçalayarak etkisizleştiriyor. E123CaG bulunduğunda OPG bu parçalanmadan korunuyor ve daha uzun süre sağlam kalıyor. Böylece TSP‑1 proteolizinden üretilen aynı fragman hem RANK’in iç sinyalini zayıflatıyor hem de OPG’yi koruyarak kemik yıkımı üzerinde iki katmanlı kontrolü güçlendiriyor.
Fragmanı Canlı Bir Sistemde Test Etmek
Bu etkilerin tüm organizmada da önemli olup olmadığını görmek için ekip, kemiğe tercihli yayılan bir fare meme kanseri hücre hattını E123CaG fragmanını salgılayacak şekilde genetik olarak düzenledi. Bu hücreler farelerin kan dolaşımına verilerek kemik metastazı oluşturulduğunda, E123CaG üreten tümörlere sahip hayvanlar kontrol grubuna göre daha uzun yaşadı ve daha az şiddetli kemik hasarı gösterdi. Yüksek çözünürlüklü mikro‑BT taramaları, süngerimsi (trabeküler) kemiğin daha iyi korunduğunu, kirişlerin daha kalın olduğunu ve aralarındaki boşlukların daha küçük olduğunu gösterdi. Bu faydalar birincil tümörün büyüme hızında değişiklik olmadan ortaya çıktı; bu da fragmanın esas olarak kemik mikroçevresini değiştirerek etki gösterdiğini, kanser hücrelerine doğrudan saldırmadığını düşündürüyor.
Bu Hastalar İçin Ne Anlama Geliyor?
Toplu olarak, bulgular kemikte daha önce fark edilmemiş bir koruyucu devreyi ortaya koyuyor: osteoklastlar TSP‑1’i kesen proteazlar salgılıyor, bu da bir fragman oluşturuyor; bu fragman ise daha fazla osteoklast aktivasyonunu frenliyor ve vücudun doğal inhibitörü OPG’yi yıkımdan koruyor. Meme kanseri kemik metastazı bağlamında bu fragman farelerde kemik‑yiyen hücrelerin oluşumunu yavaşlatabiliyor ve yıkıcı lezyonların yayılmasını sınırlayabiliyor. Herhangi bir tedavi geliştirilmeden önce daha fazla çalışma gerektiği doğru olsa da çalışma, E123CaG ve onun RANK ile OPG ile etkileşimlerini kanser ve aşırı kemik kaybıyla karakterize diğer hastalıklarda kemikleri daha iyi koruyabilecek ilaç adayları için umut verici hedefler olarak öne çıkarıyor.
Atıf: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Anahtar kelimeler: kemik metastazı, osteoklastlar, trombospondin-1, RANKL RANK OPG, kemik yenilenmesi