Clear Sky Science · sv
TSP-1 interaktion med RANK och OPG: konsekvenser för benomsättning och osteolytisk benmetastasering
Varför benangripande cancer är viktig
När cancerformer som bröstcancer sprider sig till skelettet kan de framkalla smärtsamma ”hål” i benet som leder till frakturer, svaghet och sämre livskvalitet. Dessa lesioner uppstår eftersom celler som normalt ombildar ben blir överaktiva och tär på vävnaden. Den här sammanfattade studien avslöjar en naturlig broms i systemet: en fragmenterad del av ett vanligt bindvävsprotein som kan dämpa bentillbakabrytning och bromsa cancerdriven bensskada hos möss.
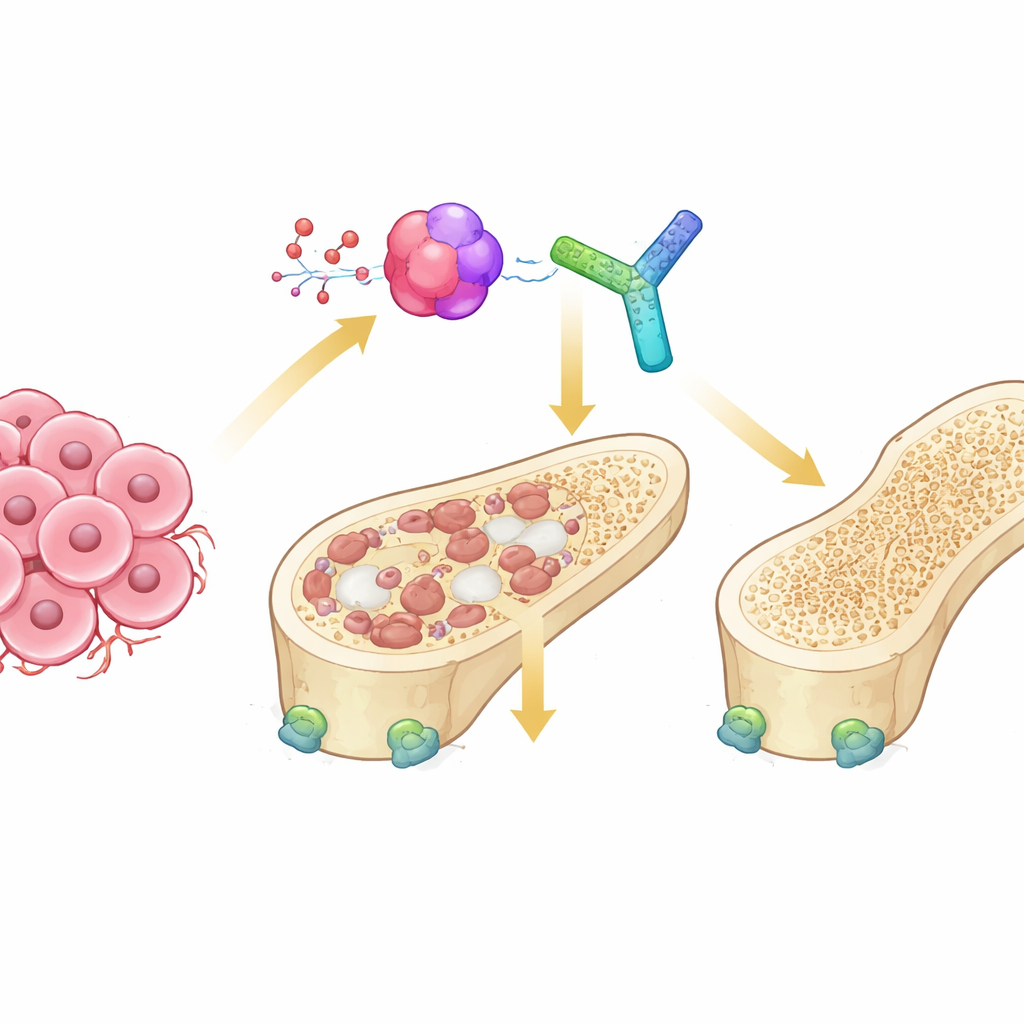
Dra‑och‑släpp‑striden inne i våra ben
Friska ben förnyas ständigt av två motsatta celltyper. Osteoklaster bryter ner gammalt ben, medan osteoblaster bygger nytt. När tumörer sprider sig till ben förloras denna balans: tumörceller skickar signaler som överstimulerar osteoklaster, vilket leder till ”osteolytiska” lesioner där ben urholkas. En nyckelkommunikationslinje i denna process är RANK–RANKL‑systemet, som slår på mognaden av osteoklaster. En tredje partner, osteoprotegerin (OPG), fungerar normalt som en säkerhetsbroms genom att binda RANKL och förhindra att det överaktiverar benätande celler. Hur denna trio finjusteras i den hårda miljön vid benmetastaser har varit oklart.
En överraskande hjälpare gömd i ett större protein
Forskarlaget fokuserade på trombospondin‑1 (TSP‑1), ett stort extracellulärt protein som påverkar vävnadsarkitektur och tumörmikromiljöer. Tidigare arbete har antytt att fullängds‑TSP‑1 under vissa förhållanden kan främja bendestruktion. Här undersökte teamet en specifik C-terminal del av TSP‑1, kallad E123CaG, som saknar vissa domäner som stimulerar osteoklaster. I cellkulturer fann de att medan intakt TSP‑1 inte förändrade RANKL‑inducerad osteoklastbildning, minskade E123CaG‑fragmentet kraftigt antalet och storleken på mogna osteoklaster och störde den aktinringstruktur som dessa celler behöver för att resorbera ben. Viktigt är att mogna osteoklaster själva frisätter proteaser, särskilt enzymet HTRA1, som klipper TSP‑1 och genererar ett fragment liknande E123CaG — vilket antyder att denna hämmare kan produceras som en inbyggd återkopplingskontroll.
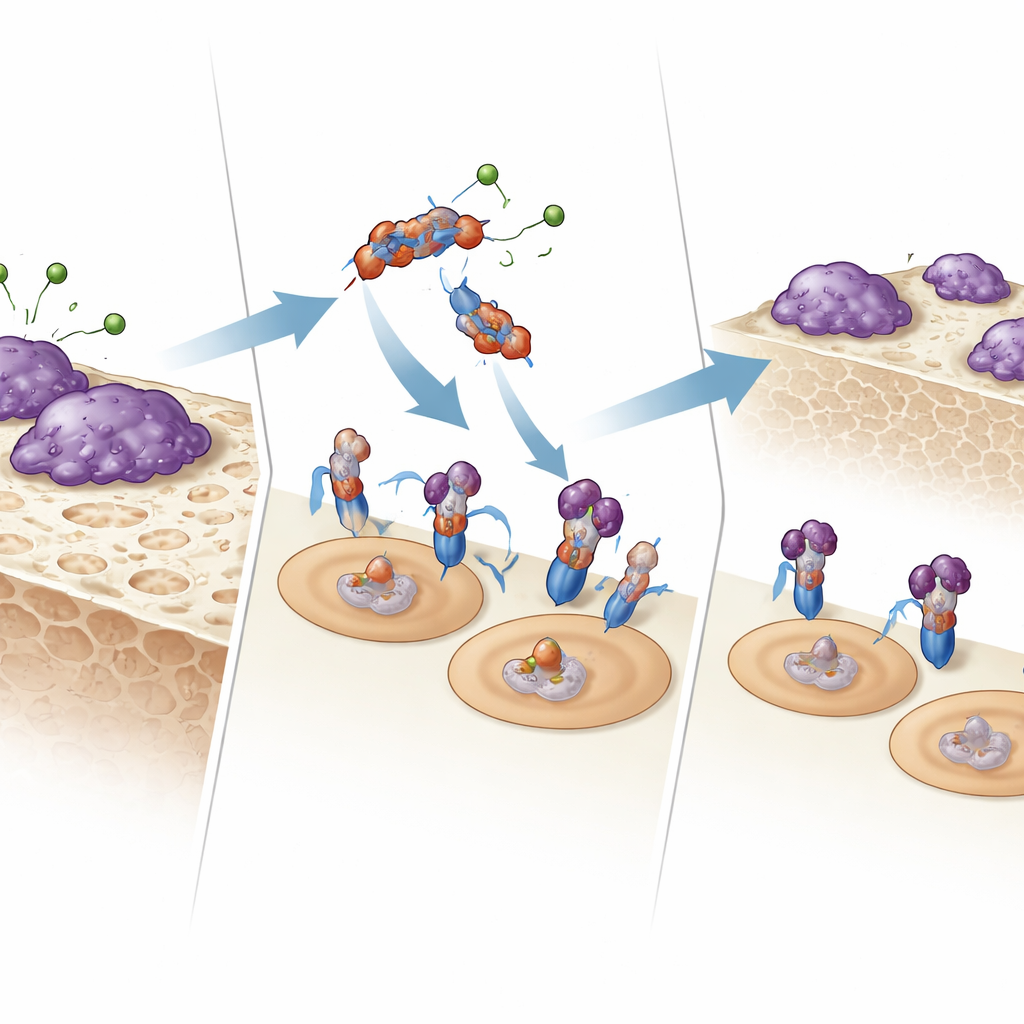
Hur fragmentet kommunicerar med benätande celler
För att förstå hur E123CaG verkar testade forskarna om det binder direkt till de receptorer som styr osteoklaster. Genom surface plasmon resonance och fast‑fasbindningsanalyser visade de att E123CaG fäster vid RANK, receptorn på osteoklastprecursorer som känner av RANKL. Denna bindning blockerar inte RANKL från att binda, men den försvagar den efterföljande signaleringen: tidiga signalproteiner (MAPK p38 och JNK) aktiveras svagare, och den viktiga transkriptionsfaktorn NFATc1 translokeras mindre effektivt till kärnan. Tillsammans dämpar dessa förändringar mognadsprogrammet som normalt omvandlar prekursorer till fullt aktiva benresorberande celler.
Skydda den naturliga bromsen mot benförlust
Fragmentet gör mer än att störa RANK‑signalering. Det binder också OPG, kroppens egen beteckningsreceptor som fångar upp RANKL. I kultur hindrade inte E123CaG OPG från att fånga RANKL; istället förstärkte det OPG:s förmåga att hämma osteoklastbildning. Forskarna upptäckte varför: under osteoklastutveckling skär proteaser från mogna osteoklaster, inklusive HTRA1, sönder och inaktiverar OPG. När E123CaG fanns närvarande skyddades OPG från denna nedbrytning och förblev intakt längre. Således dämpar samma fragment som genereras genom proteolys av TSP‑1 både RANK:s interna signal och bevarar OPG, vilket förstärker två kontrollager över bentillbakabrytning.
Test av fragmentet i ett levande system
För att se om dessa effekter spelar roll i en hel organism konstruerade teamet en bröstcancercellinje från mus som föredrar att sprida sig till ben för att utsöndra E123CaG‑fragmentet. När dessa celler injicerades i musers blodomlopp för att så frön till benmetastaser överlevde djur med tumörer som producerade E123CaG längre och hade mindre allvarliga bensskador än kontroller. Högupplöst mikro‑CT visade bättre bevarande av trabekulärt (svampigt) ben, tjockare balkar och mindre mellanrum dem emellan. Dessa fördelar uppträdde utan förändringar i primärtumörens tillväxthastighet, vilket tyder på att fragmentet huvudsakligen verkar genom att modifiera benmikromiljön snarare än att direkt angripa cancerceller.
Vad detta innebär för patienter
Tillsammans visar fynden en tidigare oupptäckt skyddscirkel i ben: osteoklaster släpper ut proteaser som klipper TSP‑1 till ett fragment som i sin tur dämpar fortsatt osteoklastaktivering och skyddar kroppens naturliga hämmare OPG från nedbrytning. I sammanhanget av bröstcancer‑benmetastasering kan detta fragment bromsa bildningen av benätande celler och begränsa spridningen av destruktiva lesioner hos möss. Även om mer arbete krävs innan någon behandling kan utvecklas, lyfter studien fram E123CaG och dess interaktioner med RANK och OPG som lovande spår för läkemedel som bättre skulle kunna skydda skelettet vid cancer och andra sjukdomar präglade av överdriven benförlust.
Citering: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Nyckelord: benmetastas, osteoklaster, trombospondin-1, RANKL RANK OPG, benomsättning