Clear Sky Science · ja
RANKとOPGとのTSP‑1相互作用:骨改変と骨吸収性転移に対する含意
なぜ骨を壊すがんが重要か
乳がんなどの腫瘍が骨に転移すると、骨に痛みを伴う“穴”が生じ、骨折や筋力低下、生活の質の低下を招きます。これらの病変は、本来骨を形作り直す役割を持つ細胞が過剰に働き、組織を過度に破壊してしまうことに起因します。本稿で要約する研究は、このシステム内に備わる自然のブレーキを明らかにします。すなわち、一般的な結合組織タンパク質の一部断片が骨破壊を抑え、マウスにおけるがんによる骨損傷の進行を鈍らせる、という発見です。
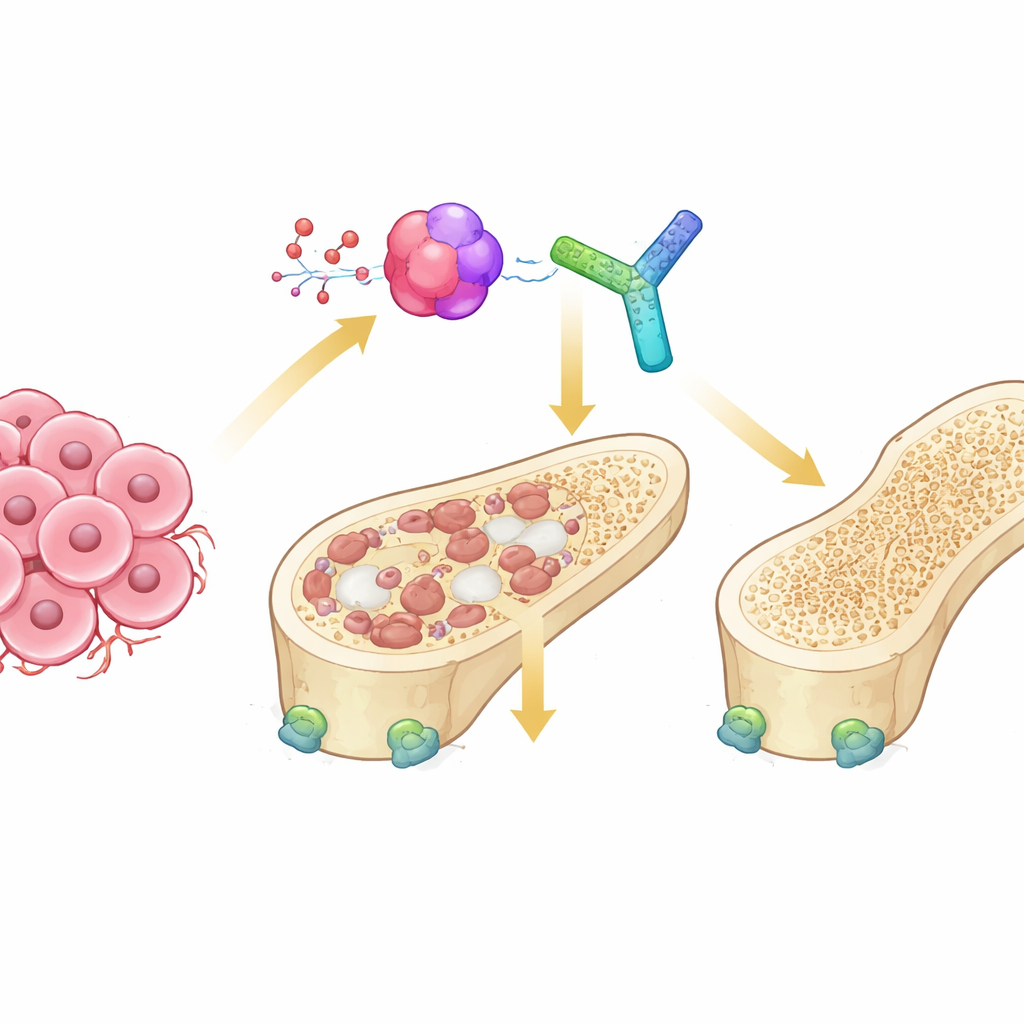
骨内の綱引き
健康な骨は、互いに対立する二種類の細胞によって常に更新されています。破骨細胞が古い骨を分解し、骨芽細胞が新しい骨を作ります。骨へ転移した腫瘍ではこのバランスが崩れ、腫瘍細胞が破骨細胞を過剰に刺激して『骨吸収性(osteolytic)』病変を引き起こし、骨が空洞化します。この過程で重要な情報伝達路はRANK–RANKLシステムであり、破骨細胞の成熟をスイッチオンします。第三の仲間であるオステオプロテゲリン(OPG)は通常安全装置として働き、RANKLに結合して骨を食べる細胞の過剰活性化を防ぎます。しかし、骨転移という厳しい環境においてこの三者がどのように精密に調節されているかは不明でした。
大きなタンパク質に隠れた意外な助っ人
研究者たちはトロンボスポンジン‑1(TSP‑1)に着目しました。TSP‑1は組織の構造や腫瘍微小環境を形作る大きな細胞外タンパク質です。これまでの研究では、全長のTSP‑1が条件によっては骨破壊を促進することさえ示唆されていました。本研究では、TSP‑1のC末端に位置する特定の部分断片、E123CaGに注目しました。この断片は破骨細胞を刺激するドメインのいくつかを欠いています。細胞培養系では、完全なTSP‑1はRANKLによる破骨細胞形成を変えませんでしたが、E123CaG断片は成熟した破骨細胞の数とサイズを強く減少させ、骨を吸収するために必要なアクチンリング構造を破壊しました。重要なのは、成熟破骨細胞自身がプロテアーゼ、特にHTRA1という酵素を放出し、これがTSP‑1を切断してE123CaGに類似した断片を生成することです—これはこの阻害因子がフィードバック制御として産生される可能性を示唆します。
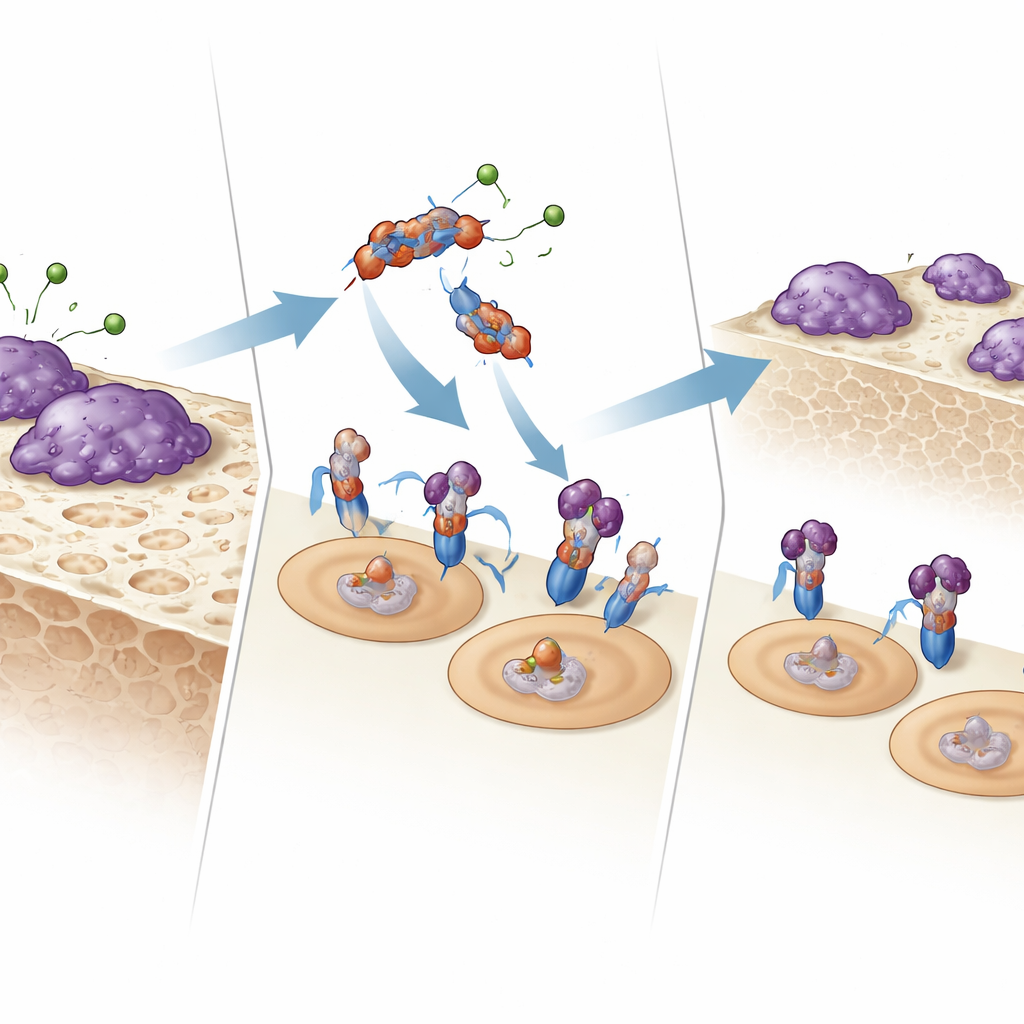
断片は骨を食べる細胞とどう対話するか
E123CaGの作用機序を理解するため、研究チームはそれが破骨細胞を制御する受容体に直接結合するかを調べました。表面プラズモン共鳴と固相結合アッセイを用いて、E123CaGが破骨細胞前駆細胞上の受容体であるRANKに付着することを示しました。この結合はRANKLのドッキングを阻止するものではありませんが、下流のシグナルを弱めます。初期シグナル経路のタンパク質(MAPKのp38やJNK)の活性化が弱まり、主要な転写因子NFATc1の核内移行も効率が落ちます。これらの変化が合わさって、前駆細胞を完全に活性化した骨吸収細胞へと成熟させるプログラムを鈍らせます。
骨喪失の自然のブレーキを守る
この断片はRANKシグナルの妨害以上の働きをします。E123CaGは、RANKLを取り除く体内のデコイ受容体であるOPGにも結合します。培養では、E123CaGはOPGがRANKLを捕まえるのを妨げるのではなく、むしろOPGの破骨細胞形成抑制能を高めました。研究者たちはその理由を突き止めました:破骨細胞の発生過程で、成熟破骨細胞由来のプロテアーゼ(HTRA1を含む)がOPGを切断し、不活化してしまうのです。E123CaGが存在すると、OPGはこの分解から保護され、より長く完全体として残ります。したがって、TSP‑1のプロテオリシスで生じる同じ断片が、RANKの内的シグナルを抑えると同時にOPGを保護し、骨破壊に対する二重の制御層を強化します。
生体内で断片を試す
これらの効果が生体全体で重要かを確認するために、研究チームは骨へ優先的に転移するマウス乳がん細胞株を改変し、E123CaG断片を分泌させました。これらの細胞をマウスの血流に注入して骨転移を形成させると、E123CaG産生腫瘍を持つ動物は対照群より生存期間が延び、骨損傷も軽度でした。高分解能のマイクロCTスキャンでは、海綿骨(トラベキュラー骨)の保存状態が良く、梁が太く、梁間の隙間が小さいことが示されました。これらの利益は原発腫瘍の増殖速度に変化を伴わなかったため、この断片が主に骨の微小環境を修飾することで作用し、がん細胞自体を直接攻撃しているわけではないことが示唆されます。
患者にとっての意義
総じて、この研究は骨内に従来知られていなかった保護回路を明らかにします:破骨細胞はTSP‑1を切断して断片を生成し、その断片がさらに破骨細胞の活性化を抑え、体内の自然の阻害因子であるOPGを破壊から守ります。乳がんの骨転移という文脈では、この断片は破骨細胞の形成を遅らせ、マウスにおける破壊性病変の拡大を抑制します。治療へ応用するにはさらなる検証が必要ですが、E123CaGとそのRANKおよびOPGとの相互作用は、がんや過剰な骨喪失を特徴とする他の疾患に対して骨をよりよく保護する薬剤の有望なリードとなる可能性を示しています。
引用: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
キーワード: 骨転移, 破骨細胞, トロンボスポンジン‑1, RANKL RANK OPG, 骨改変