Clear Sky Science · it
Interazione di TSP-1 con RANK e OPG: implicazioni per il rimodellamento osseo e le metastasi ossee osteolitiche
Perché i tumori che distruggono l’osso sono importanti
Quando tumori come il carcinoma mammario si diffondono allo scheletro, possono causare dolorose “cavità” nell’osso che portano a fratture, debolezza e una qualità della vita ridotta. Queste lesioni nascono perché le cellule che normalmente rimodellano l’osso diventano iperattive e demolano troppo tessuto. Lo studio qui riassunto mette in luce un freno naturale all’interno di questo sistema: un frammento di una comune proteina della matrice che può ridurre la distruzione ossea e rallentare il danno osseo indotto dal cancro nei topi.
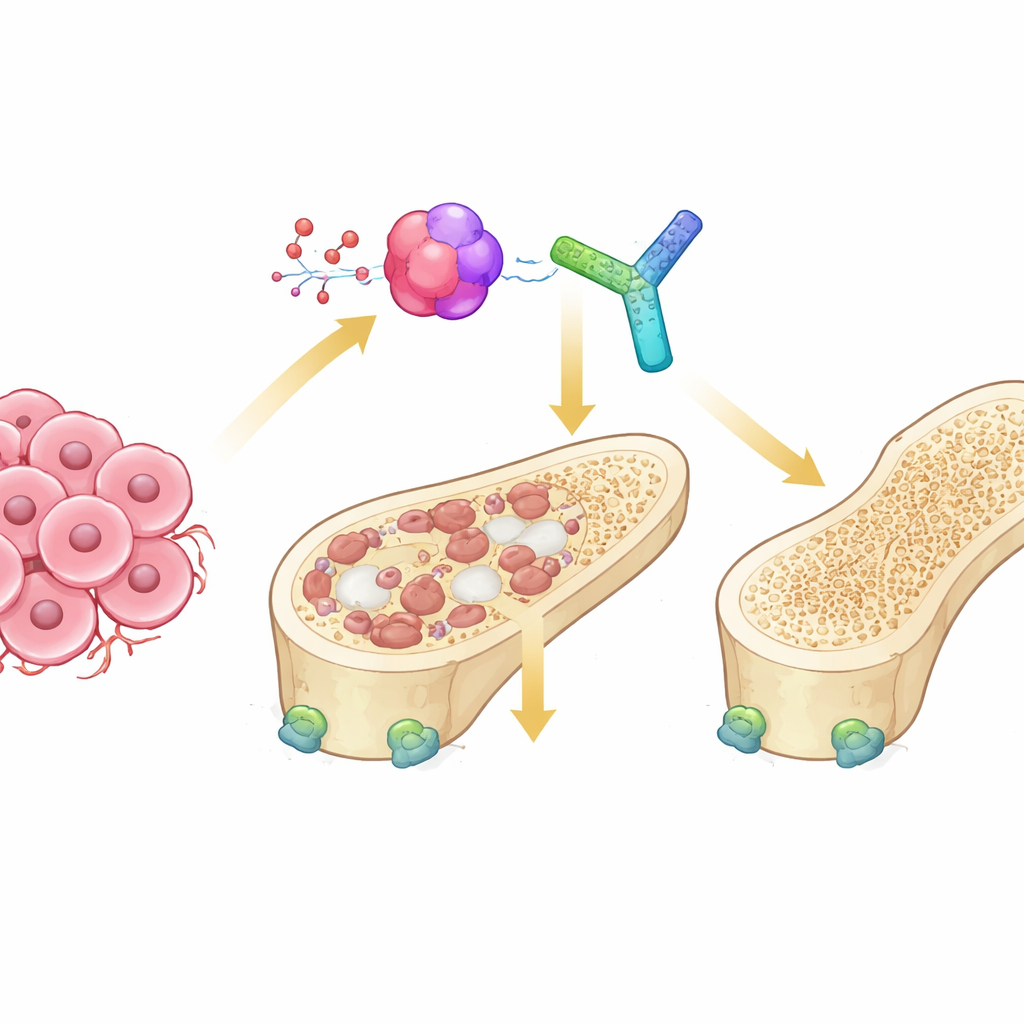
La lotta interna alle nostre ossa
Le ossa sane sono continuamente rinnovate da due tipi cellulari opposti. Gli osteoclasti degradano l’osso vecchio, mentre gli osteoblasti ne costruiscono di nuovo. Nei tumori che si diffondono all’osso questo equilibrio si perde: le cellule tumorali inviano segnali che iperstimolano gli osteoclasti, portando a lesioni “osteolitiche” in cui l’osso viene svuotato. Una linea di comunicazione chiave in questo processo è il sistema RANK–RANKL, che attiva la maturazione degli osteoclasti. Un terzo partner, l’osteoprotegerina (OPG), normalmente funge da dispositivo di sicurezza, legando RANKL e impedendogli di sovraattivare le cellule che consumano osso. Come questo trio venga regolato nel duro ambiente delle metastasi ossee non era chiaro.
Un aiuto sorprendente nascosto in una proteina più grande
I ricercatori si sono concentrati sulla trombospondina‑1 (TSP‑1), una grande proteina extracellulare nota per modellare l’architettura dei tessuti e il microambiente tumorale. Lavori precedenti suggerivano che la TSP‑1 a lunghezza intera possa in certe condizioni favorire la degradazione ossea. Qui il team ha esaminato una specifica porzione C-terminale di TSP‑1, chiamata E123CaG, che è priva di alcuni domini che stimolano gli osteoclasti. In colture cellulari hanno riscontrato che mentre la TSP‑1 intatta non modificava la formazione di osteoclasti indotta da RANKL, il frammento E123CaG riduceva fortemente il numero e le dimensioni degli osteoclasti maturi e interrompeva la struttura dell’anello di actina necessaria a queste cellule per riassorbire l’osso. Importante, gli osteoclasti maturi rilasciano essi stessi proteasi, in particolare un enzima chiamato HTRA1, che tagliano la TSP‑1 e generano un frammento simile a E123CaG — suggerendo che questo inibitore possa essere prodotto come controllo di retroazione intrinseco.
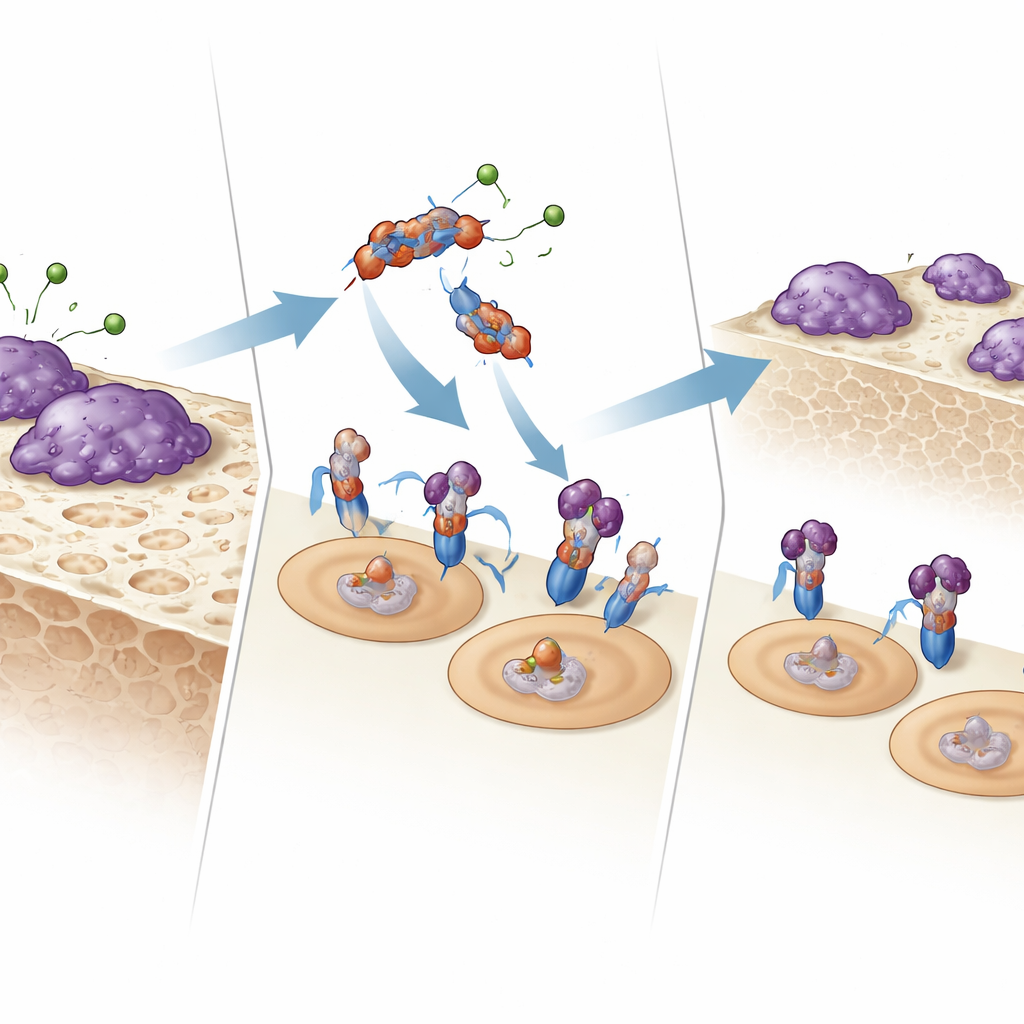
Come il frammento comunica con le cellule che mangiano l’osso
Per capire come funziona E123CaG, il team ha testato se si lega direttamente ai recettori che controllano gli osteoclasti. Usando risonanza plasmonica di superficie e saggi di legame in fase solida, hanno mostrato che E123CaG si attacca a RANK, il recettore sui precursori degli osteoclasti che rileva RANKL. Questo legame non impedisce a RANKL di associarsi, ma indebolisce il segnale a valle: le proteine di segnalazione precoci (MAPK p38 e JNK) si attivano meno intensamente e il fattore di trascrizione chiave NFATc1 entra nel nucleo in modo meno efficiente. Nel complesso, questi cambiamenti attenuano il programma di maturazione che normalmente trasforma i precursori in cellule pienamente attive nel riassorbimento osseo.
Proteggere il freno naturale alla perdita ossea
Il frammento fa più che interferire con la segnalazione di RANK. Si lega anche a OPG, il recettore spiazzante dell’organismo che sequestra RANKL. In coltura, E123CaG non impediva a OPG di catturare RANKL; al contrario, ne potenziava la capacità di inibire la formazione di osteoclasti. I ricercatori hanno scoperto il perché: durante lo sviluppo degli osteoclasti, proteasi rilasciate dagli osteoclasti maturi, incluso HTRA1, tagliano e inattivano OPG. Quando E123CaG era presente, OPG veniva protetto da questa degradazione, rimanendo intatto più a lungo. Così, lo stesso frammento generato dalla proteolisi di TSP‑1 attenua il segnale interno di RANK e preserva OPG, rafforzando due livelli di controllo sulla distruzione ossea.
Mettere alla prova il frammento in un organismo vivente
Per verificare se questi effetti contano in un organismo intero, il team ha ingegnerizzato una linea cellulare di carcinoma mammario murino che predilige la diffusione all’osso per secernere il frammento E123CaG. Quando queste cellule sono state iniettate nel flusso sanguigno dei topi per impiantare metastasi ossee, gli animali che ospitavano tumori produttrici di E123CaG sono sopravvissuti più a lungo e hanno mostrato danni ossei meno gravi rispetto ai controlli. Scansioni micro‑CT ad alta risoluzione hanno evidenziato una migliore conservazione dell’osso trabecolare (spugnoso), travi più spesse e spazi più piccoli tra di esse. Questi benefici si sono verificati senza variazioni nel tasso di crescita del tumore primario, suggerendo che il frammento agisca principalmente modificando il microambiente osseo piuttosto che attaccando direttamente le cellule tumorali.
Cosa significa per i pazienti
Nel complesso, i risultati rivelano un circuito protettivo precedentemente non riconosciuto nell’osso: gli osteoclasti rilasciano proteasi che scindono la TSP‑1 in un frammento che, a sua volta, limita l’ulteriore attivazione degli osteoclasti e protegge l’inibitore naturale dell’organismo, OPG, dalla distruzione. Nel contesto delle metastasi ossee del carcinoma mammario, questo frammento può rallentare la formazione di cellule che mangiano l’osso e limitare la diffusione di lesioni distruttive nei topi. Sebbene servano ulteriori studi prima di poter sviluppare una terapia, lo studio mette in evidenza E123CaG e le sue interazioni con RANK e OPG come piste promettenti per farmaci che potrebbero proteggere meglio le ossa nel cancro e in altre malattie caratterizzate da eccessiva perdita ossea.
Citazione: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Parole chiave: metastasi ossea, osteoclasti, trombospondina-1, RANKL RANK OPG, rimodellamento osseo