Clear Sky Science · nl
TSP-1-interactie met RANK en OPG: implicaties voor botremodellering en osteolytische botmetastasen
Waarom botaantastende vormen van kanker ertoe doen
Wanneer kanker, zoals bij borstkanker, naar het skelet uitzaait, kan dat pijnlijke “gaten” in het bot veroorzaken die leiden tot breuken, zwakte en een verminderde levenskwaliteit. Deze letsels ontstaan omdat cellen die normaal gesproken bot hervormen te actief worden en te veel weefsel afbreken. De hier samengevatte studie onthult een natuurlijke rem binnen dit systeem: een fragment van een veelvoorkomend bindweefsel‑eiwit dat botafbraak kan afremmen en kankergerelateerde botaantasting bij muizen vertraagt.
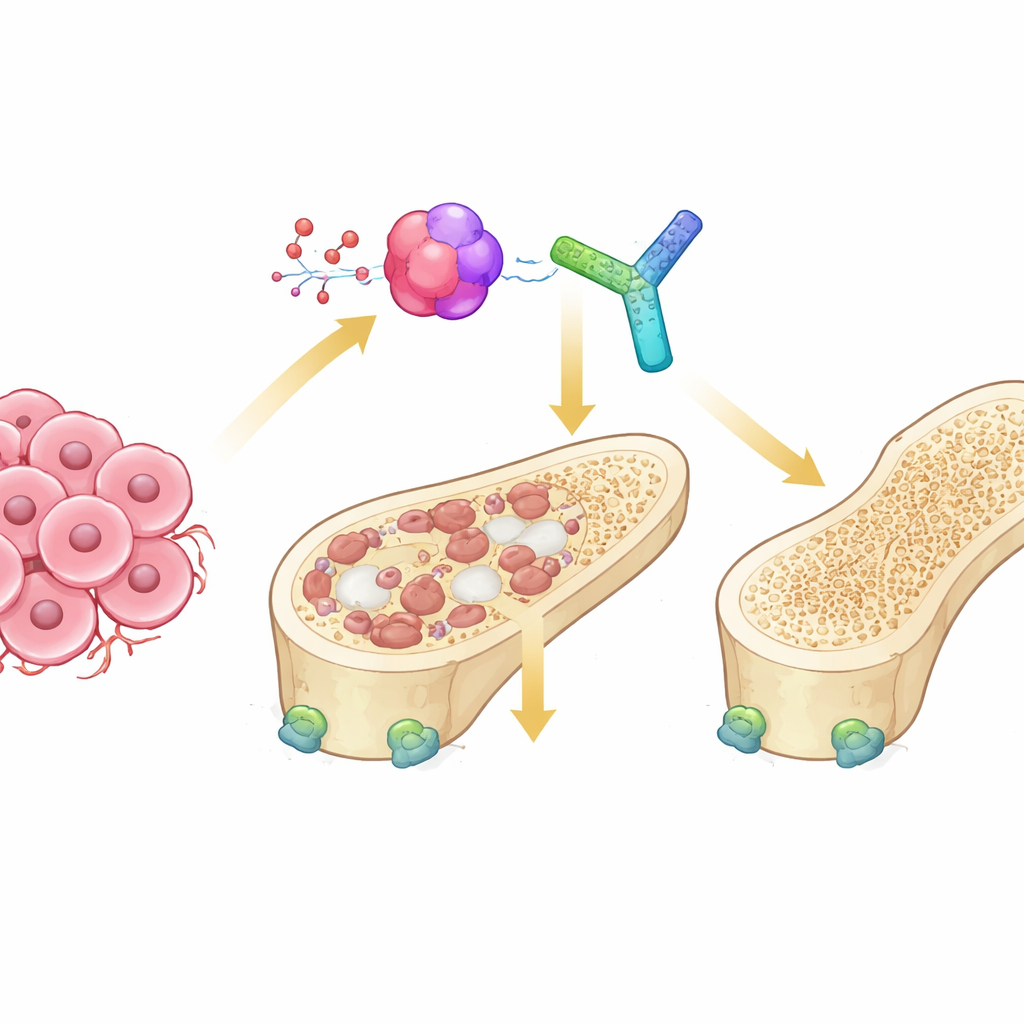
Het touwtrekken binnen ons bot
Gezonde botten worden voortdurend vernieuwd door twee tegengestelde celtypen. Osteoclasten breken oud bot af, terwijl osteoblasten nieuw bot opbouwen. Bij kanker die naar het bot uitzaait, raakt dit evenwicht verstoord: tumorcellen sturen signalen die osteoclasten overstimuleren, wat leidt tot «osteolytische» letsels waarbij bot wordt uitgehold. Een sleutelcommunicatielijn in dit proces is het RANK–RANKL-systeem, dat de rijping van osteoclasten inschakelt. Een derde partner, osteoprotegerine (OPG), fungeert normaal gesproken als een veiligheidsrem door RANKL te binden en te voorkomen dat het botetende cellen overactiveert. Hoe deze drie-eenheid wordt bijgestuurd in de vijandige omgeving van botmetastasen was onduidelijk.
Een verrassende helper verborgen in een groter eiwit
De onderzoekers richtten zich op thrombospondine‑1 (TSP‑1), een groot extracellulair eiwit dat het weefselkader en het tumormicro‑milieu vormt. Eerder werk suggereerde dat volledig TSP‑1 onder bepaalde omstandigheden botafbraak juist kan bevorderen. Hier onderzocht het team een specifiek C‑terminaal deel van TSP‑1, genoemd E123CaG, dat enkele domeinen mist die osteoclasten stimuleren. In celkweken vonden ze dat terwijl intact TSP‑1 de door RANKL geïnduceerde osteoclastvorming niet veranderde, het E123CaG‑fragment het aantal en de grootte van rijpe osteoclasten sterk verminderde en de actineringstructuur die deze cellen nodig hebben om bot te resorberen verstoorde. Belangrijk is dat rijpe osteoclasten zelf proteasen afgeven, met name een enzym HTRA1, dat TSP‑1 doorsnijdt en een fragment genereert dat lijkt op E123CaG — wat suggereert dat deze remmer kan ontstaan als ingebouwde negatieve terugkoppeling.
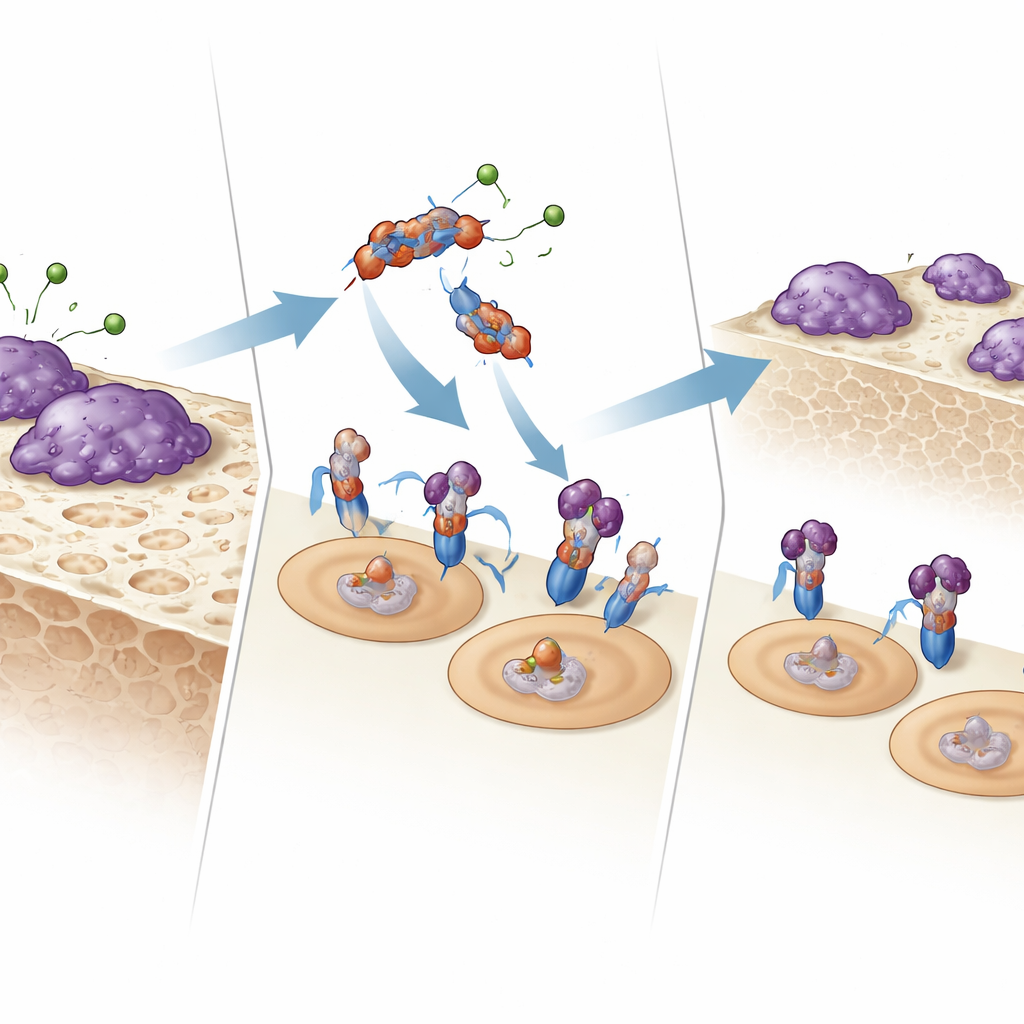
Hoe het fragment met botetende cellen communiceert
Om te begrijpen hoe E123CaG werkt, testte het team of het direct bindt aan de receptoren die osteoclasten aansturen. Met oppervlakteplasmaresonantie en vastfase-bindingsassays lieten ze zien dat E123CaG zich hecht aan RANK, de receptor op osteoclastvoorlopers die RANKL detecteert. Deze binding verhindert niet dat RANKL zich bindt, maar verlaagt wel het downstreamsignaal: vroege signaalmoleculen (MAPKs p38 en JNK) worden minder sterk geactiveerd en de belangrijke transcriptiefactor NFATc1 verplaatst zich minder efficiënt naar de celkern. Gezamenlijk dempen deze veranderingen het rijpingsprogramma dat normaal voorlopers tot volledig actieve botresorberende cellen omzet.
De natuurlijke rem op botverlies beschermen
Het fragment doet meer dan alleen RANK‑signaal verstoren. Het bindt ook aan OPG, de eigen decoy‑receptor van het lichaam die RANKL wegvangt. In kweek remde E123CaG OPG niet in het vastleggen van RANKL; in plaats daarvan versterkte het OPG’s vermogen om osteoclastvorming te verhinderen. De onderzoekers ontdekten waarom: tijdens de ontwikkeling van osteoclasten knippen proteasen van rijpe osteoclasten, waaronder HTRA1, OPG in stukjes en inactiveren het. Wanneer E123CaG aanwezig was, werd OPG beschermd tegen deze afbraak en bleef het langer intact. Zo dempt hetzelfde fragment, dat door proteolyse van TSP‑1 ontstaat, zowel RANK’s interne signaal als de degradatie van OPG, waarmee twee lagen van controle over botafbraak worden versterkt.
Het fragment in een levend systeem testen
Om te zien of deze effecten in een geheel organisme relevant zijn, maakte het team een muis‑borstkankercellijn die bij voorkeur naar bot uitzaait en E123CaG uitscheidt. Wanneer deze cellen in de bloedbaan van muizen werden ingebracht om botmetastasen te zaaien, overleefden dieren met E123CaG‑producerende tumoren langer en hadden ze minder ernstige botaantasting dan controles. Hoogresolutie micro‑CT‑scans toonden een betere instandhouding van trabeculair (sponsachtig) bot, dikkere strengen en kleinere tussenruimten. Deze voordelen traden op zonder veranderingen in de groei van de primaire tumor, wat suggereert dat het fragment voornamelijk werkt door het botmicro‑milieu te wijzigen en niet door direct kankercellen aan te vallen.
Wat dit betekent voor patiënten
Samengevat onthullen de bevindingen een eerder onerkende beschermende schakeling in bot: osteoclasten scheiden proteasen uit die TSP‑1 in een fragment knippen dat op zijn beurt verdere activatie van osteoclasten tempert en de natuurlijke remmer OPG beschermt tegen vernietiging. In de context van borstkanker‑botmetastasen kan dit fragment de vorming van botetende cellen vertragen en de uitbreiding van destructieve letsels bij muizen beperken. Hoewel er meer onderzoek nodig is voordat uit dit inzicht een therapie kan volgen, benadrukt de studie E123CaG en zijn interacties met RANK en OPG als veelbelovende aanknopingspunten voor middelen die botten bij kanker en andere ziekten met overmatig botverlies beter zouden kunnen beschermen.
Bronvermelding: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Trefwoorden: botmetastasen, osteoclasten, thrombospondine-1, RANKL RANK OPG, botremodellering