Clear Sky Science · pl
Interakcja TSP-1 z RANK i OPG: implikacje dla przebudowy kości i osteolitycznych przerzutów do kości
Dlaczego nowotwory niszczące kości mają znaczenie
Gdy nowotwory, takie jak rak piersi, rozprzestrzeniają się do szkieletu, mogą wywoływać bolesne „dziury” w kościach prowadzące do złamań, osłabienia i pogorszenia jakości życia. Zmiany te powstają, ponieważ komórki odpowiedzialne za przebudowę kości stają się nadaktywne i rozkładają zbyt wiele tkanki. Badanie opisane tutaj ujawnia naturalny hamulec w tym systemie: fragment powszechnego białka tkanki łącznej, który potrafi zmniejszyć niszczenie kości i spowolnić uszkodzenia kości wywołane przez nowotwór u myszy.
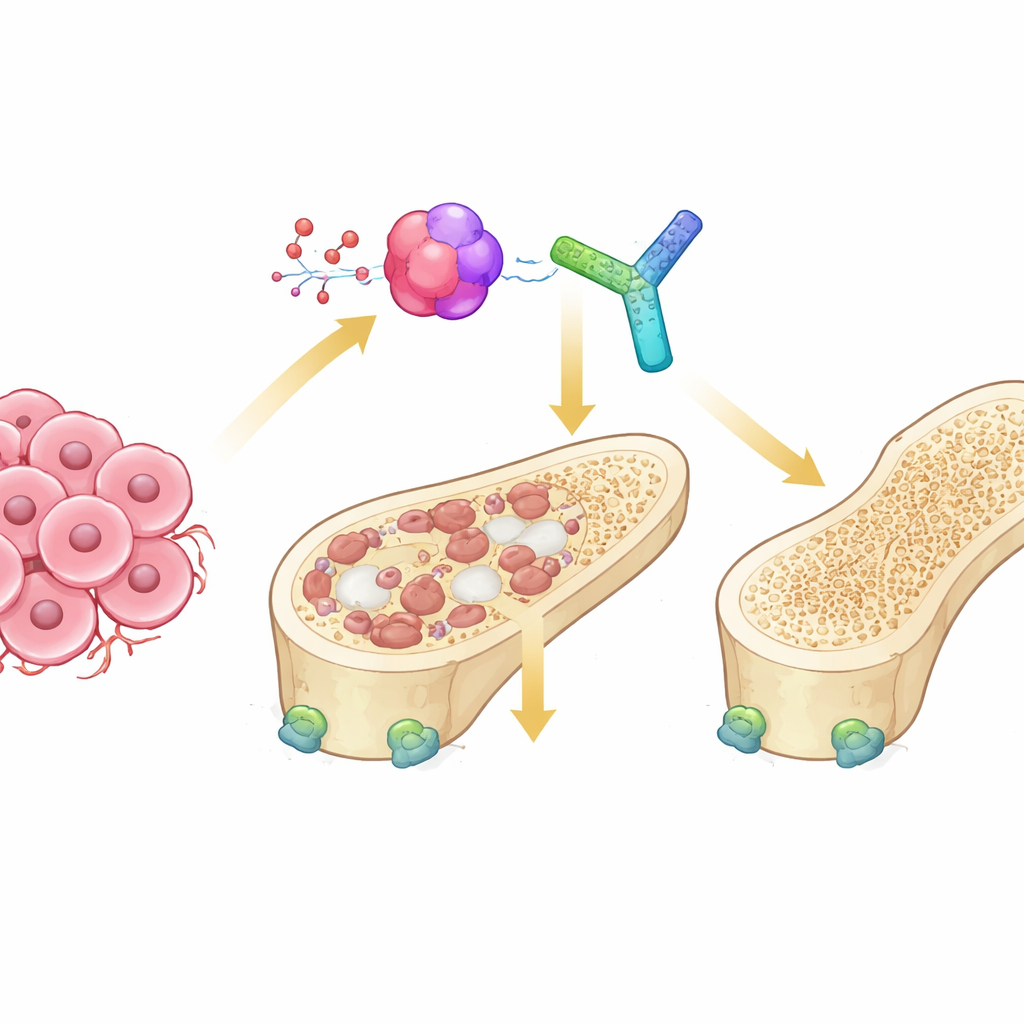
Siłowanie się wewnątrz naszych kości
Zdrowe kości są nieustannie odnawiane przez dwa przeciwstawne typy komórek. Osteoklasty rozkładają starą kość, a osteoblasty budują nową. W nowotworach, które dają przerzuty do kości, ta równowaga zostaje zachwiana: komórki nowotworowe wysyłają sygnały nadmiernie pobudzające osteoklasty, prowadząc do zmian „osteolitycznych”, w których kość jest wydrążana. Kluczową linią komunikacji w tym procesie jest układ RANK–RANKL, który uruchamia dojrzewanie osteoklastów. Trzeci partner, osteoprotegeryna (OPG), normalnie działa jak zabezpieczenie, wiążąc RANKL i uniemożliwiając mu nadmierne aktywowanie komórek trawiących kość. Sposób, w jaki to trio jest regulowane w surowym środowisku przerzutów kostnych, pozostawał niejasny.
Zaskakujący pomocnik ukryty w większym białku
Naukowcy skupili się na trombospondynie‑1 (TSP‑1), dużym białku zewnątrzkomórkowym znanym z kształtowania architektury tkanek i mikrośrodowiska nowotworowego. Wcześniejsze prace sugerowały, że pełnej długości TSP‑1 może w niektórych warunkach sprzyjać niszczeniu kości. W tej pracy zespół badał konkretny fragment C‑końcowy TSP‑1, nazwany E123CaG, któremu brakuje niektórych domen stymulujących osteoklasty. W hodowlach komórkowych stwierdzono, że podczas gdy niezmieniona TSP‑1 nie zmieniała tworzenia osteoklastów indukowanego przez RANKL, fragment E123CaG wyraźnie zmniejszał liczbę i rozmiar dojrzałych osteoklastów oraz zaburzał pierścieniową strukturę aktyny, której te komórki potrzebują do resorpcji kości. Co ważne, same dojrzałe osteoklasty uwalniają proteazy, zwłaszcza enzym HTRA1, który przecina TSP‑1 i generuje fragment podobny do E123CaG — co sugeruje, że ten inhibitor może powstawać jako wbudowana kontrola zwrotna.
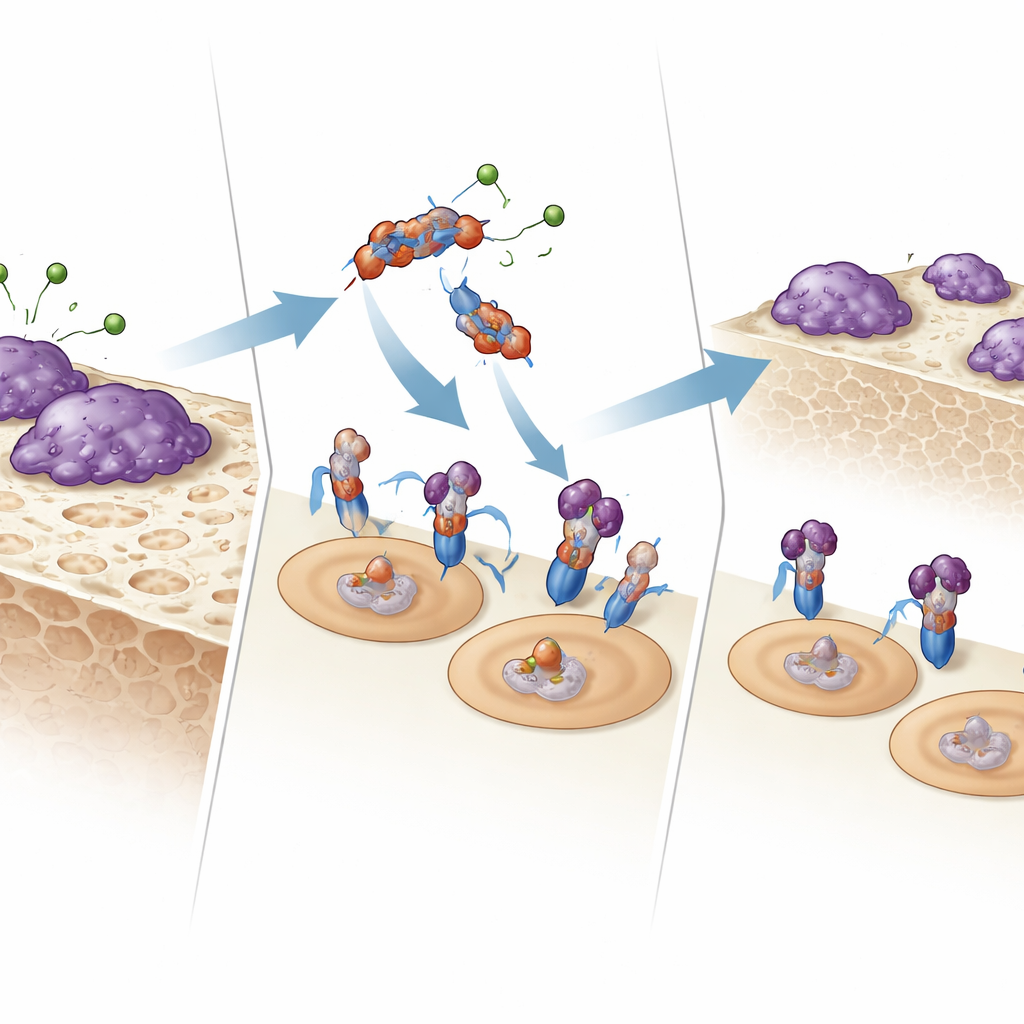
Jak fragment komunikuje się z komórkami trawiącymi kość
Aby zrozumieć działanie E123CaG, zespół sprawdził, czy wiąże się on bezpośrednio z receptorami kontrolującymi osteoklasty. Za pomocą spektrometrii powierzchniowej z plazmonem i testów wiązania w fazie stałej wykazali, że E123CaG przyłącza się do RANK — receptora na prekursorach osteoklastów wyczuwającego RANKL. To wiązanie nie blokuje dokowania RANKL, ale osłabia sygnał w dół szlaku: wczesne białka sygnałowe (MAPK p38 i JNK) aktywują się słabiej, a kluczowy czynnik transkrypcyjny NFATc1 przechodzi do jądra mniej wydajnie. Te zmiany razem tłumią program dojrzewania, który normalnie przekształca prekursory w w pełni aktywne komórki resorbujące kość.
Ochrona naturalnego hamulca przed utratą kości
Fragment robi więcej niż tylko zakłóca sygnalizację RANK. Wiąże się także z OPG, naturalnym atrapowym receptorem organizmu, który pochłania RANKL. W hodowli E123CaG nie uniemożliwiał OPG wychwytania RANKL; przeciwnie, wzmacniał zdolność OPG do hamowania powstawania osteoklastów. Naukowcy wyjaśnili dlaczego: podczas dojrzewania osteoklastów proteazy pochodzące z dojrzałych osteoklastów, w tym HTRA1, rozcinają i unieczynniają OPG. W obecności E123CaG OPG był chroniony przed tym rozkładem i pozostawał nienaruszony dłużej. Tak więc ten sam fragment powstający w wyniku proteolizy TSP‑1 zarówno osłabia wewnętrzny sygnał RANK, jak i zachowuje OPG, wzmacniając dwie warstwy kontroli nad niszczeniem kości.
Testowanie fragmentu w żywym organizmie
Aby sprawdzić, czy te efekty mają znaczenie w całym organizmie, zespół zmodyfikował linię mysiego raka piersi, wykazującą skłonność do przerzutów do kości, tak aby wydzielała fragment E123CaG. Gdy te komórki wstrzyknięto do krwiobiegu myszy w celu zainicjowania przerzutów kostnych, zwierzęta noszące guzy produkujące E123CaG przeżywały dłużej i miały mniej nasilone uszkodzenia kości niż kontrole. Badania za pomocą wysokorozdzielczej mikro‑CT wykazały lepsze zachowanie kości beleczkowej (gąbczastej), grubsze przegrody i mniejsze przerwy między nimi. Korzyści te występowały bez zmian w tempie wzrostu guza pierwotnego, co sugeruje, że fragment działa przede wszystkim przez modyfikację mikrośrodowiska kostnego, a nie przez bezpośrednie atakowanie komórek nowotworowych.
Co to oznacza dla pacjentów
Podsumowując, wyniki ujawniają wcześniej nierozpoznany obwód ochronny w kości: osteoklasty uwalniają proteazy, które tną TSP‑1 na fragment, który z kolei tłumi dalszą aktywację osteoklastów i chroni naturalnego inhibitora OPG przed zniszczeniem. W kontekście przerzutów raka piersi do kości ten fragment może spowalniać powstawanie komórek trawiących kość i ograniczać rozwój destrukcyjnych zmian u myszy. Chociaż przed opracowaniem terapii potrzebne są dalsze badania, praca wskazuje E123CaG i jego interakcje z RANK i OPG jako obiecujące cele dla leków, które mogłyby lepiej chronić kości przy nowotworach i innych chorobach charakteryzujących się nadmierną utratą kości.
Cytowanie: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Słowa kluczowe: przerzuty do kości, osteoklasty, trombospondyna-1, RANKL RANK OPG, przebudowa kości