Clear Sky Science · ar
تفاعل TSP-1 مع RANK و OPG: تداعيات على إعادة تشكيل العظام والنقائل العظمية التحلّلية
لماذا تهم السرطانات المدمِّرة للعظام
عندما تنتشر سرطانات مثل سرطان الثدي إلى الهيكل العظمي، يمكن أن تثير ثقوباً مؤلمة في العظم تؤدي إلى كسور وضعف وتردّ في جودة الحياة. تنشأ هذه الآفات لأن الخلايا المسؤولة عادة عن إعادة تشكيل العظم تصبح مفرطة النشاط وتؤكل نسيج العظم أكثر من اللازم. تكشف الدراسة الملخّصة هنا عن فرامل طبيعية داخل هذا النظام: جزء من بروتين نسيجي شائع يستطيع تقليل تدمير العظم وإبطاء الضرر العظمي الناجم عن السرطان في الفئران.
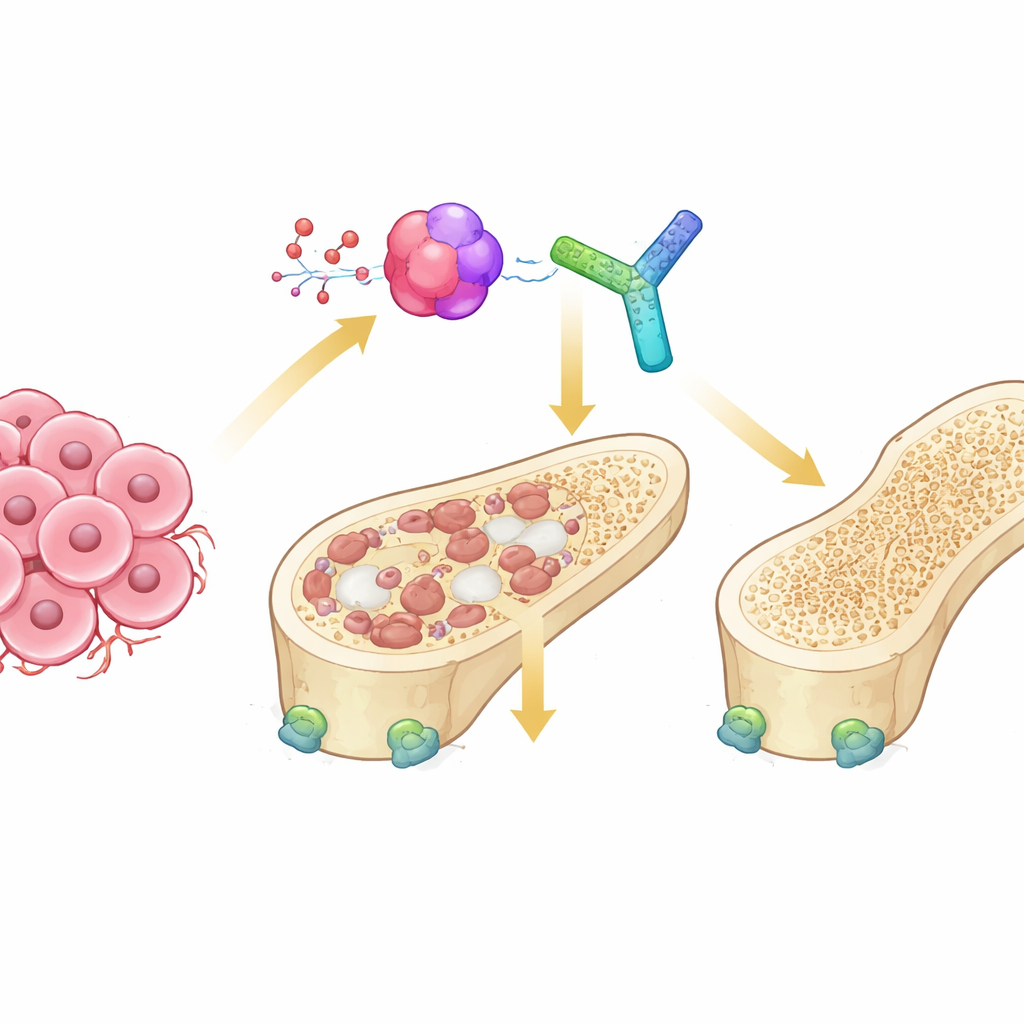
الصراع داخل عظامنا
تتجدد العظام السليمة باستمرار بواسطة نوعين من الخلايا المتقابلة. تفرّغ الخلايا الناقضة للعظم العظم القديم، بينما تبني الخلايا البانية للعظم عظماً جديداً. في السرطانات التي تنتشر إلى العظم يُفقد هذا التوازن: ترسل الخلايا الورمية إشارات تفرط في تحفيز الخلايا الناقضة، ما يؤدي إلى آفات «تحلُّلية» حيث يُفرغ العظم من داخله. أحد خطوط الاتصال الرئيسية في هذه العملية هو نظام RANK–RANKL، الذي يشغّل نضج الخلايا الناقضة للعظم. شريك ثالث، أوستيوبروتيجيرين (OPG)، يعمل عادة كقفل أمان، يلتصق بـRANKL ويمنعه من تنشيط خلايا أكل العظم المفرطة. كيف يُضبط هذا الثلاثي في بيئة النقائل العظمية القاسية ظل أمراً غير واضح.
مساعد مفاجئ مخفي في بروتين أكبر
ركز الباحثون على ثرومبوسبودين‑1 (TSP‑1)، بروتين خارج خلوي كبير معروف بتشكيل بنية الأنسجة وبيئات الأورام. أشارت أعمال سابقة إلى أن TSP‑1 كامل الطول قد يشجع تحلل العظم في بعض الظروف. هنا فحص الفريق جزءاً محدداً من الطرف الكربوكسيلي لـTSP‑1 يُدعى E123CaG، الذي يفتقر إلى بعض النطاقات التي تحفز الخلايا الناقضة. في مزروعات خلوية وجدوا أنه بينما لم يغير TSP‑1 الكامل تكوين الخلايا الناقضة المحفزة بواسطة RANKL، قلّل شظية E123CaG بقوة من عدد وحجم الخلايا الناقضة الناضجة وعطّلت بنية حلقة الأكتين التي تحتاجها هذه الخلايا لهضم العظم. والأهم أن الخلايا الناقضة الناضجة نفسها تفرز بروتيازات، خصوصاً إنزيماً اسمه HTRA1، يقطع TSP‑1 ويولد شظية مشابهة لـE123CaG—مما يلمّح إلى أن هذا المثبّط قد يُنتَج كآلية تغذية راجعة مدمجة.
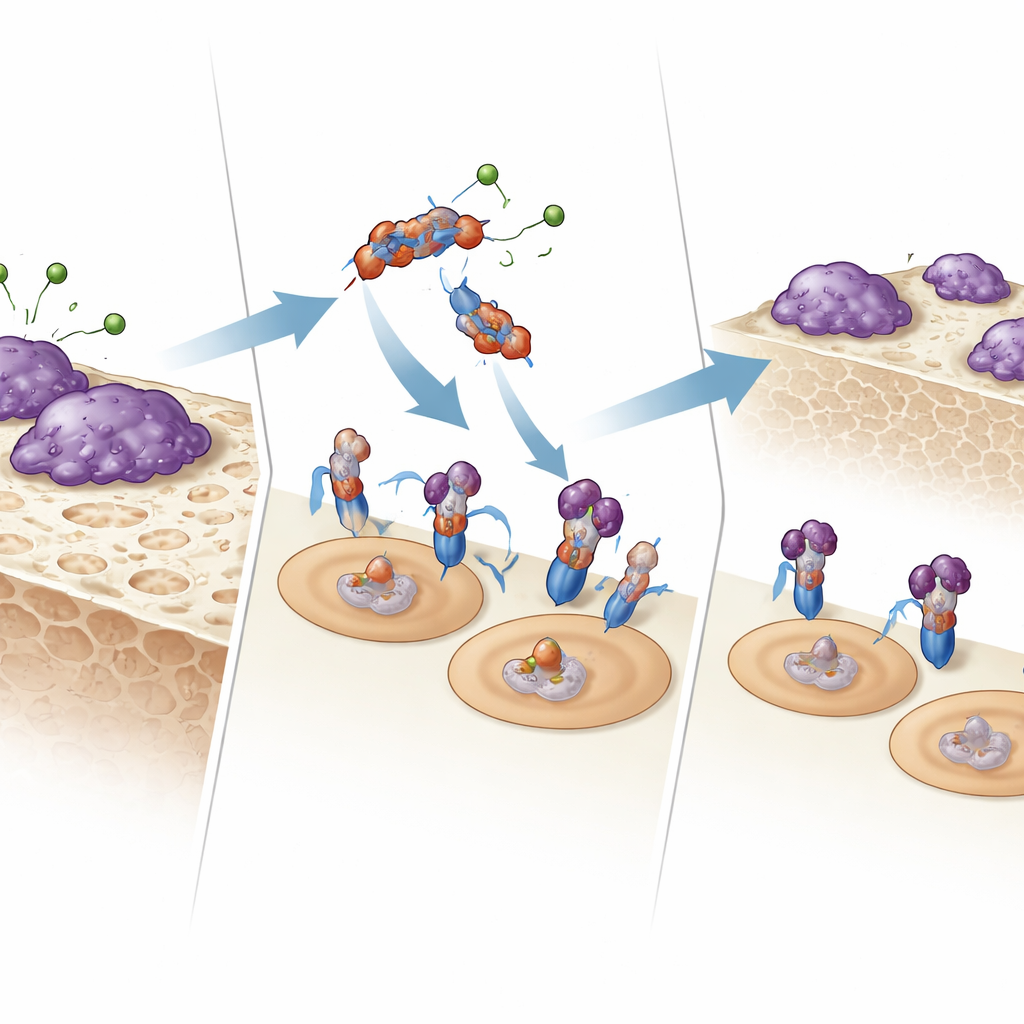
كيف تتواصل الشظية مع خلايا أكل العظم
لفهم آلية عمل E123CaG، اختبر الفريق ما إذا كانت الشظية ترتبط مباشرة بالمستقبلات التي تتحكم في الخلايا الناقضة. باستخدام رنين بلازما السطح وتجارب ربط طور صلب، أظهروا أن E123CaG تلتصق بـRANK، مستقبل محضّرات الخلايا الناقضة الذي يستشعر RANKL. هذا الارتباط لا يمنع RANKL من الالتحام، لكنه يضعف الإشارة اللاحقة: بروتينات الإشارة المبكرة (الـMAPKs p38 و JNK) تنشط بدرجة أقل، والعامل النسخي الرئيسي NFATc1 يدخل النواة بكفاءة أقل. مجتمعة، تقلل هذه التغيرات من برنامج النضج الذي يحوّل المحضّرات إلى خلايا فعّالة قادرة على إذابة العظم.
حماية فرامل الجسم الطبيعية لفقدان العظم
لا تقتصر تأثيرات الشظية على تعطيل إشارة RANK. فهي أيضاً ترتبط بـOPG، مستقبل الطعم الطبيعي الذي يلتقط RANKL. في الثقافة الخلوية، لم تمنع E123CaG OPG من التقاط RANKL؛ بل عزّزت قدرة OPG على تثبيط تكوين الخلايا الناقضة. اكتشف الباحثون السبب: خلال تطور الخلايا الناقضة، تقطع بروتيازات من الخلايا الناقضة الناضجة، بما في ذلك HTRA1، OPG وتُعطّلها. عندما كانت E123CaG موجودة، حُمِيَت OPG من هذا التحلل وبقيت سليمة لفترة أطول. هكذا، فإن الشظية نفسها الناتجة عن تحلل TSP‑1 تُضعف إشارة RANK الداخلية وتحافظ على OPG، معززةً طبقتين من الضبط على تدمير العظم.
اختبار الشظية في نظام حي
للتأكد ما إذا كانت هذه التأثيرات مهمة في كائن كامل، مهّند الفريق سلالة خلوية سرطانية ثديية للفئران تُفضّل الانتشار إلى العظم لتفرز شظية E123CaG. عندما حقنوا هذه الخلايا في مجرى الدم للفئران لتؤسس نقائل عظمية، عاشت الحيوانات الحاملة لأورام منتجة لـE123CaG فترة أطول وكان لديها تلف عظمي أقل حدة مقارنةً بالمجموعة الضابطة. أظهرت فحوصات التصوير الميكرو‑مقطعي عالية الدقة حفاظاً أفضل على العظم الإسفنجي، وعوارض أكثر سمكاً، وفراغات أصغر بينها. حدثت هذه الفوائد دون تغيُّر في معدل نمو الورم الأساسي، ما يشير إلى أن الشظية تعمل بشكل أساسي عن طريق تعديل البيئة الميكروية للعظم بدلاً من مهاجمة الخلايا السرطانية مباشرة.
ماذا يعني هذا للمرضى
تجتمع النتائج لتكشف عن دائرة حماية لم تُعرف سابقاً في العظم: تفرز الخلايا الناقضة بروتيازات تقص TSP‑1 إلى شظية تُثبِّط بدورها مزيداً من تنشيط الخلايا الناقضة وتحمي مثبط الجسم الطبيعي OPG من التدمير. في سياق نقائل سرطان الثدي إلى العظم، تستطيع هذه الشظية إبطاء تكوّن خلايا أكل العظم والحد من انتشار الآفات المدمرة في الفئران. ومع أن ثمة حاجة لمزيد من العمل قبل تطوير أي علاج، تبرز الدراسة E123CaG وتفاعلاتها مع RANK وOPG كدلائل واعدة لتطوير أدوية قد تحمي العظام بشكل أفضل في السرطان وغيره من الأمراض المصحوبة بفقدان عظمي مفرط.
الاستشهاد: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
الكلمات المفتاحية: نقائل عظمية, خلايا ناقضة للعظم, ثرومبوسبودين-1, RANKL RANK OPG, إعادة تشكيل العظام