Clear Sky Science · pt
Interação de TSP‑1 com RANK e OPG: implicações para remodelamento ósseo e metástase óssea osteolítica
Por que os cânceres que destroem os ossos importam
Quando cânceres como o de mama se espalham para o esqueleto, podem provocar “buracos” dolorosos no osso que levam a fraturas, fraqueza e piora da qualidade de vida. Essas lesões surgem porque células que normalmente remodelam o osso ficam hiperativas e degradam tecido em excesso. O estudo resumido aqui revela um freio natural nesse sistema: um fragmento de uma proteína comum do tecido conjuntivo que consegue reduzir a destruição óssea e retardar o dano ósseo induzido por câncer em camundongos.
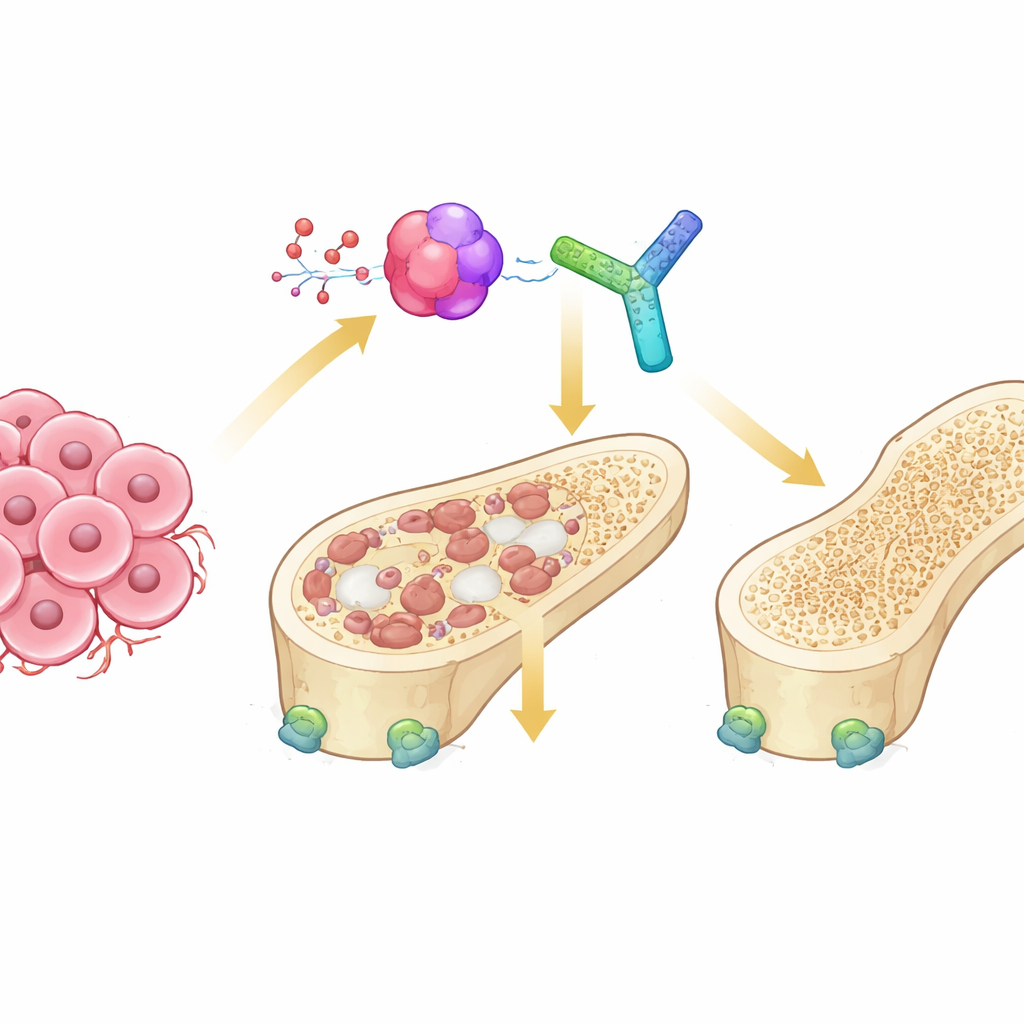
A disputa dentro dos nossos ossos
Ossos saudáveis são constantemente renovados por dois tipos celulares opostos. Osteoclastos degradam o osso antigo, enquanto osteoblastos constroem osso novo. Em cânceres que atingem o osso, esse equilíbrio se perde: células tumorais enviam sinais que superestimulam os osteoclastos, levando a lesões “osteolíticas” em que o osso é escavado. Uma via de comunicação chave nesse processo é o sistema RANK–RANKL, que liga a maturação dos osteoclastos. Um terceiro parceiro, a osteoprotegerina (OPG), normalmente atua como um trava‑segurança, ligando‑se ao RANKL e impedindo que ele superative as células que comem osso. Como esse trio é afinado no ambiente hostil das metástases ósseas não estava claro.
Um ajudante surpreendente escondido em uma proteína maior
Os pesquisadores focaram na trombospondina‑1 (TSP‑1), uma grande proteína extracelular conhecida por moldar a arquitetura tecidual e o microambiente tumoral. Trabalhos anteriores sugeriam que a TSP‑1 intacta pode, em certas condições, favorecer a degradação óssea. Aqui, a equipe examinou uma porção C‑terminal específica da TSP‑1, chamada E123CaG, que carece de alguns domínios que estimulam osteoclastos. Em culturas celulares, descobriram que, enquanto a TSP‑1 intacta não alterou a formação de osteoclastos induzida por RANKL, o fragmento E123CaG reduziu fortemente o número e o tamanho de osteoclastos maduros e perturbou o anel de actina que essas células precisam para reabsorver o osso. Importante: os próprios osteoclastos maduros liberam proteases, especialmente uma enzima chamada HTRA1, que cortam a TSP‑1 e geram um fragmento semelhante ao E123CaG — sugerindo que esse inibidor pode ser produzido como um mecanismo de realimentação intrínseco.
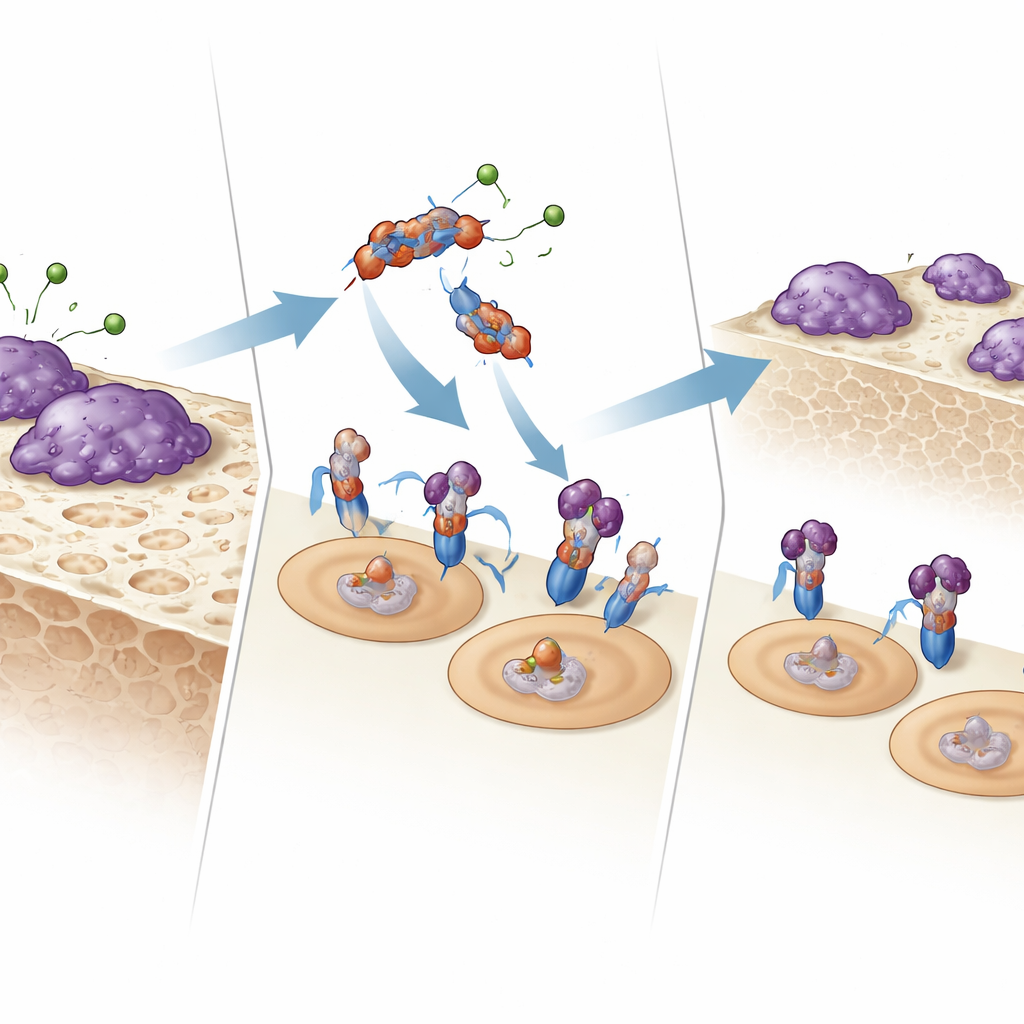
Como o fragmento se comunica com as células que comem osso
Para entender como o E123CaG funciona, a equipe testou se ele se liga diretamente aos receptores que controlam os osteoclastos. Usando ressonância de plasmão de superfície e ensaios de ligação em fase sólida, mostraram que o E123CaG se anexa ao RANK, o receptor em precursores de osteoclastos que detecta o RANKL. Essa ligação não impede o encaixe do RANKL, mas enfraquece o sinal a jusante: proteínas de sinalização precoces (MAPKs p38 e JNK) ativam‑se menos intensamente, e o fator de transcrição chave NFATc1 transloca‑se para o núcleo com menor eficiência. Em conjunto, essas mudanças atenuam o programa de maturação que normalmente converte precursores em células totalmente ativas que reabsorvem o osso.
Preservando o freio natural contra a perda óssea
O fragmento faz mais do que interferir na sinalização de RANK. Ele também se liga à OPG, o receptor‑cebo do organismo que neutraliza o RANKL. Em cultura, o E123CaG não impediu que a OPG capturasse o RANKL; em vez disso, aumentou a capacidade da OPG de inibir a formação de osteoclastos. Os pesquisadores descobriram o porquê: durante o desenvolvimento dos osteoclastos, proteases liberadas por osteoclastos maduros, incluindo a HTRA1, fragmentam e inativam a OPG. Quando o E123CaG estava presente, a OPG foi protegida dessa degradação, permanecendo intacta por mais tempo. Assim, o mesmo fragmento gerado pela proteólise da TSP‑1 tanto atenua o sinal interno de RANK quanto preserva a OPG, reforçando duas camadas de controle sobre a destruição óssea.
Testando o fragmento em um sistema vivo
Para ver se esses efeitos importam em um organismo inteiro, a equipe engenheirou uma linha de células de câncer de mama de camundongo com tropismo para osso para secretar o fragmento E123CaG. Quando essas células foram injetadas na corrente sanguínea de camundongos para semear metástases ósseas, os animais com tumores produtores de E123CaG sobreviveram mais e apresentaram danos ósseos menos severos do que os controles. Tomografias micro‑CT de alta resolução mostraram melhor preservação do osso trabecular (esponjoso), vigas mais espessas e espaços menores entre elas. Esses benefícios ocorreram sem alterações na taxa de crescimento do tumor primário, sugerindo que o fragmento age principalmente modificando o microambiente ósseo em vez de atacar diretamente as células cancerosas.
O que isto significa para pacientes
Em conjunto, os achados revelam um circuito protetor previamente não reconhecido no osso: osteoclastos liberam proteases que clivam a TSP‑1 em um fragmento que, por sua vez, reprime a ativação adicional de osteoclastos e protege o inibidor natural do corpo, a OPG, da destruição. No contexto de metástase óssea de câncer de mama, esse fragmento pode retardar a formação de células que comem osso e limitar a propagação de lesões destrutivas em camundongos. Embora seja necessário mais trabalho antes que qualquer terapia possa ser desenvolvida, o estudo destaca o E123CaG e suas interações com RANK e OPG como pistas promissoras para fármacos que poderiam proteger melhor os ossos em cânceres e outras doenças marcadas por perda óssea excessiva.
Citação: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Palavras-chave: metástase óssea, osteoclastos, trombospondina‑1, RANKL RANK OPG, remodelamento ósseo