Clear Sky Science · fr
Interaction TSP-1 avec RANK et OPG : implications pour le remodelage osseux et les métastases osseuses ostéolytiques
Pourquoi les cancers destructeurs d’os comptent
Lorsque des cancers comme le cancer du sein se propagent au squelette, ils peuvent provoquer des « trous » douloureux dans l’os qui entraînent des fractures, une faiblesse et une baisse de la qualité de vie. Ces lésions apparaissent parce que les cellules qui remodèlent normalement l’os deviennent hyperactives et dégradent trop de tissu. L’étude résumée ici révèle un frein naturel au sein de ce système : un fragment d’une protéine de la matrice courante qui peut réduire la destruction osseuse et ralentir les dégâts osseux induits par le cancer chez la souris.
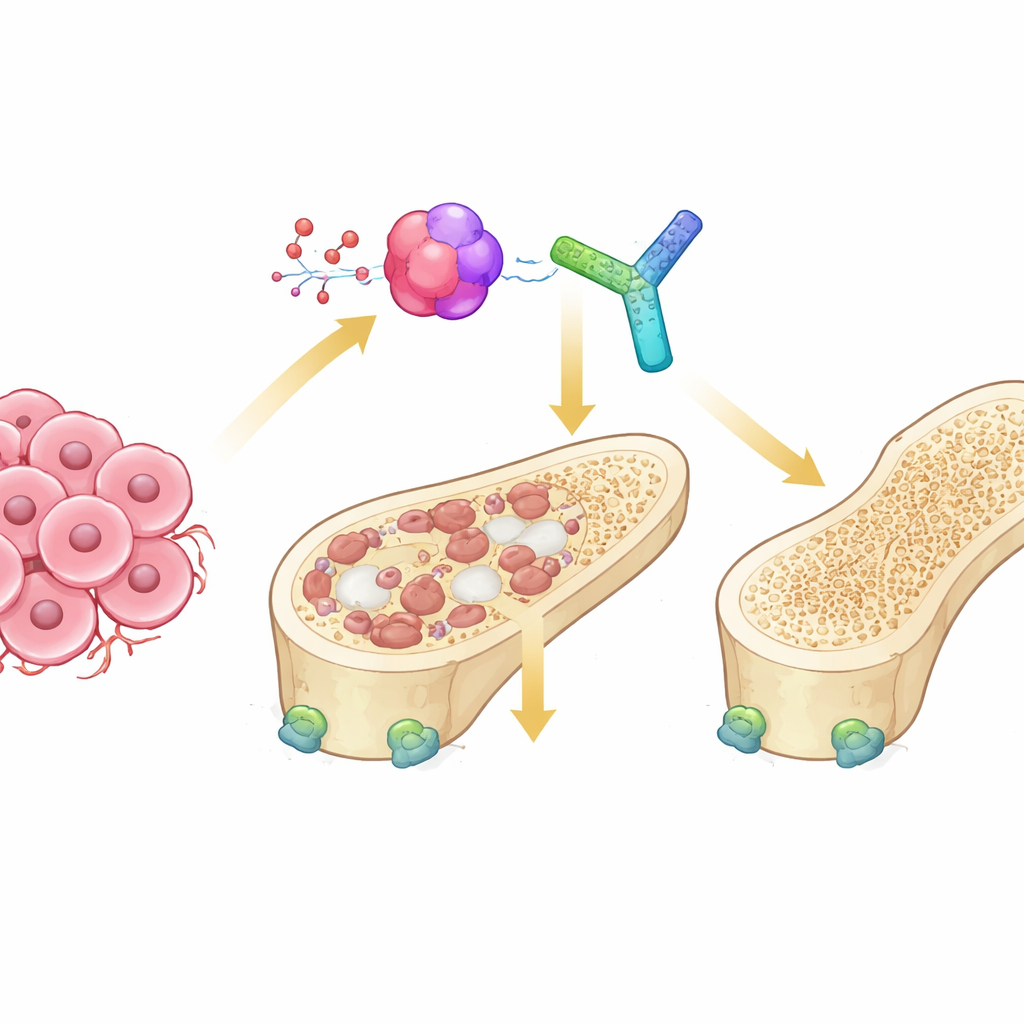
La lutte intérieure dans nos os
Les os sains sont constamment renouvelés par deux types cellulaires opposés. Les ostéoclastes dégradent l’os ancien, tandis que les ostéoblastes fabriquent du nouvel os. Dans les cancers qui métastasent vers l’os, cet équilibre est rompu : les cellules tumorales envoient des signaux qui surexcitent les ostéoclastes, conduisant à des lésions « ostéolytiques » où l’os est creusé. Une voie de communication clé dans ce processus est le système RANK–RANKL, qui déclenche la maturation des ostéoclastes. Un troisième partenaire, l’ostéoprotégérine (OPG), agit normalement comme une sécurité, se liant à RANKL et l’empêchant de surexciter les cellules qui rongent l’os. La manière dont ce trio est finement régulé dans l’environnement hostile des métastases osseuses restait peu claire.
Un assistant surprenant caché dans une plus grosse protéine
Les chercheurs se sont intéressés à la thrombospondine‑1 (TSP‑1), une grande protéine extracellulaire connue pour façonner l’architecture tissulaire et les microenvironnements tumoraux. Des travaux antérieurs suggéraient que la TSP‑1 en pleine longueur peut, dans certaines conditions, favoriser la dégradation osseuse. Ici, l’équipe a examiné une portion C‑terminale spécifique de la TSP‑1, appelée E123CaG, qui est dépourvue de certains domaines stimulant les ostéoclastes. En cultures cellulaires, ils ont trouvé que si la TSP‑1 intacte ne modifiait pas la formation d’ostéoclastes induite par RANKL, le fragment E123CaG réduisait fortement le nombre et la taille des ostéoclastes matures et perturbait l’anneau d’actine dont ces cellules ont besoin pour résorber l’os. Fait important, les ostéoclastes matures libèrent eux‑mêmes des protéases, en particulier une enzyme nommée HTRA1, qui clivent la TSP‑1 et génèrent un fragment similaire à E123CaG — suggérant que cet inhibiteur peut être produit comme un contrôle de rétroaction intégré.
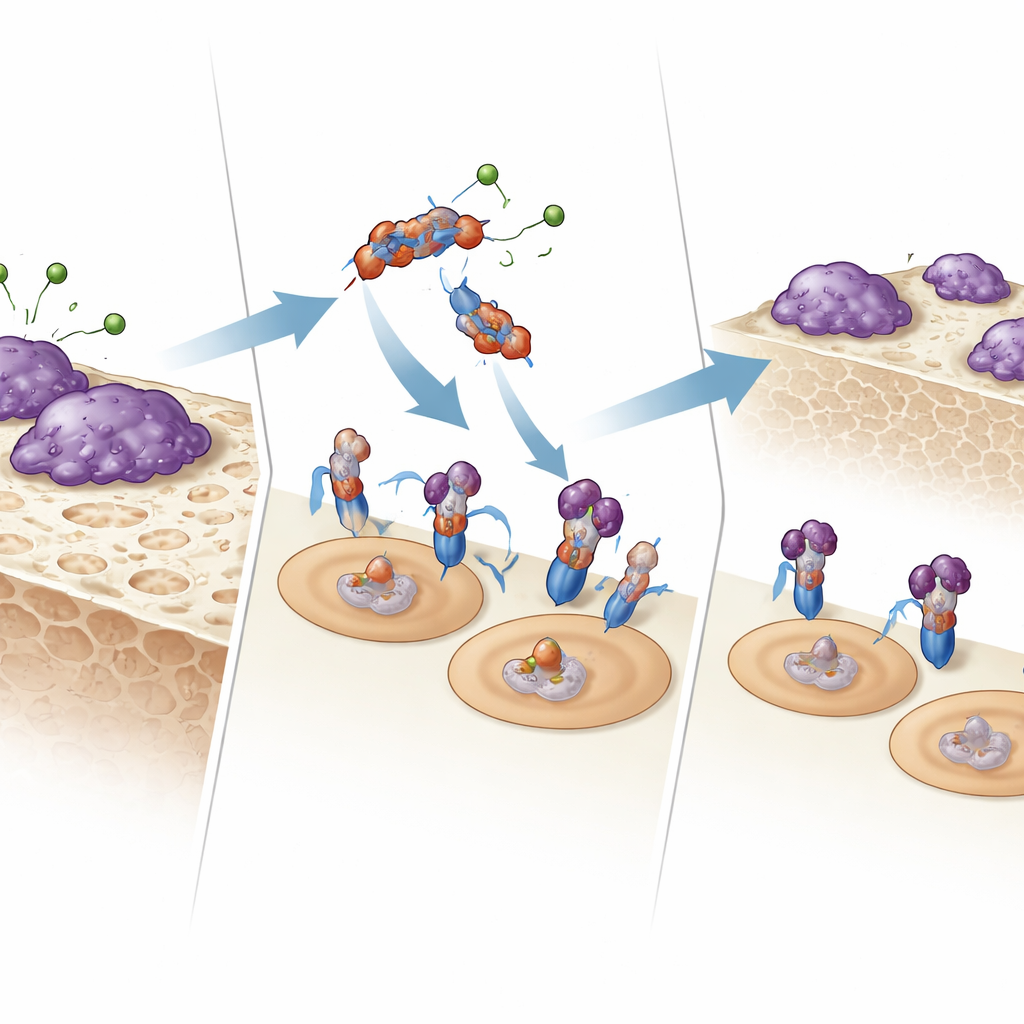
Comment le fragment s’adresse aux cellules qui rongent l’os
Pour comprendre comment E123CaG agit, l’équipe a testé s’il se lie directement aux récepteurs qui contrôlent les ostéoclastes. À l’aide de la résonance plasmonique de surface et d’essais de liaison en phase solide, ils ont montré que E123CaG s’attache à RANK, le récepteur présent sur les précurseurs d’ostéoclastes qui détecte RANKL. Cette liaison n’empêche pas RANKL de se fixer, mais elle affaiblit le signal en aval : les premières protéines de signalisation (les MAPK p38 et JNK) s’activent moins fortement, et le facteur de transcription clé NFATc1 pénètre moins efficacement dans le noyau. Ensemble, ces changements atténuent le programme de maturation qui convertit normalement les précurseurs en cellules pleinement actives et résorbantes.
Protéger le frein naturel contre la perte osseuse
Le fragment fait plus que perturber la signalisation via RANK. Il se lie aussi à l’OPG, le récepteur leurre naturel qui neutralise RANKL. En culture, E123CaG n’empêchait pas l’OPG d’attraper RANKL ; au contraire, il renforçait la capacité de l’OPG à inhiber la formation d’ostéoclastes. Les chercheurs ont découvert pourquoi : pendant le développement des ostéoclastes, des protéases issues des ostéoclastes matures, dont HTRA1, fragmentent et inactivent l’OPG. En présence d’E123CaG, l’OPG était protégée de cette dégradation et demeurait intacte plus longtemps. Ainsi, le même fragment généré par la protéolyse de la TSP‑1 atténue à la fois le signal interne de RANK et préserve l’OPG, renforçant deux niveaux de contrôle de la destruction osseuse.
Tester le fragment dans un système vivant
Pour vérifier si ces effets sont pertinents au niveau d’un organisme entier, l’équipe a modifié une lignée de cellules de cancer du sein murin qui migre préférentiellement vers l’os pour sécréter le fragment E123CaG. Lorsqu’elles ont injecté ces cellules dans la circulation de souris pour coloniser les os, les animaux porteurs de tumeurs produisant E123CaG ont survécu plus longtemps et présenté moins de dommages osseux sévères que les témoins. Des scans micro‑CT à haute résolution montraient une meilleure préservation de l’os trabéculaire (spongieux), des travées plus épaisses et des espaces inter‑trabéculaires plus petits. Ces bénéfices sont apparus sans changement du taux de croissance de la tumeur primaire, ce qui suggère que le fragment agit principalement en modifiant le microenvironnement osseux plutôt qu’en attaquant directement les cellules cancéreuses.
Ce que cela signifie pour les patients
Pris ensemble, les résultats révèlent un circuit protecteur jusqu’ici méconnu dans l’os : les ostéoclastes libèrent des protéases qui clivent la TSP‑1 en un fragment qui, à son tour, freine l’activation supplémentaire des ostéoclastes et protège l’inhibiteur naturel OPG de la destruction. Dans le contexte des métastases osseuses du cancer du sein, ce fragment peut ralentir la formation des cellules qui rongent l’os et limiter la progression des lésions destructrices chez la souris. Bien que des travaux supplémentaires soient nécessaires avant de développer un traitement, l’étude met en évidence E123CaG et ses interactions avec RANK et OPG comme des pistes prometteuses pour des médicaments susceptibles de mieux protéger les os dans le cancer et d’autres maladies marquées par une perte osseuse excessive.
Citation: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Mots-clés: métastase osseuse, ostéoclastes, thrombospondine-1, RANKL RANK OPG, remodelage osseux