Clear Sky Science · ru
Взаимодействие TSP‑1 с RANK и OPG: значение для ремоделирования кости и остеолитических костных метастазов
Почему важны раки, разрушающие кость
Когда такие опухоли, как рак молочной железы, распространяются в скелет, они могут вызывать болезненные «дыры» в кости, приводящие к переломам, слабости и ухудшению качества жизни. Эти поражения возникают потому, что клетки, которые обычно перестраивают кость, становятся чрезмерно активными и разъедают слишком много ткани. В приведённом здесь исследовании выявлен природный «тормоз» в этой системе: фрагмент распространённого внеклеточного белка, который способен ослаблять разрушение кости и замедлять вызываемое раком повреждение кости у мышей.
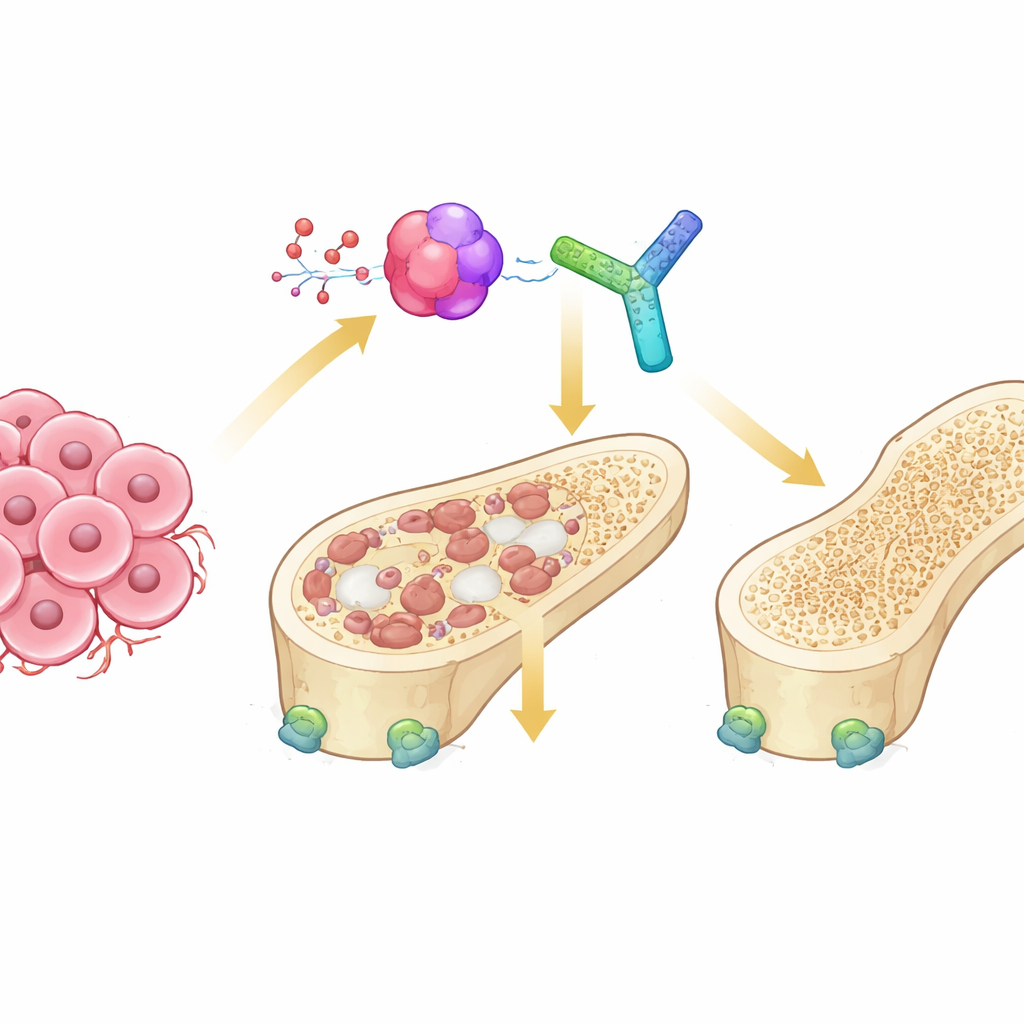
Вытягивание каната внутри нашей кости
Здоровые кости постоянно обновляются двумя противоположными типами клеток. Остеокласты разрушают старую кость, тогда как остеобласты строят новую. При опухолях, распространяющихся в кость, этот баланс нарушается: опухолевые клетки посылают сигналы, которые чрезмерно стимулируют остеокласты, что приводит к остеолитическим поражениям, где кость полая. Ключевой линией связи в этом процессе является система RANK–RANKL, которая запускает созревание остеокластов. Третья участница, остеопротегерин (OPG), обычно действует как предохранитель, связывая RANKL и препятствуя его чрезмерной активации клеток, поедающих кость. То, как этот триумвират точно регулируется в суровой микросреде костных метастазов, оставалось неясным.
Неожиданный помощник, скрытый в большом белке
Авторы сосредоточили внимание на тромбоспондине‑1 (TSP‑1), крупном внеклеточном белке, известном тем, что формирует архитектуру тканей и микроокружение опухолей. Предыдущие работы указывали, что полноразмерный TSP‑1 в некоторых условиях может способствовать разрушению кости. В этой работе команда изучала конкретную С‑концевую часть TSP‑1, названную E123CaG, которой не хватает некоторых доменов, стимулирующих остеокласты. В культурах клеток они обнаружили, что в то время как целый TSP‑1 не менял образование остеокластов, вызванное RANKL, фрагмент E123CaG значительно уменьшал число и размер зрелых остеокластов и нарушал структуру актинового кольца, необходимого этим клеткам для резорбции кости. Важно, что сами зрелые остеокласты выделяют протеазы, особенно фермент HTRA1, который разрезает TSP‑1 и генерирует фрагмент, похожий на E123CaG — это наводит на мысль, что этот ингибитор может образовываться как встроенный механизм обратной связи.
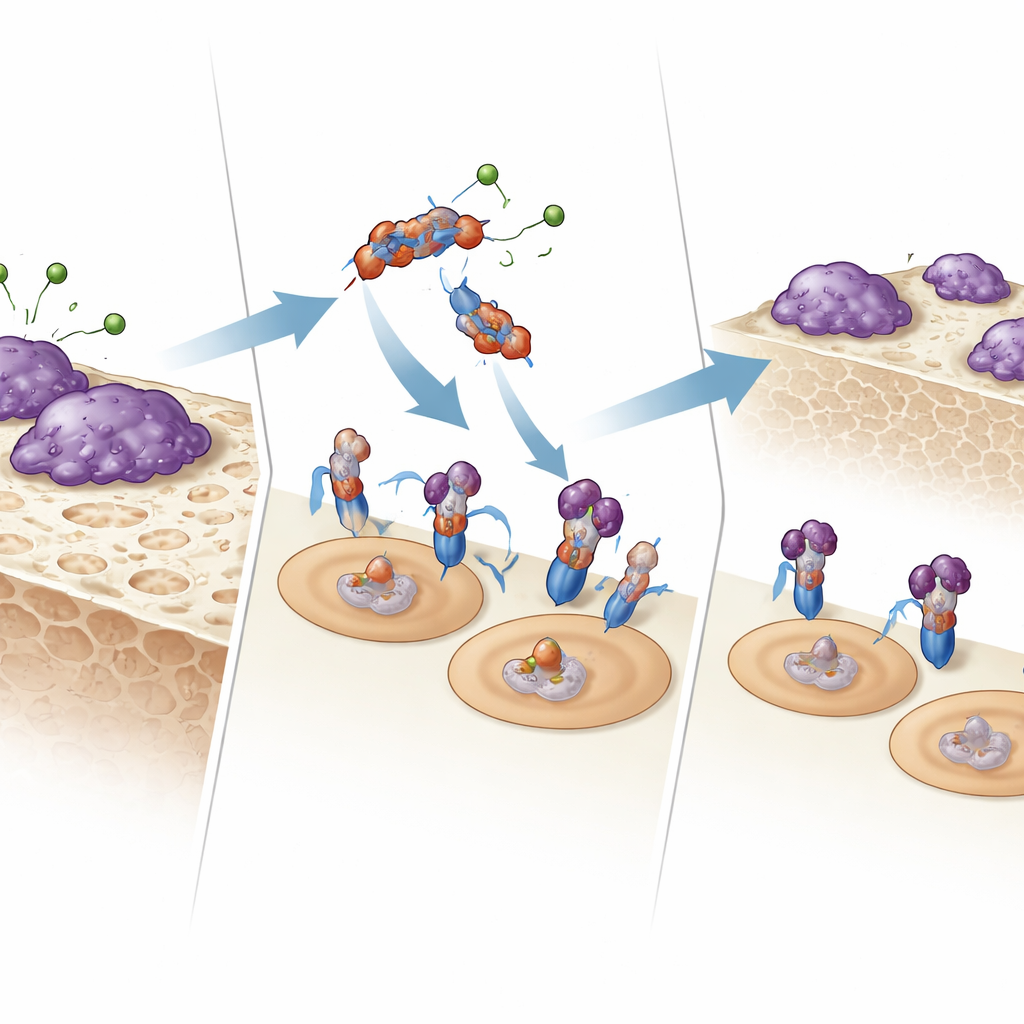
Как фрагмент «разговаривает» с клетками, поедающими кость
Чтобы понять механизм действия E123CaG, исследователи проверили, связывается ли он напрямую с рецепторами, управляющими остеокластами. С помощью поверхностного плазмонного резонанса и твердофазных связывающих тестов они показали, что E123CaG прикрепляется к RANK — рецептору на предшественниках остеокластов, воспринимающему RANKL. Это связывание не препятствует посадке RANKL, но ослабляет последующий сигнал: ранние сигнальные белки (MAPK p38 и JNK) активируются слабее, а ключевой транскрипционный фактор NFATc1 менее эффективно перемещается в ядро. В совокупности эти изменения притупляют программу созревания, которая обычно превращает предшественники в полнофункциональные клетки, разрушающие кость.
Защита природного предохранителя от потери функции
Фрагмент действует не только через вмешательство в сигналы RANK. Он также связывается с OPG — собственным «ловчих» рецептором организма, нейтрализующим RANKL. В культуре E123CaG не мешал OPG захватывать RANKL; напротив, он усиливал способность OPG подавлять образование остеокластов. Исследователи выяснили причину: в процессе развития остеокластов протеазы зрелых остеокластов, включая HTRA1, разрезают и инактивируют OPG. При наличии E123CaG OPG защищён от этого разрушения и остаётся целым дольше. Таким образом, один и тот же фрагмент, образующийся при протеолизе TSP‑1, одновременно ослабляет внутренний сигнал RANK и сохраняет OPG, усиливая две ступени контроля над разрушением кости.
Проверка фрагмента в живой системе
Чтобы выяснить, имеют ли эти эффекты значение для организма в целом, команда модифицировала линию клеток рака молочной железы мышей, предпочитающую метастазировать в кость, чтобы она секретировала фрагмент E123CaG. Когда эти клетки вводили в кровоток мышам для образования костных метастазов, животные с опухолями, продуцирующими E123CaG, жили дольше и имели менее выраженные повреждения кости по сравнению с контрольной группой. Снимки микротомографии высокой чёткости показали лучшее сохранение трабекулярной (губчатой) кости, утолщённые балочки и меньшие промежутки между ними. Эти преимущества проявлялись без изменений скорости роста первичной опухоли, что предполагает, что фрагмент преимущественно действует, изменяя микроокружение кости, а не напрямую атакует раковые клетки.
Что это значит для пациентов
В совокупности результаты раскрывают ранее не распознанную защитную схему в кости: остеокласты выделяют протеазы, которые отрезают TSP‑1, образуя фрагмент, который, в свою очередь, сдерживает дальнейшую активацию остеокластов и защищает природный ингибитор OPG от разрушения. В контексте костных метастазов при раке молочной железы этот фрагмент может замедлять образование клеток, поедающих кость, и ограничивать появление разрушающих поражений у мышей. Хотя до разработки терапии ещё далеко, исследование выделяет E123CaG и его взаимодействия с RANK и OPG как перспективные мишени для препаратов, которые могли бы лучше защищать кости при раке и других заболеваниях, сопровождающихся избыточной потерей костной ткани.
Цитирование: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Ключевые слова: метастазы в кости, остеокласты, тромбоспондин‑1, RANKL RANK OPG, ремоделирование кости