Clear Sky Science · de
TSP-1-Interaktion mit RANK und OPG: Auswirkungen auf Knochenumbau und osteolytische Knochenmetastasen
Warum knochenzerstörende Krebsarten wichtig sind
Wenn Krebsarten wie Brustkrebs in das Skelett streuen, können sie schmerzhafte „Löcher“ im Knochen auslösen, die zu Frakturen, Schwäche und einer geringeren Lebensqualität führen. Diese Läsionen entstehen, weil Zellen, die normalerweise den Knochen umgestalten, überaktiv werden und zu viel Gewebe abbauen. Die hier zusammengefasste Studie beschreibt eine natürliche Bremse in diesem System: ein Fragment eines weit verbreiteten Bindegewebsproteins, das den Knochenabbau drosseln und krebsbedingte Knochenschädigung bei Mäusen verlangsamen kann.
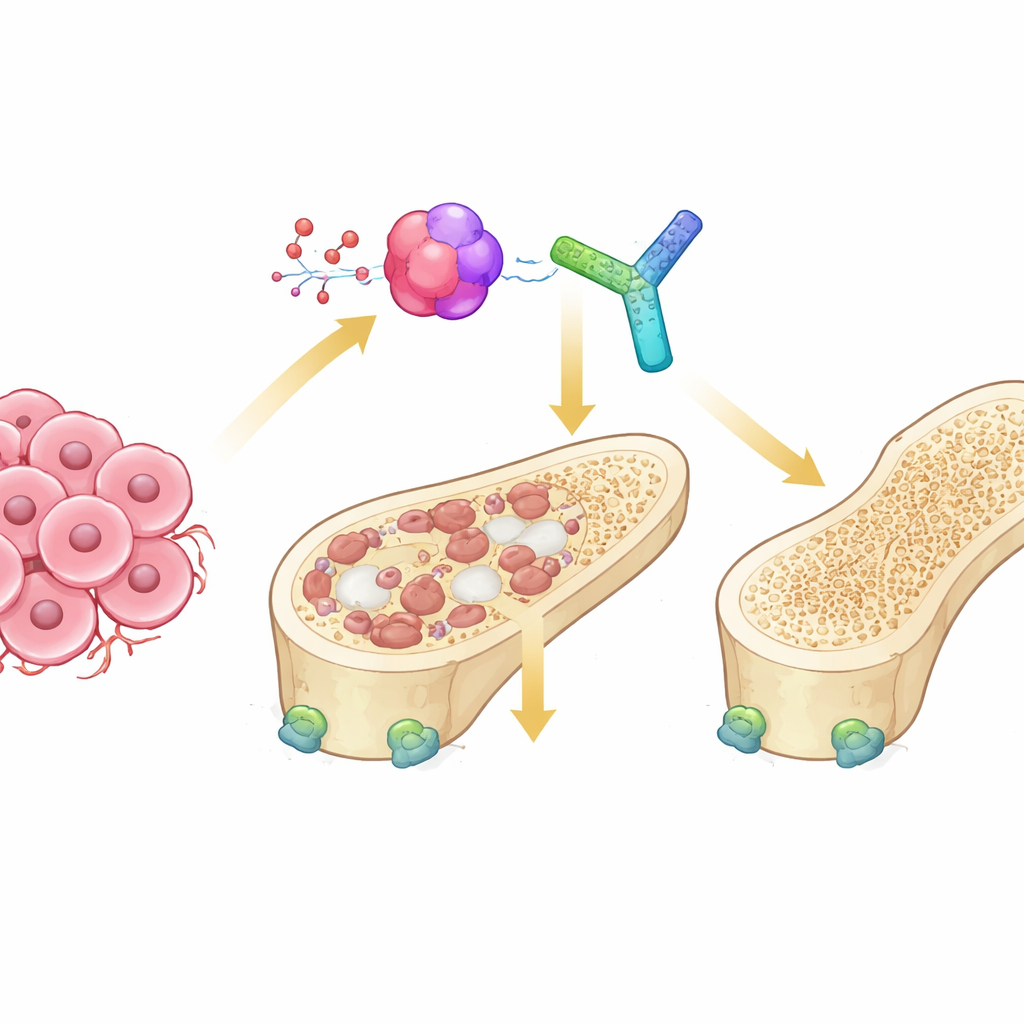
Das Tauziehen in unseren Knochen
Gesunde Knochen werden ständig durch zwei entgegengesetzte Zelltypen erneuert. Osteoklasten bauen alten Knochen ab, während Osteoblasten neuen Knochen aufbauen. Bei Krebs, der in den Knochen metastasiert, geht dieses Gleichgewicht verloren: Tumorzellen senden Signale, die Osteoklasten überstimulieren und zu „osteolytischen“ Läsionen führen, in denen Knochen ausgehöhlt wird. Eine entscheidende Kommunikationsachse in diesem Prozess ist das RANK–RANKL-System, das die Reifung der Osteoklasten einschaltet. Ein dritter Partner, Osteoprotegerin (OPG), wirkt normalerweise als Sicherheitsbremse, indem es RANKL bindet und verhindert, dass es knochenfressende Zellen überaktiviert. Wie dieses Trio im harschen Milieu von Knochenmetastasen feinabgestimmt wird, war bislang unklar.
Ein überraschender Helfer, versteckt in einem größeren Protein
Die Forscher konzentrierten sich auf Thrombospondin‑1 (TSP‑1), ein großes extrazelluläres Protein, das die Gewebearchitektur und das Tumormikromilieu prägt. Frühere Arbeiten legten nahe, dass das vollständige TSP‑1 unter bestimmten Bedingungen tatsächlich den Knochenabbau fördern kann. Hier untersuchte das Team einen spezifischen C-terminalen Teil von TSP‑1, genannt E123CaG, der einige der Domänen vermisst, die Osteoklasten stimulieren. In Zellkulturen fanden sie, dass während intaktes TSP‑1 die durch RANKL induzierte Osteoklastenbildung nicht veränderte, das E123CaG‑Fragment stark die Anzahl und Größe reifer Osteoklasten reduzierte und die Aktinringstruktur störte, die diese Zellen zum Knochenresorbieren benötigen. Wichtig ist, dass reife Osteoklasten selbst Proteasen freisetzen, insbesondere ein Enzym namens HTRA1, das TSP‑1 zerschneidet und ein Fragment ähnlich E123CaG erzeugt — ein Hinweis darauf, dass dieser Inhibitor als eingebauter Rückkopplungsmechanismus entstehen könnte.
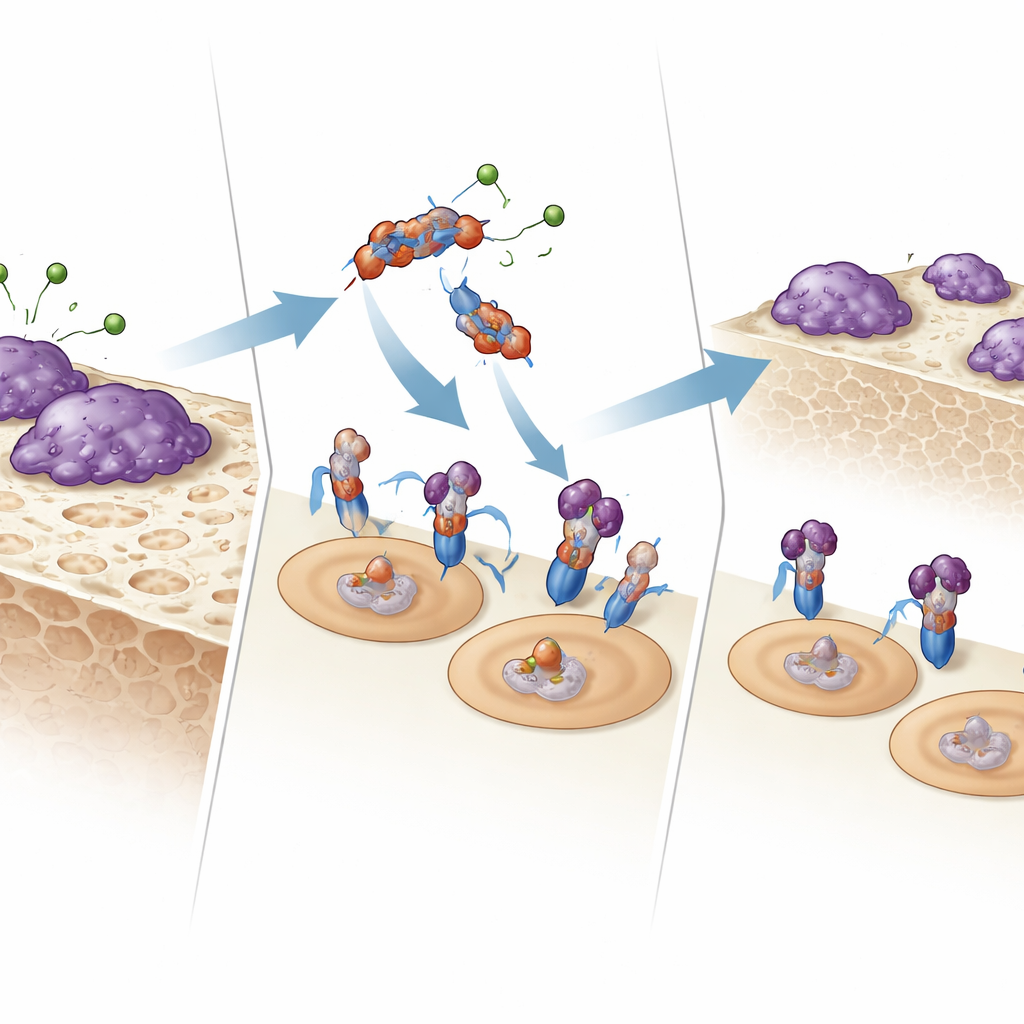
Wie das Fragment mit knochenfressenden Zellen kommuniziert
Um zu verstehen, wie E123CaG wirkt, prüfte das Team, ob es direkt an die Rezeptoren bindet, die Osteoklasten steuern. Mittels Oberflächenplasmonresonanz und Festphasen-Bindungsassays zeigten sie, dass E123CaG an RANK bindet, den Rezeptor auf Osteoklasten‑Vorläufern, der RANKL erkennt. Diese Bindung verhindert nicht, dass RANKL andockt, schwächt aber das nachgeschaltete Signal ab: frühe Signalmoleküle (MAPKs p38 und JNK) werden weniger stark aktiviert und der wichtige Transkriptionsfaktor NFATc1 gelangt weniger effizient in den Zellkern. Zusammen dämpfen diese Veränderungen das Reifungsprogramm, das Vorläufer in voll aktive, knochenresorbierende Zellen umwandelt.
Die natürliche Bremse vor Knochenverlust schützen
Das Fragment tut mehr, als nur die RANK-Signalweiterleitung zu stören. Es bindet auch OPG, den körpereigenen Lockvogelrezeptor, der RANKL abfängt. In Kultur verhinderte E123CaG nicht, dass OPG RANKL auffängt; stattdessen verstärkte es OPGs Fähigkeit, die Osteoklastenbildung zu hemmen. Die Forscher fanden den Grund: Während der Osteoklastenentwicklung zerschneiden Proteasen reifer Osteoklasten, darunter HTRA1, OPG und inaktivieren es. In Gegenwart von E123CaG wurde OPG vor diesem Abbau geschützt und blieb länger intakt. Somit dämpft dasselbe Fragment, das durch Proteolyse von TSP‑1 entsteht, sowohl RANK‑interne Signale als auch erhält OPG — und verstärkt damit zwei Kontrollschichten gegen Knochenzerstörung.
Test des Fragments in einem lebenden System
Um zu prüfen, ob diese Effekte in einem ganzen Organismus von Bedeutung sind, erzeugte das Team eine Maus‑Brustkrebszelllinie, die bevorzugt in Knochen metastasiert und das E123CaG‑Fragment sezerniert. Als diese Zellen in die Blutbahn von Mäusen injiziert wurden, um Knochenmetastasen zu etablieren, überlebten Tiere mit E123CaG‑produzierenden Tumoren länger und wiesen weniger schwere Knochenschäden auf als Kontrollen. Hochauflösende Mikro‑CT‑Scans zeigten eine bessere Erhaltung des trabekulären (schwammigen) Knochens, dickere Strukturen und kleinere Abstände zwischen ihnen. Diese Vorteile traten ohne Veränderungen der Wachstumsrate des Primärtumors auf, was darauf hindeutet, dass das Fragment hauptsächlich durch Modifikation des Knochenmikromilieus wirkt und die Tumorzellen nicht direkt angreift.
Was das für Patientinnen und Patienten bedeutet
Insgesamt enthüllen die Befunde einen bisher wenig beachteten Schutzkreis im Knochen: Osteoklasten setzen Proteasen frei, die TSP‑1 in ein Fragment schneiden, das wiederum weitere Osteoklasten‑Aktivierung bremst und den körpereigenen Inhibitor OPG vor Zerstörung bewahrt. Im Kontext von Brustkrebs‑Knochenmetastasen kann dieses Fragment die Bildung knochenfressender Zellen verlangsamen und die Ausbreitung zerstörerischer Läsionen bei Mäusen begrenzen. Zwar sind weitere Arbeiten nötig, bevor sich daraus eine Therapie entwickeln lässt, doch hebt die Studie E123CaG und seine Wechselwirkungen mit RANK und OPG als vielversprechende Ansatzpunkte für Medikamente hervor, die Knochen bei Krebs und anderen Erkrankungen mit übermäßigem Knochenverlust besser schützen könnten.
Zitation: Carminati, L., Sangalli, F., Urbinati, C. et al. TSP-1 interaction with RANK and OPG: implications for bone remodeling and osteolytic bone metastasis. Cell Death Dis 17, 332 (2026). https://doi.org/10.1038/s41419-026-08600-9
Schlüsselwörter: Knochenmetastase, Osteoklasten, Thrombospondin-1, RANKL RANK OPG, Knochenumbau