Clear Sky Science · tr
ZNRF1 eksikliği Fas ligand trafğini ve bağışıklık dengesini bozuyor
Bu, bağışıklık sağlığımız için neden önemli
Bağışıklık sistemimiz ince bir çizgide yürümek zorunda: mikroplar ve yabancı kan hücreleri gibi tehditlere saldırırken, yanıt kontrolden çıkmadan önce kendini kapatmalı. Bu çalışma, aktifleşmiş bağışıklık hücrelerinin sessizce uzaklaştırılıp uzaklaştırılmayacağına karar vermeye yardımcı olan makrofaj adlı yaygın bir bağışıklık hücresi içinde gizli bir kontrol anahtarını ortaya koyuyor. Bu anahtarın anlaşılması, kronik iltihap, otoimmünite veya transfüzyon komplikasyonlarıyla ilişkili durumların daha iyi yönetilmesine nihayetinde yardımcı olabilir.
Bağışıklık kendini yok etmesi için bir trafik ışığı
Bağışıklık hücreleri işlerini bitirdiğinde, birçokları yüzeyde bulunan Fas ligand adlı bir molekülü içeren yerleşik bir intihar sinyaliyle ortadan kaldırılır. Bir hücredeki Fas ligand, eşleşen reseptörü taşıyan diğer hücrede ölümü tetikleyerek aşırı aktif yanıtları budamaya yardımcı olur. Çoğu araştırma bir hücrenin ne kadar Fas ligand ürettiğine odaklandı. Bu çalışmada yazarlar farklı bir soruyu sordular: Fas ligand dahili depolama bölmelerinden makrofajların dış yüzeyine tam zamanında nasıl taşınıyor ve bu taşıma adımı yanlış giderse ne oluyor?
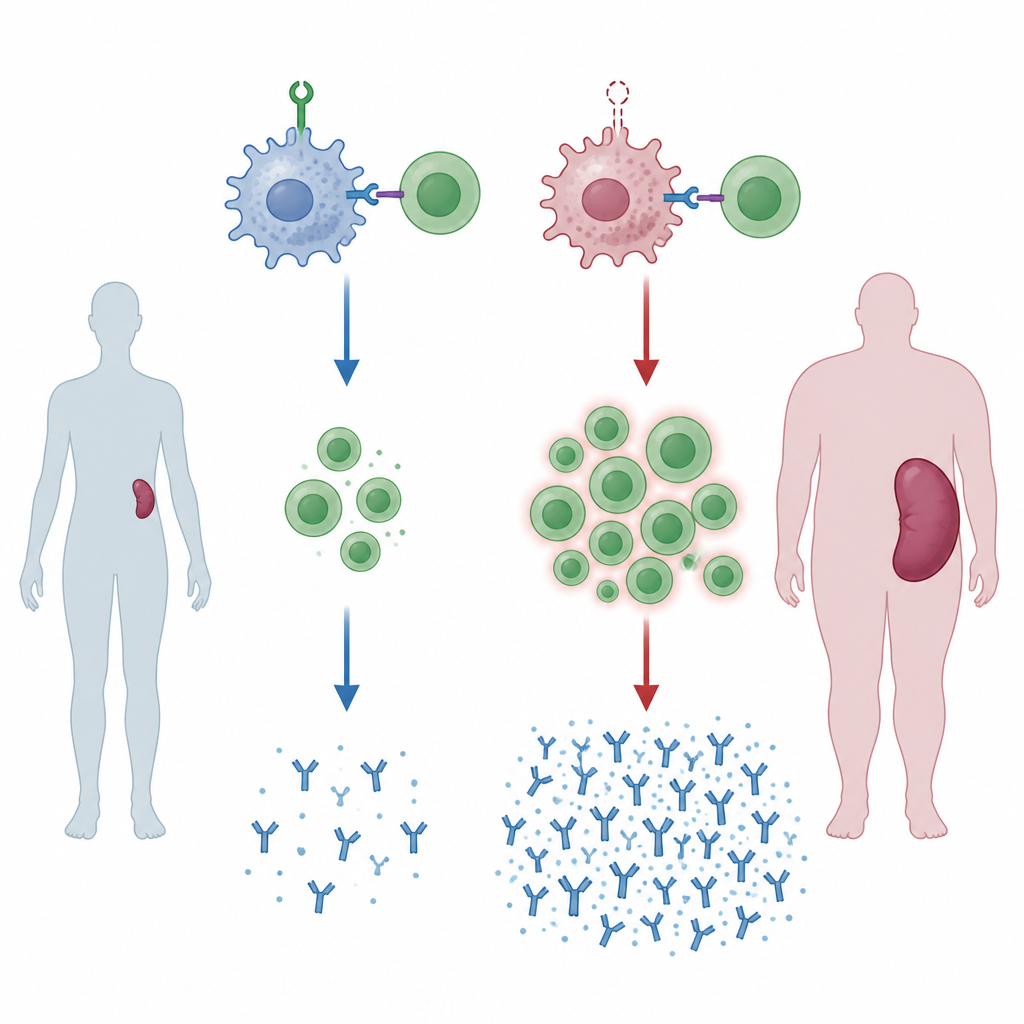
Eksik bir bekçi, şişkin dalaklara yol açıyor
Takım, makrofajlar da dahil olmak üzere miyeloid hücreleri ZNRF1 adlı bir proteinden yoksun olan fareler oluşturdu. Bu fareler yaşlandıkça dalakları büyüdü; bu kronik bağışıklık aktivasyonunun bir işareti. Hayvanlar genetik olarak farklı bir donörden gelen bir transfüzyonu taklit eden yabancı kana maruz bırakıldığında değişiklikler daha belirgin hale geldi. Dalağın B hücreleri ile T hücrelerinin etkileşip çoğaldığı bölgeleri genişledi ve yardımcı T hücrelerine kıyasla öldürücü T hücrelerin dengesi yukarı kaydı. Bu fareler ayrıca verici kana karşı belirli antikor sınıflarını daha yüksek miktarda üretti; bu da miyeloid hücrelerde ZNRF1 olmadığında bağışıklık sisteminin aşırı yanıt vermeye eğilimli olduğunu gösteriyor.
Yüzey sinyali engellenmiş, yük içerde birikmiş
ZNRF1’in makrofajlar içinde ne yaptığını anlamak için araştırmacılar hücre kültürüne yöneldi. Normal ve ZNRF1‑yetersiz makrofajları bakteriyel bileşenlerle veya canlı bakterilerle uyarıp Fas ligandı ölçtüler. Şaşırtıcı bir şekilde ZNRF1 eksik hücreler genel olarak bol miktarda Fas ligand üretiyordu; çoğu zaman normal hücrelerden daha bile fazla, ancak bunları yüzeylerinde gösteremiyorlardı. Mikroskop altında LAMP1 proteini ile işaretlenen iç depolama kompartmanları her iki hücre tipinde de hücre kenarına doğru hareket etti, ancak ZNRF1‑yetersiz hücrelerde Fas ligand yükü kortekse birlikte gitmedi ve merkez yakınlarında takılı kaldı. Bu, Fas ligand üretiminde veya ilk depolanmasında bir sorundan ziyade yuvalama veya füzyon adımında geç bir bozulmaya işaret ediyordu.
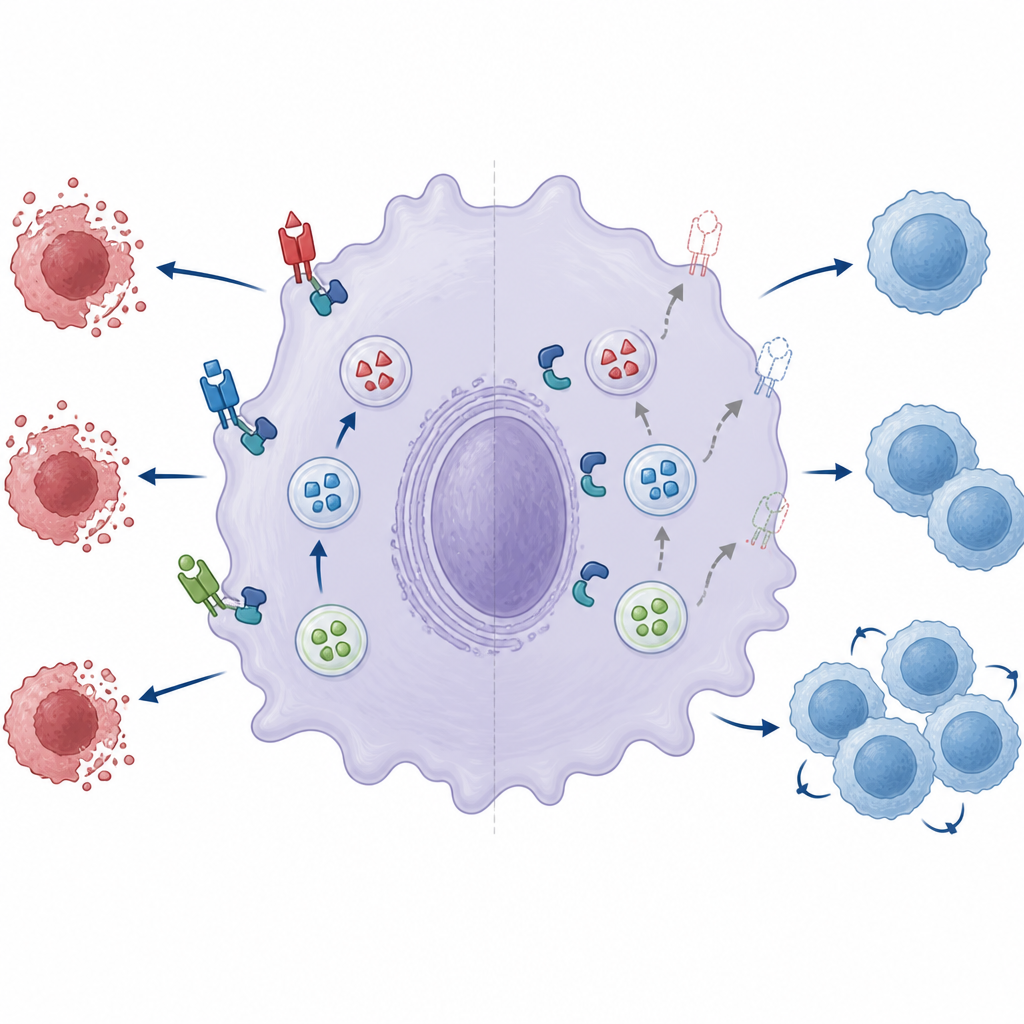
Kırık bir füzyon makinesi bağışıklık frenini zayıflatıyor
Yazarlar daha sonra depolama veziküllerinin hücre yüzeyiyle birleşmesine izin veren küçük füzyon makinesinin iki önemli bileşenini incelediler: Munc18‑2 ve Syntaxin‑3 adlı protein çifti. Normal makrofajlarda bu iki ortak, veziküllerin açılmasına ve yüklerini salmasına yardımcı olan bir kompleks oluşturur. ZNRF1 eksik olduğunda Munc18‑2 ile Syntaxin‑3 arasındaki ortaklık belirgin şekilde zayıftı. Munc18‑2 seviyelerinin daha da azaltılması yüzey Fas ligandını daha da düşürdü ve önemini vurguladı. Eksik hücrelere normal ZNRF1’i yeniden sokmak Fas ligand gösterimini iyileştirdi, ancak katalitik olarak inaktif bir ZNRF1 versiyonu bunu yapmadı; bu da, ZNRF1’in enzimatik aktivitesinin, kompleks yine de bir araya gelse bile füzyon makinesini tam olarak yetkin hale getirmek için gerekli olduğunu düşündürüyor.
Tükenmiş bağışıklık hücrelerini öldürmenin sonuçları
Fas ligandının görevi aktifleşmiş hücrelerde ölümü tetiklemek olduğundan, ekip makrofajların hedef hücreleri ne kadar iyi öldürebildiğini test etti. Normal makrofajlar aktifleşmiş yardımcı T hücreleri veya Fas sinyallerine çok duyarlı bir hücre hattıyla karıştırıldığında zamanla birçok hedef öldü. Buna karşılık, ZNRF1‑yetersiz makrofajlar bu hücrelerin çok daha fazlasını sağ bıraktı, hatta güçlü uyarılsa bile. Bu azalmış öldürme yeteneği fare verileriyle uyumlu: makrofajlar yüzeylerinde Fas ligandını verimli şekilde ortaya koyamazsa, aktifleşmiş T hücreleri daha uzun süre hayatta kalır, B hücrelerine daha fazla yardım sağlar ve bu da genişlemiş dalaklar ile artmış antikor üretimini besler.
Kontrolden çıkan bağışıklığı kontrol etmek için ne anlama geliyor
Birlikte, bulgular ZNRF1’i Fas ligand dolu paketlerin iç hareketini makrofaj yüzeyiyle son füzyonlarına bağlayan yerleşik bir emniyet cihazı olarak ortaya koyuyor. ZNRF1 normal şekilde işlediğinde Fas ligand hücrenin dışına ulaşır, makrofajların aktif T hücrelerini budamasına ve bağışıklık reaksiyonlarını kontrol altında tutmasına izin verir. ZNRF1 yok olduğunda bu taşıma adımı başarısız olur, yüzey Fas ligandı düşük kalır ve bağışıklık hücreleri daha serbestçe proliferasyona devam eder. Bu içgörülerin tedavilere dönüştürülmesinden önce yapılması gereken çok çalışma olsa da çalışma, vücudun bağışıklık yanıtlarının kapatma aşamasını ince ayarlayan spesifik bir moleküler tutamaç olduğunu vurguluyor.
Atıf: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Anahtar kelimeler: Fas ligand, makrofajlar, bağışıklık homeostazı, ZNRF1, T hücresi apoptozu