Clear Sky Science · pl
Niedobór ZNRF1 zaburza transport liganda Fas i równowagę układu odpornościowego
Dlaczego to ma znaczenie dla zdrowia układu odpornościowego
Nasz układ odpornościowy musi iść po cienkiej linii: musi zwalczać zagrożenia, takie jak drobnoustroje czy obce komórki krwi, a jednocześnie wyłączyć się zanim reakcja wymknie się spod kontroli. W tym badaniu odkryto ukryty przełącznik w obrębie powszechnej komórki odpornościowej — makrofaga — który pomaga decydować, czy aktywowane komórki odpornościowe zostaną dyskretnie usunięte, czy też będą nadal się mnożyć. Zrozumienie tego przełącznika może w przyszłości pomóc lepiej kontrolować schorzenia związane z przewlekłym zapaleniem, autoimmunizacją lub powikłaniami po transfuzji.
Światło sygnalizacyjne dla samodestrukcji układu odpornościowego
Kiedy komórki odpornościowe wypełnią swoje zadanie, wiele z nich jest eliminowanych poprzez wbudowany sygnał samodestrukcji z udziałem cząsteczki powierzchniowej zwanej ligandem Fas. Ligand Fas na jednej komórce wywołuje śmierć w komórce niosącej odpowiadający mu receptor, pomagając ograniczyć nadaktywne reakcje. Większość badań skupiała się na tym, ile liganda Fas wytwarza komórka. Autorzy postawili inne pytanie: jak ligand Fas jest przemieszczany z wewnętrznych magazynów na zewnętrzną powierzchnię makrofagów w odpowiednim momencie i co się dzieje, gdy ten etap dostawy zawodzi?
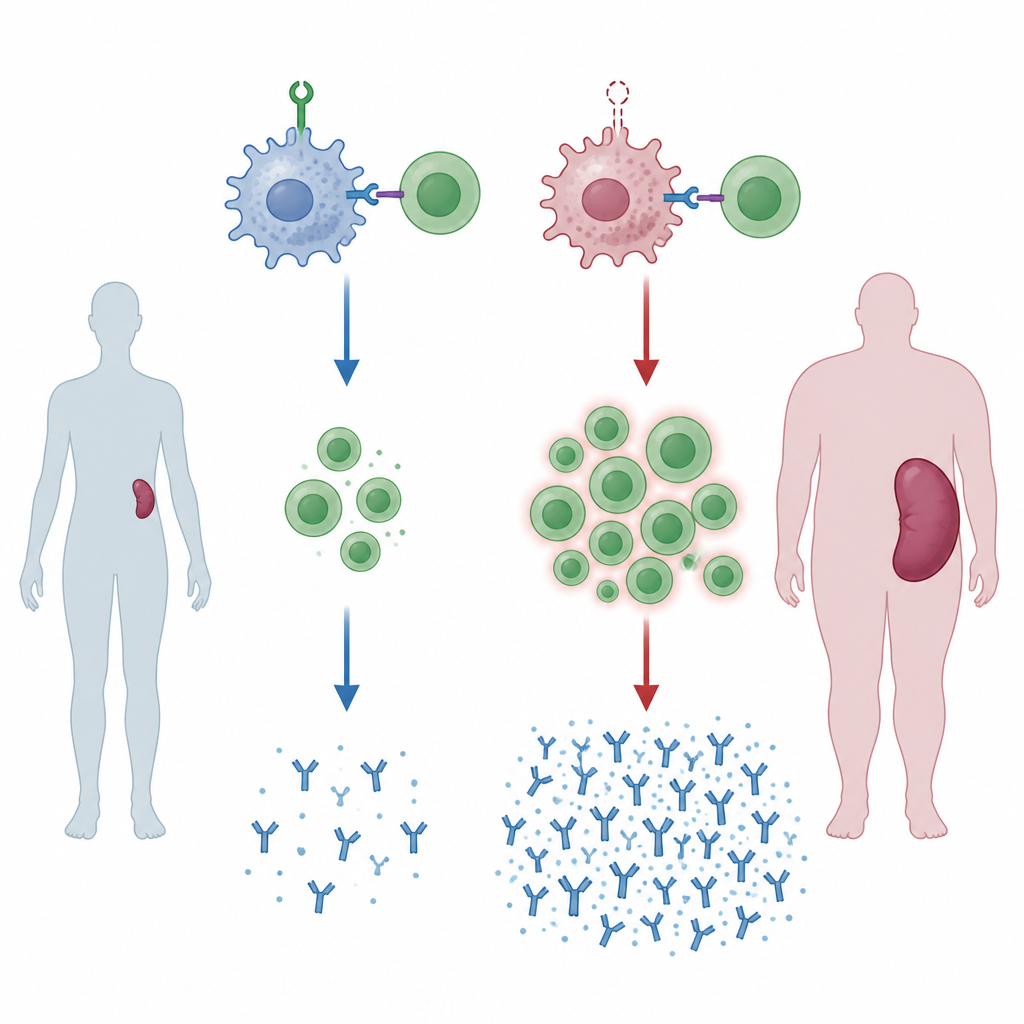
Brak strażnika prowadzi do powiększonych śledzion
Zespół stworzył myszy, których komórki mieloidalne, w tym makrofagi, nie mają białka o nazwie ZNRF1. W miarę starzenia się tych myszy ich śledziony powiększały się, co jest oznaką przewlekłej aktywacji układu odpornościowego. Gdy zwierzęta były eksponowane na obcą krew, naśladując transfuzję od genetycznie innego dawcy, zmiany stawały się bardziej wyraźne. W śledzionach poszerzyły się obszary, gdzie komórki B i T wchodzą w interakcje i mnożą się, a proporcja pomocniczych limfocytów T do cytotoksycznych przesunęła się w górę. Te myszy wytwarzały także większe ilości określonych klas przeciwciał przeciwko krwi dawcy, co wskazuje, że bez ZNRF1 w komórkach mieloidalnych układ odpornościowy jest gotowy do zbyt silnej reakcji.
Sygnał powierzchniowy zablokowany, podczas gdy ładunek gromadzi się w środku
Aby zrozumieć, co robi ZNRF1 w makrofagach, badacze sięgnęli po hodowle komórkowe. Pobudzili makrofagi prawidłowe i pozbawione ZNRF1 składnikami bakteryjnymi lub żywymi bakteriami i zmierzyli ligand Fas. Ku zaskoczeniu, komórki pozbawione ZNRF1 wytwarzały ogólnie dużo liganda Fas, często nawet więcej niż komórki normalne, ale nie potrafiły go eksponować na swojej powierzchni. Pod mikroskopem wewnętrzne magazyny oznaczone białkiem LAMP1 w obu typach komórek przesuwały się w stronę krawędzi komórki, lecz w komórkach pozbawionych ZNRF1 ładunek liganda Fas nie podążał z nimi ku korze i pozostawał utknięty blisko środka. Wskazywało to na późny defekt w etapie dokowania lub fuzji, a nie na problem z produkcją czy początkowym magazynowaniem liganda Fas.
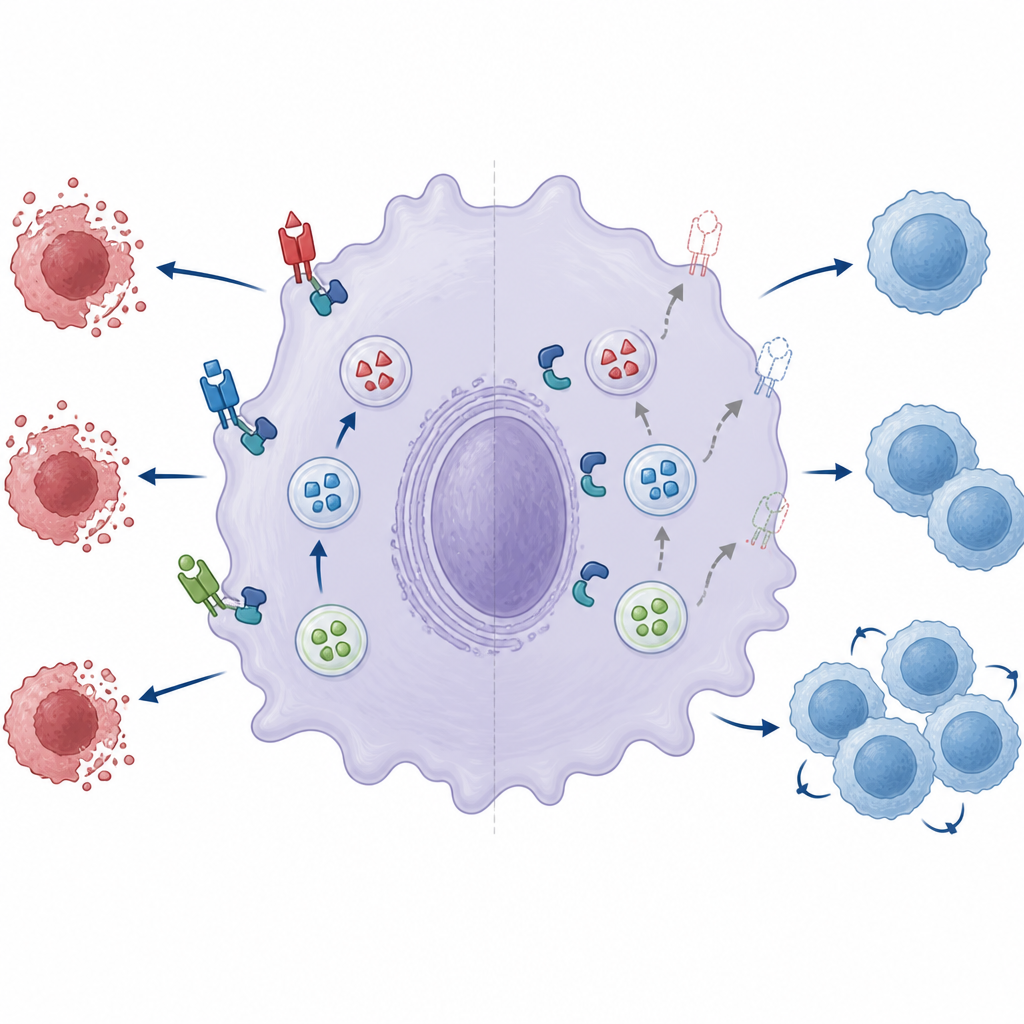
Uszkodzony mechanizm fuzji osłabia hamowanie odpowiedzi
Autorzy zbadali następnie dwa kluczowe składniki maleńkiej maszyny fuzji, która pozwala pęcherzykom magazynowym łączyć się z powierzchnią komórki: parę białek Munc18‑2 i Syntaxin‑3. W normalnych makrofagach te dwie partnerujące cząsteczki tworzą kompleks, który pomaga pęcherzykom otworzyć się i uwolnić ładunek. Gdy ZNRF1 był nieobecny, partnerstwo między Munc18‑2 a Syntaxin‑3 było wyraźnie słabsze. Obniżenie poziomów Munc18‑2 dodatkowo zmniejszało ilość liganda Fas na powierzchni, podkreślając jego znaczenie. Ponowne wprowadzenie prawidłowego ZNRF1 do komórek deficytowych poprawiało ekspozycję liganda Fas, lecz katalitycznie nieaktywna wersja ZNRF1 nie dawała takiego efektu, co sugeruje, że aktywność enzymatyczna ZNRF1 jest potrzebna, by maszyna fuzji działała w pełni sprawnie, nawet jeśli sam kompleks wciąż może się złożyć.
Konsekwencje dla eliminacji zużytych komórek odpornościowych
Ponieważ zadaniem liganda Fas jest wywoływanie śmierci w aktywowanych komórkach, zespół przetestował, jak dobrze makrofagi potrafią zabijać komórki docelowe. Gdy normalne makrofagi były mieszane z aktywowanymi pomocniczymi limfocytami T lub z linią komórkową bardzo wrażliwą na sygnały Fas, wiele komórek docelowych ginęło z czasem. W przeciwieństwie do tego, makrofagi pozbawione ZNRF1 oszczędzały znacznie więcej tych komórek, nawet gdy były silnie pobudzone. Ta zmniejszona zdolność do zabijania odpowiada obserwacjom u myszy: jeśli makrofagi nie potrafią efektywnie eksponować liganda Fas na swojej powierzchni, aktywowane limfocyty T przeżywają dłużej, dostarczając więcej wsparcia komórkom B i napędzając powiększanie śledzion oraz zwiększoną produkcję przeciwciał.
Co to oznacza dla kontroli wymykającej się odporności
W sumie wyniki wskazują, że ZNRF1 działa jako wbudowane urządzenie bezpieczeństwa łączące wewnętrzny transport pęcherzyków wypełnionych ligandem Fas z ich końcową fuzją z powierzchnią makrofaga. Gdy ZNRF1 funkcjonuje prawidłowo, ligand Fas trafia na zewnątrz komórki, umożliwiając makrofagom usuwanie aktywowanych limfocytów T i utrzymanie reakcji immunologicznych w ryzach. Gdy ZNRF1 jest nieobecny, etap dostawy zawodzi, poziom liganda Fas na powierzchni pozostaje niski, a komórki odpornościowe mogą się swobodniej rozmnażać. Choć przed przekształceniem tych obserwacji w terapie pozostaje jeszcze dużo pracy, badanie uwydatnia konkretny molekularny punkt uchwytu, przez który organizm precyzyjnie dostraja fazę wygaszania odpowiedzi immunologicznych.
Cytowanie: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Słowa kluczowe: ligand Fas, makrofagi, homeostaza odpornościowa, ZNRF1, apoptoza limfocytów T