Clear Sky Science · de
ZNRF1‑Mangel stört den Fas‑Ligand‑Transport und das Immungleichgewicht
Warum das für unsere Immun‑Gesundheit wichtig ist
Unser Immunsystem muss eine Gratwanderung meistern: Es muss Bedrohungen wie Mikroben oder fremde Blutzellen bekämpfen, sich aber rechtzeitig abschalten, bevor die Reaktion eskaliert. Diese Studie deckt einen verborgenen Kontrollschalter in einer häufigen Immunzelle, dem Makrophagen, auf, der mitentscheidet, ob aktivierte Immunzellen still entfernt werden oder weiter proliferieren dürfen. Das Verständnis dieses Schalters könnte langfristig helfen, Zustände mit chronischer Entzündung, Autoimmunität oder Transfusionskomplikationen besser zu steuern.
Ein Verkehrslicht für die immunvermittelte Selbstzerstörung
Wenn Immunzellen ihre Aufgabe erfüllt haben, werden viele von ihnen über ein eingebautes Selbstzerstörsignal beseitigt, an dem ein Oberflächenmolekül namens Fas‑Ligand beteiligt ist. Fas‑Ligand auf einer Zelle löst den Tod in einer anderen Zelle aus, die den passenden Rezeptor trägt, und hilft so, überaktive Reaktionen zurückzuschneiden. Die meisten Studien konzentrierten sich darauf, wie viel Fas‑Ligand eine Zelle produziert. Hier stellten die Autoren eine andere Frage: Wie wird Fas‑Ligand von internen Speicherkammern zur Außenfläche von Makrophagen transportiert – und was passiert, wenn dieser Liefer-schritt fehlschlägt?
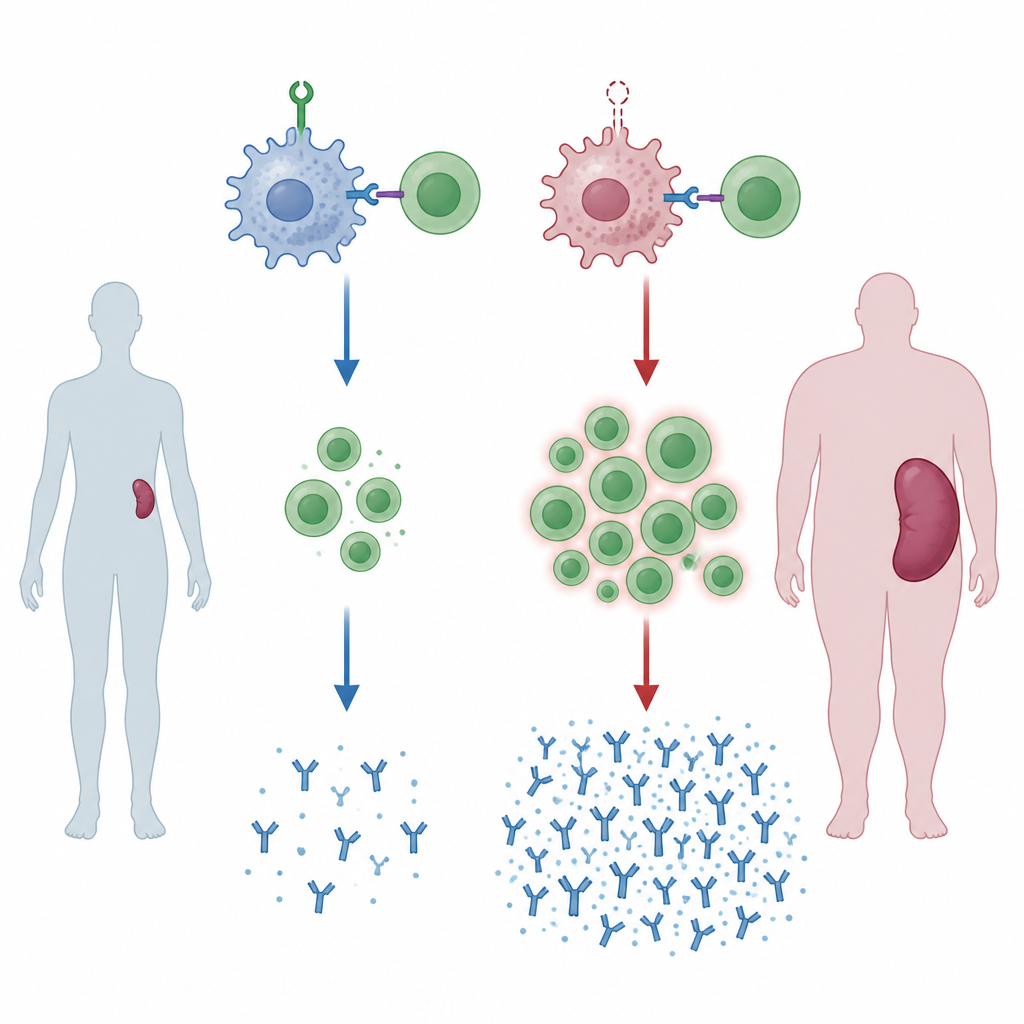
Ein fehlender Wächter führt zu geschwollenen Milzen
Das Team erzeugte Mäuse, deren myeloische Zellen, einschließlich Makrophagen, ein Protein namens ZNRF1 nicht besitzen. Mit zunehmendem Alter dieser Tiere vergrößerte sich die Milz, ein Hinweis auf chronische Immunaktivierung. Beim Kontakt mit fremdem Blut, als Modell für eine Transfusion von genetisch unterschiedlichen Spendern, wurden die Veränderungen noch deutlicher. In ihren Milzen waren Regionen erweitert, in denen B‑ und T‑Zellen interagieren und proliferieren, und das Verhältnis von Helfer‑ zu Killer‑T‑Zellen verschob sich nach oben. Diese Mäuse produzierten außerdem höhere Mengen bestimmter Antikörperklassen gegen das Fremdblut, was darauf hindeutet, dass ohne ZNRF1 in myeloiden Zellen das Immunsystem zu einer überstarken Reaktion neigt.
Oberflächensignal blockiert, während Fracht sich innen staut
Um zu verstehen, was ZNRF1 in Makrophagen bewirkt, untersuchten die Forscher Zellen im Kulturmodell. Sie stimulierten normale und ZNRF1‑defiziente Makrophagen mit bakteriellen Komponenten oder lebenden Bakterien und bestimmten den Fas‑Ligand. Überraschenderweise produzierten ZNRF1‑freie Zellen insgesamt viel Fas‑Ligand, oft sogar mehr als normale Zellen, konnten ihn aber nicht an ihrer Oberfläche präsentieren. Unter dem Mikroskop bewegten sich in beiden Zelltypen interne Speichervesikel, markiert durch das Protein LAMP1, zur Zellperipherie, doch in ZNRF1‑defizienten Zellen reiste die Fas‑Ligand‑Fracht nicht mit und blieb in der Nähe des Zellzentrums stecken. Das deutet auf einen späten Defekt beim Andocken oder der Fusion hin, nicht auf ein Problem bei der Produktion oder initialen Speicherung des Fas‑Ligands.
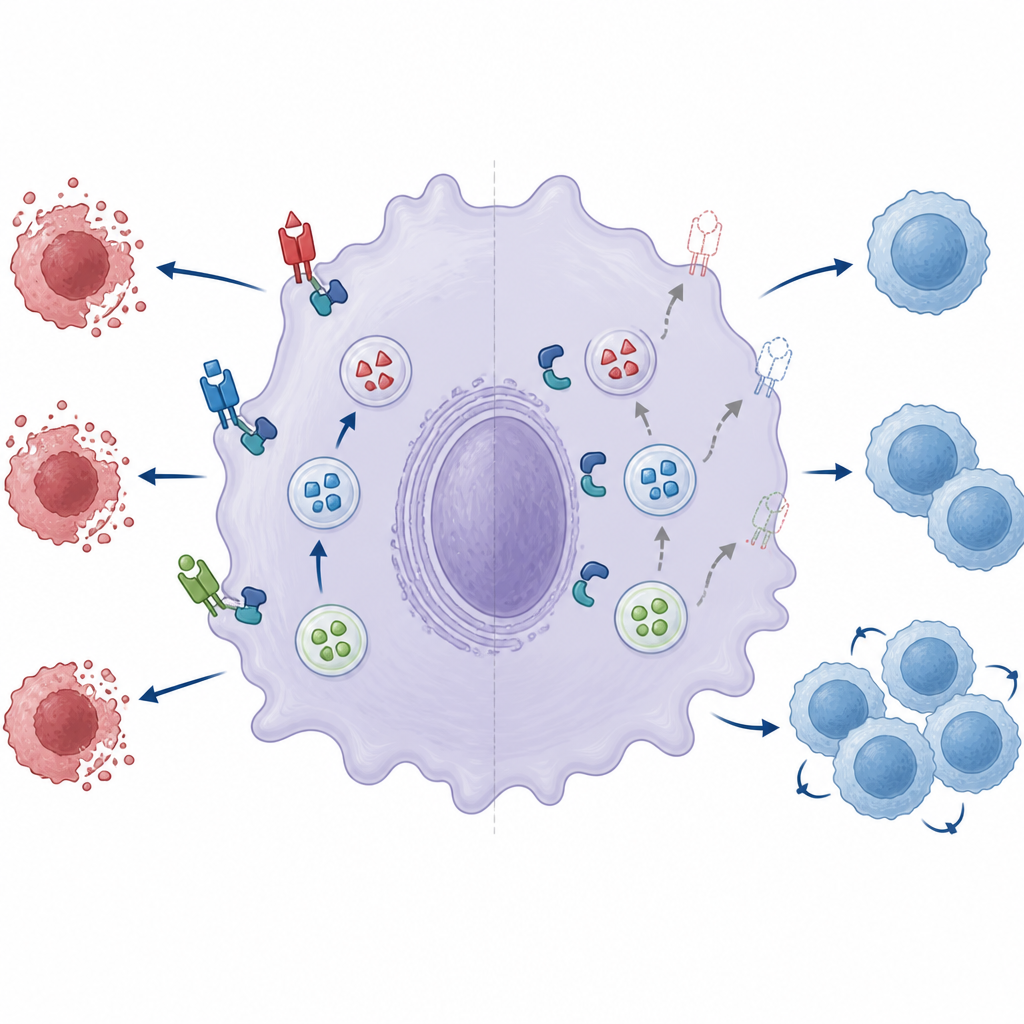
Eine gestörte Fusionsmaschine schwächt die Immun‑Bremsen
Die Autoren untersuchten daraufhin zwei Schlüsselkomponenten der winzigen Fusionsmaschine, die es Speichervesikeln ermöglicht, mit der Zelloberfläche zu verschmelzen: ein Paar Proteine namens Munc18‑2 und Syntaxin‑3. In normalen Makrophagen bilden diese beiden Partner einen Komplex, der Vesikeln beim Öffnen und Freisetzen ihrer Fracht hilft. Fehlt ZNRF1, war die Partnerschaft zwischen Munc18‑2 und Syntaxin‑3 deutlich schwächer. Eine Reduktion von Munc18‑2 verringerte die Oberflächenpräsentation von Fas‑Ligand weiter und unterstrich damit seine Bedeutung. Die Wiedereinführung von normalem ZNRF1 in defiziente Zellen verbesserte die Fas‑Ligand‑Anzeige, eine katalytisch inaktive ZNRF1‑Variante tat dies jedoch nicht, was darauf hindeutet, dass die enzymatische Aktivität von ZNRF1 nötig ist, um die Fusionsmaschine voll funktionsfähig zu machen, selbst wenn sich der Komplex formell noch zusammenbauen kann.
Folgen für das Abtöten verbrauchter Immunzellen
Da die Aufgabe des Fas‑Ligands darin besteht, aktivierte Zellen in den Tod zu schicken, testete das Team, wie gut Makrophagen Zielzellen töten können. Wurden normale Makrophagen mit aktivierten Helfer‑T‑Zellen oder mit einer Zelllinie, die besonders empfindlich auf Fas‑Signale reagiert, gemischt, starben viele Zielzellen im Verlauf. Im Gegensatz dazu schonten ZNRF1‑defiziente Makrophagen deutlich mehr dieser Zellen, selbst bei starker Stimulation. Diese verringerte Tötungsfähigkeit passt zu den Mausdaten: Können Makrophagen Fas‑Ligand nicht effizient an ihrer Oberfläche präsentieren, überleben aktivierte T‑Zellen länger, geben B‑Zellen mehr Unterstützung und treiben vergrößerte Milzen sowie erhöhte Antikörperproduktion voran.
Was das für die Kontrolle entgleister Immunantworten bedeutet
Insgesamt zeigen die Ergebnisse, dass ZNRF1 als eingebautes Sicherheitsbauteil fungiert, das die interne Bewegung von mit Fas‑Ligand gefüllten Vesikeln mit ihrer finalen Fusion an der Makrophagenoberfläche verknüpft. Funktioniert ZNRF1 normal, erreicht Fas‑Ligand die Außenseite der Zelle, sodass Makrophagen aktivierte T‑Zellen aussondern und Immunreaktionen im Zaum halten können. Fehlt ZNRF1, scheitert dieser Lieferschritt, die Oberflächenpräsentation von Fas‑Ligand bleibt niedrig und Immunzellen können freier proliferieren. Obwohl noch viel Arbeit nötig ist, bevor sich diese Erkenntnisse in Therapien übersetzen lassen, bietet die Studie einen konkreten molekularen Ansatzpunkt dafür, wie der Körper die Abschaltphase von Immunreaktionen feinjustiert.
Zitation: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Schlüsselwörter: Fas ligand, Makrophagen, Immunhomöostase, ZNRF1, T‑Zell‑Apoptose