Clear Sky Science · fr
Une carence en ZNRF1 perturbe le trafic du ligand Fas et l’équilibre immunitaire
Pourquoi cela compte pour notre santé immunitaire
Notre système immunitaire doit marcher sur une ligne fine : il doit attaquer les menaces comme les microbes ou les cellules sanguines étrangères, tout en s’éteignant avant que la réponse ne déraille. Cette étude met au jour un interrupteur de contrôle caché à l’intérieur d’une cellule immunitaire courante, le macrophage, qui aide à décider si des cellules immunitaires activées sont éliminées discrètement ou autorisées à continuer de se multiplier. Comprendre cet interrupteur pourrait éventuellement nous aider à mieux gérer des affections impliquant inflammation chronique, auto-immunité ou complications liées aux transfusions.
Un feu de circulation pour l’autodestruction immunitaire
Lorsque les cellules immunitaires ont accompli leur tâche, beaucoup sont éliminées via un signal d’autodestruction impliquant une molécule de surface appelée ligand Fas. Le ligand Fas d’une cellule déclenche la mort d’une autre cellule portant son récepteur correspondant, aidant ainsi à réduire les réponses excessives. La majorité des recherches s’est concentrée sur la quantité de ligand Fas produite par une cellule. Ici, les auteurs posent une question différente : comment le ligand Fas est‑il acheminé depuis des compartiments de stockage internes vers la surface externe des macrophages au bon moment, et que se passe‑t‑il si cette étape de livraison échoue ?
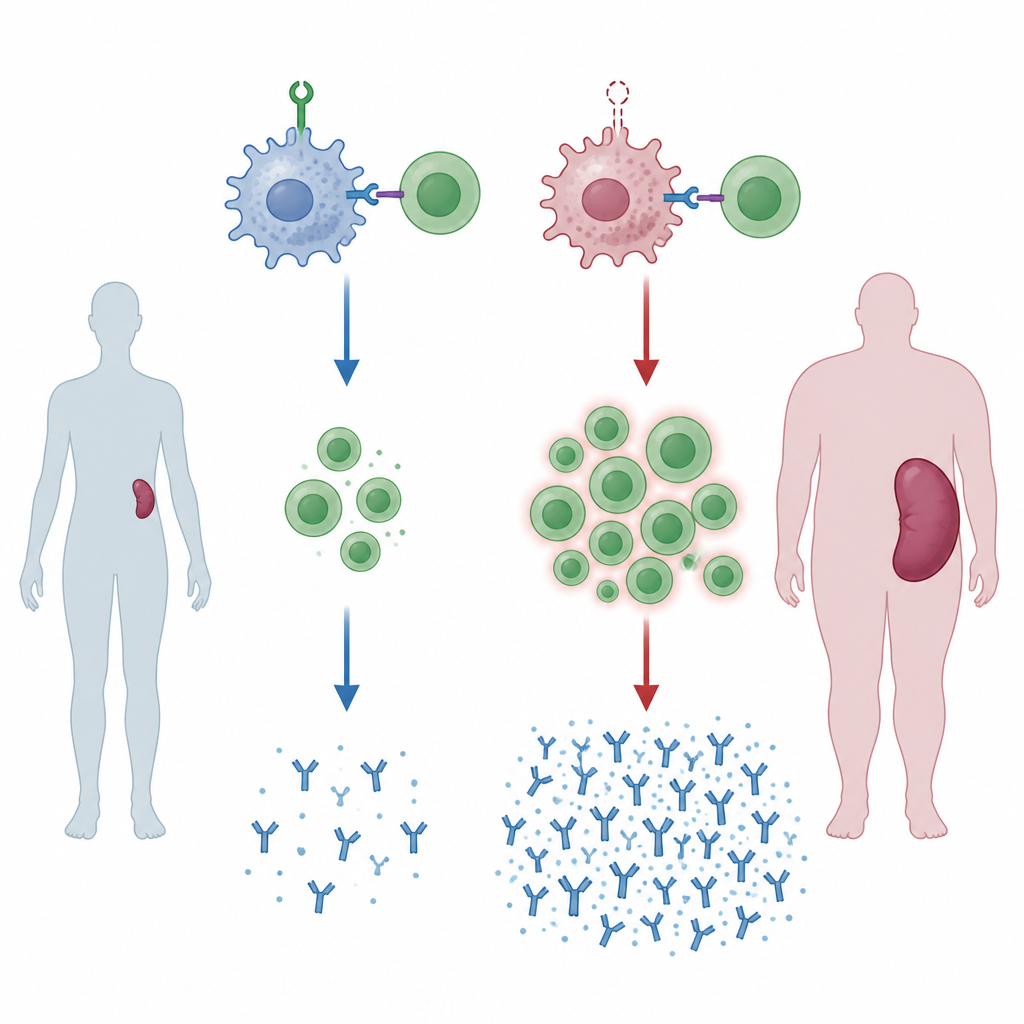
Un gardien manquant entraîne des rateaux enflées
L’équipe a généré des souris dont les cellules myéloïdes, y compris les macrophages, sont dépourvues d’une protéine appelée ZNRF1. En vieillissant, ces souris ont développé une augmentation de volume de la rate, signe d’une activation immunitaire chronique. Lorsque les animaux ont été exposés à du sang étranger, simulant une transfusion d’un donneur génétiquement différent, les changements sont devenus plus marqués. Leurs rates présentaient des régions élargies où les cellules B et T interagissent et se multiplient, et le rapport entre cellules T auxiliaires et cellules T tueuses s’est déplacé vers le haut. Ces souris produisaient également des quantités plus élevées de certaines classes d’anticorps dirigés contre le sang du donneur, indiquant que, sans ZNRF1 dans les cellules myéloïdes, le système immunitaire est prêt à répondre de manière excessive.
Signal de surface bloqué tandis que la cargaison s’accumule à l’intérieur
Pour comprendre le rôle de ZNRF1 dans les macrophages, les chercheurs sont passés à des cultures cellulaires. Ils ont stimulé des macrophages normaux et dépourvus de ZNRF1 avec des composants bactériens ou des bactéries vivantes et ont mesuré le ligand Fas. Surprise : les cellules sans ZNRF1 produisaient globalement beaucoup de ligand Fas, souvent même davantage que les cellules normales, mais elles ne parvenaient pas à l’exposer à leur surface. Au microscope, les compartiments de stockage internes marqués par la protéine LAMP1 se déplaçaient encore vers le bord cellulaire dans les deux types de cellules, mais dans les cellules déficientes en ZNRF1 la cargaison de ligand Fas ne suivait pas ce trajet vers le cortex et restait coincée près du centre. Cela indique une défaillance tardive lors de l’étape d’arrimage ou de fusion plutôt qu’un problème de synthèse ou de stockage initial du ligand Fas.
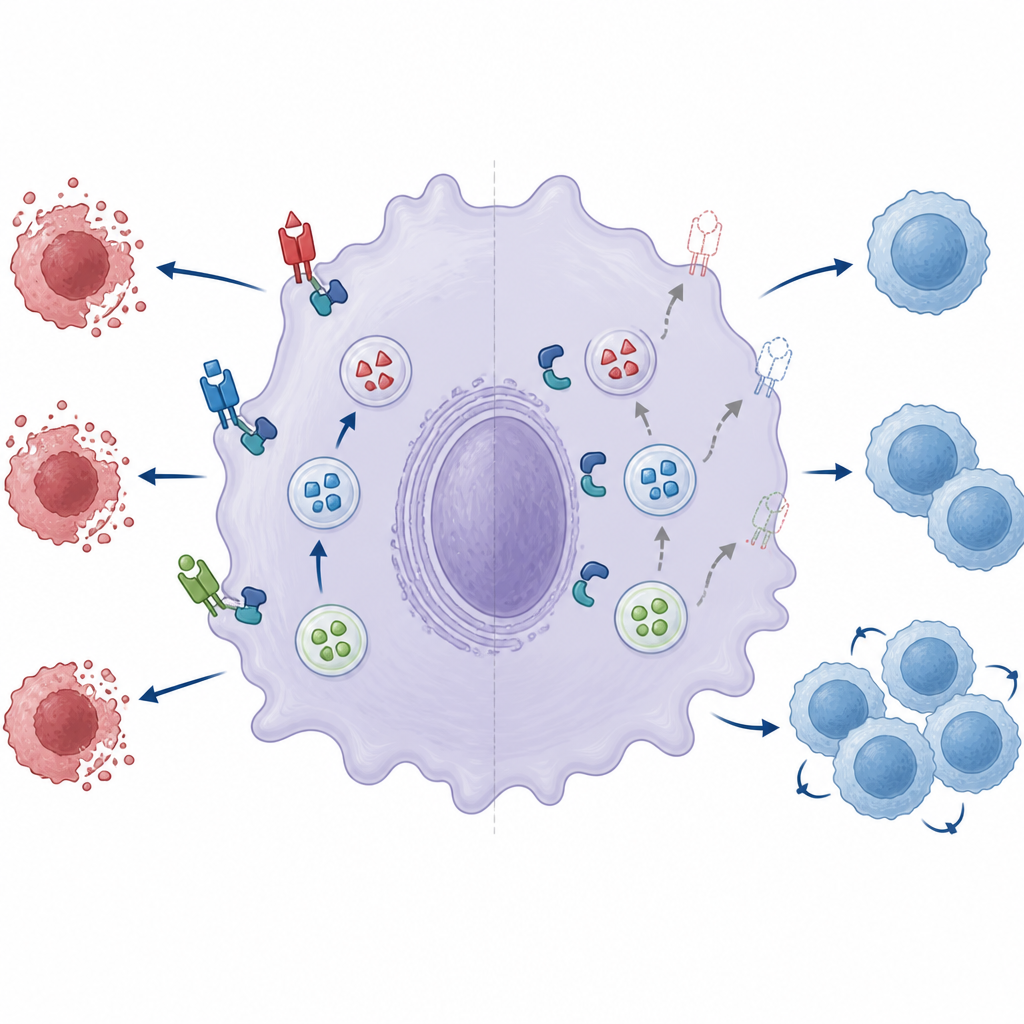
Une machinerie de fusion cassée affaiblit le frein immunitaire
Les auteurs ont ensuite examiné deux composants clés de la mini‑machinerie de fusion qui permet aux vésicules de stockage de fusionner avec la membrane cellulaire : une paire de protéines nommées Munc18‑2 et Syntaxin‑3. Dans les macrophages normaux, ces deux partenaires forment un complexe qui aide les vésicules à s’ouvrir et à libérer leur cargaison. En l’absence de ZNRF1, le partenariat entre Munc18‑2 et Syntaxin‑3 était nettement affaibli. La réduction supplémentaire des niveaux de Munc18‑2 diminuait encore le ligand Fas de surface, soulignant son importance. La réintroduction de ZNRF1 fonctionnel dans les cellules déficientes améliorait l’exposition du ligand Fas, mais une version catalytiquement inactive de ZNRF1 ne le faisait pas, suggérant que l’activité enzymatique de ZNRF1 est nécessaire pour rendre la machinerie de fusion entièrement opérationnelle, même si le complexe peut encore s’assembler.
Conséquences pour l’élimination des cellules immunitaires épuisées
Parce que le rôle du ligand Fas est d’induire la mort des cellules activées, l’équipe a testé l’efficacité des macrophages à tuer des cellules cibles. Lorsque des macrophages normaux ont été mis en contact avec des lymphocytes T auxiliaires activés ou avec une lignée cellulaire très sensible aux signaux Fas, beaucoup de cibles sont mortes avec le temps. En revanche, les macrophages déficients en ZNRF1 ont épargné beaucoup plus de ces cellules, même lorsqu’elles étaient fortement stimulées. Cette capacité réduite à tuer concorde avec les données chez la souris : si les macrophages ne peuvent pas exposer efficacement le ligand Fas à leur surface, les lymphocytes T activés survivent plus longtemps, apportent davantage d’aide aux cellules B et alimentent des rates hypertrophiées ainsi qu’une production d’anticorps augmentée.
Ce que cela signifie pour le contrôle d’une immunité incontrôlée
Ensemble, ces résultats révèlent ZNRF1 comme un dispositif de sécurité intégré qui relie le mouvement interne des paquets remplis de ligand Fas à leur fusion finale avec la surface du macrophage. Quand ZNRF1 fonctionne normalement, le ligand Fas atteint l’extérieur de la cellule, permettant aux macrophages d’éliminer les lymphocytes T activés et de maintenir les réactions immunitaires sous contrôle. Lorsque ZNRF1 est absent, cette étape de livraison échoue, le ligand Fas de surface reste bas et les cellules immunitaires peuvent proliférer plus librement. Bien que beaucoup de travail reste à faire avant que ces connaissances puissent être traduites en thérapies, l’étude met en lumière une poignée moléculaire spécifique par laquelle l’organisme ajuste la phase d’extinction des réponses immunitaires.
Citation: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Mots-clés: ligand Fas, macrophages, homéostasie immune, ZNRF1, apoptose des lymphocytes T