Clear Sky Science · ru
Дефицит ZNRF1 нарушает транспортировку лиганда Fas и иммунный баланс
Почему это важно для нашего иммунного здоровья
Наш иммунитет вынужден балансировать: он должен атаковать угрозы, такие как микробы и чужеродные клетки крови, и одновременно отключаться до того, как ответ выйдет из-под контроля. В этом исследовании обнаружен скрытый механизм в обычной иммунной клетке — макрофаге — который помогает решать, будут ли активированные клетки тихо удалены или смогут продолжать размножаться. Понимание этого переключателя в перспективе может помочь лучше управлять состояниями с хроническим воспалением, аутоиммунными заболеваниями или осложнениями после переливания.
Светофор для иммунной самоуничтожения
Когда иммунные клетки выполнили свою работу, многие из них устраняются с помощью встроенного сигнала самоуничтожения, включающего молекулу на поверхности — лиганд Fas. Лиганд Fas на одной клетке вызывает гибель другой клетки, несущей соответствующий рецептор, что помогает сократить чрезмерную активность. Большинство работ фокусировались на том, сколько лиганда Fas синтезирует клетка. Авторы поставили иной вопрос: как лиганд Fas перемещается из внутренних резервуаров на поверхность макрофагов в нужный момент и что происходит, если этот этап доставки нарушается?
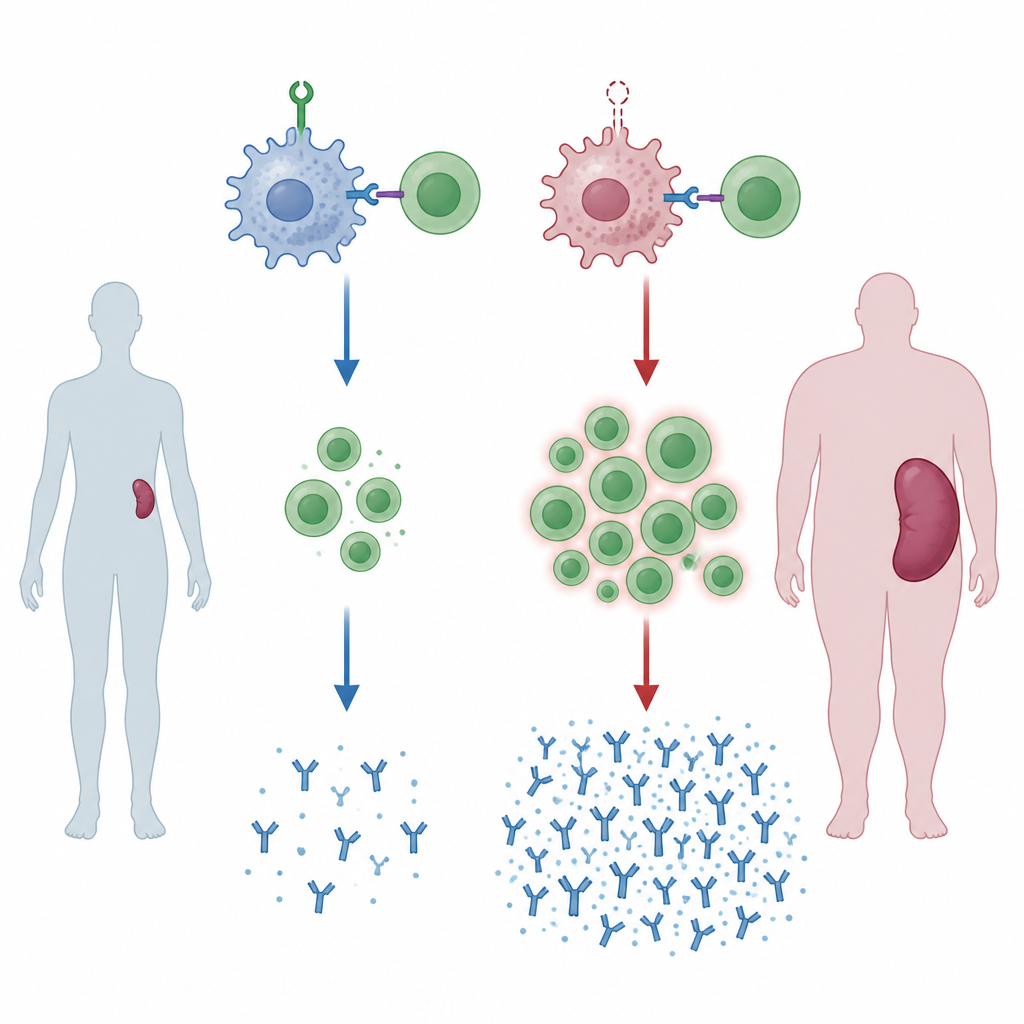
Отсутствующий страж приводит к увеличению селезенки
Команда создала мышей, у которых миелоидные клетки, включая макрофаги, лишены белка ZNRF1. По мере старения у этих животных селезенка увеличивалась — признак хронической активации иммунной системы. При воздействии чужой крови, имитирующем переливание от генетически отличного донора, изменения становились еще более заметными. В селезенке расширялись области, где взаимодействуют и размножаются В‑ и Т‑клетки, а соотношение хелперов к киллерам сдвигалось в пользу первых. Кроме того, такие мыши продуцировали больше определённых классов антител против донорской крови, что указывает на то, что при отсутствии ZNRF1 в миелоидных клетках иммунная система склонна к чрезмерному ответу.
Сигнал на поверхности блокируется, пока грузы накапливаются внутри
Чтобы понять функцию ZNRF1 в макрофагах, исследователи перешли к культуре клеток. Они стимулировали нормальные и лишённые ZNRF1 макрофаги компонентами бактерий или живыми бактериями и измеряли уровни лиганда Fas. Удивительно, но клетки без ZNRF1 в целом синтезировали много лиганда Fas, часто даже больше, чем нормальные клетки, однако не могли отобразить его на своей поверхности. Под микроскопом внутренние резервуары, отмеченные белком LAMP1, всё равно перемещались к периферии клетки в обоих типах клеток, но у клеток без ZNRF1 груз с лигандом Fas не шёл с ними к коре и оставался застрявшим ближе к центру. Это указывало на сбой на позднем этапе — при стыковке или слиянии — а не на проблему синтеза или начального хранения лиганда Fas.
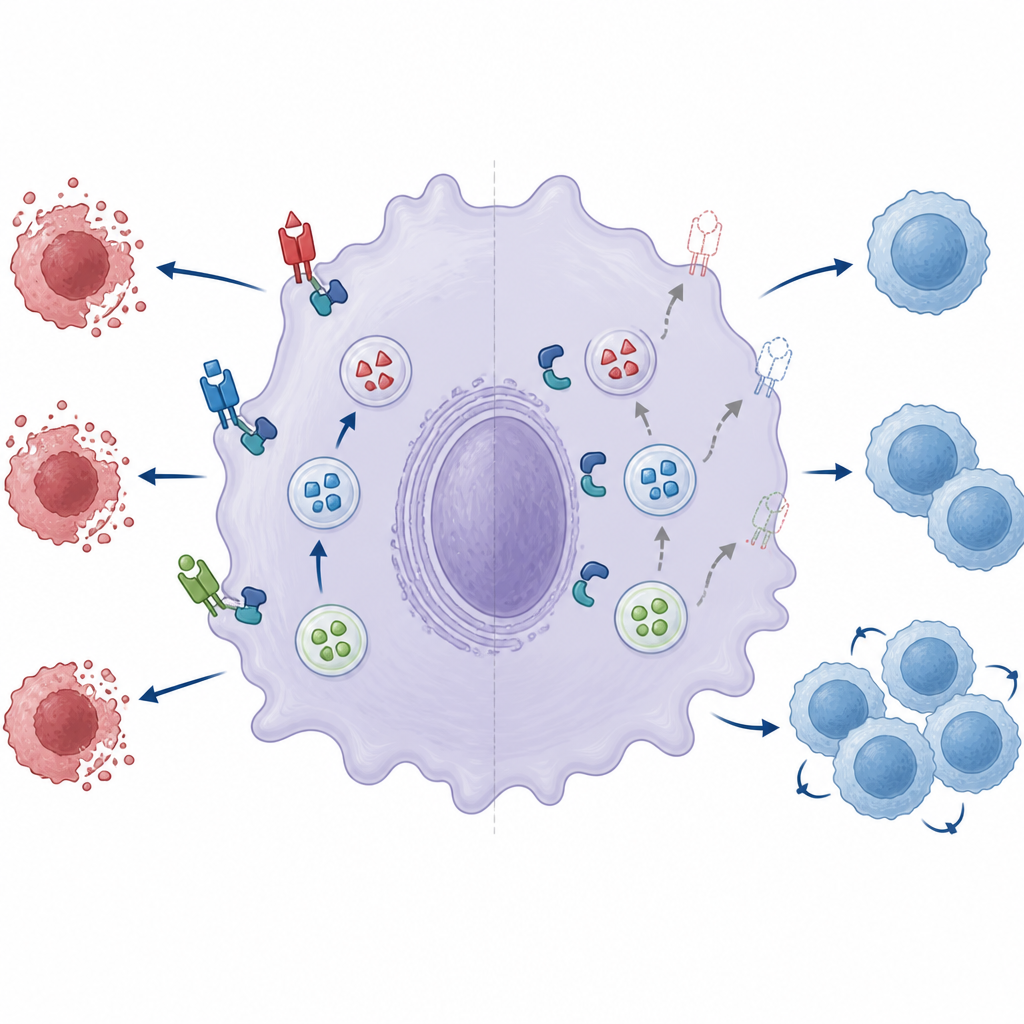
Неисправный «механизм слияния» ослабляет тормоз иммунитета
Далее авторы изучили два ключевых компонента микроаппарата слияния, который позволяет везикулам объединяться с клеточной мембраной: пару белков Munc18‑2 и Syntaxin‑3. В нормальных макрофагах эти два партнёра формируют комплекс, облегчающий открытие везикул и выпуск их груза. При отсутствии ZNRF1 партнёрство между Munc18‑2 и Syntaxin‑3 было заметно слабее. Дальнейшее снижение уровня Munc18‑2 ещё сильнее уменьшало количество лиганда Fas на поверхности, подчёркивая его важность. Повторное введение нормального ZNRF1 в дефицитные клетки улучшало экспрессию лиганда Fas, тогда как каталитически неактивная версия ZNRF1 не давала эффекта, что говорит о необходимости ферментативной активности ZNRF1 для полноценной работы аппарата слияния, даже если сам комплекс по‑прежнему может собираться.
Последствия для уничтожения отживших иммунных клеток
Поскольку задача лиганда Fas — вызывать гибель активированных клеток, команда проверила, насколько эффективно макрофаги могут убивать мишенные клетки. В сочетании с активированными хелперными Т‑клетками или с клеточной линией, сильно чувствительной к сигналам Fas, нормальные макрофаги вызывали гибель многих мишеней со временем. В отличие от них, макрофаги без ZNRF1 щадили значительно больше таких клеток, даже при мощной стимуляции. Снижение способности к инициации гибели согласуется с данными по мышам: если макрофаги не могут эффективно выставлять лиганд Fas на поверхности, активированные Т‑клетки дольше выживают, оказывают больше помощи В‑клеткам и способствуют увеличению селезенки и усиленному образованию антител.
Что это значит для контроля неконтролируемого иммунитета
Вместе результаты показывают, что ZNRF1 выполняет функцию встроенного предохранителя, связывающего внутреннее перемещение пакетов, наполненных лигандом Fas, с их финальным слиянием с поверхностью макрофага. При нормальной работе ZNRF1 лиганд Fas достигает внешней стороны клетки, позволяя макрофагам отсеивать активированные Т‑клетки и сдерживать иммунные реакции. При отсутствии ZNRF1 этот этап доставки нарушается, поверхность остаётся бедной на лиганд Fas, и иммунные клетки получают возможность свободнее размножаться. Хотя предстоит ещё много работы, прежде чем эти открытия можно будет превратить в терапевтические подходы, исследование выделяет конкретную молекулярную «ручку», с помощью которой организм тонко регулирует фазу выключения иммунного ответа.
Цитирование: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Ключевые слова: Лиганд Fas, макрофаги, иммунное гомеостаз, ZNRF1, апоптоз Т‑клеток