Clear Sky Science · pt
Deficiência de ZNRF1 atrapalha o tráfego do ligante Fas e o equilíbrio imune
Por que isso importa para nossa saúde imunológica
Nosso sistema imune precisa caminhar por uma linha tênue: deve atacar ameaças como micróbios e células sanguíneas estranhas, mas também se desligar antes que a resposta saia do controle. Este estudo revela um interruptor de controle oculto dentro de uma célula imune comum chamada macrófago que ajuda a decidir se células imunes ativadas são removidas discretamente ou podem continuar a se multiplicar. Entender esse interruptor pode, no futuro, nos ajudar a manejar melhor condições envolvendo inflamação crônica, autoimunidade ou complicações de transfusão.
Um semáforo para a autodestruição imune
Quando as células imunes cumprem sua função, muitas são eliminadas por um sinal de autodestruição que envolve uma molécula de superfície chamada ligante Fas. O ligante Fas em uma célula desencadeia morte em outra que carrega o receptor correspondente, ajudando a reduzir respostas excessivas. A maior parte das pesquisas se concentrou em quanto ligante Fas uma célula produz. Aqui, os autores fizeram outra pergunta: como o ligante Fas é transportado de compartimentos de armazenamento internos para a superfície externa dos macrófagos no momento certo, e o que acontece se essa etapa de entrega falha?
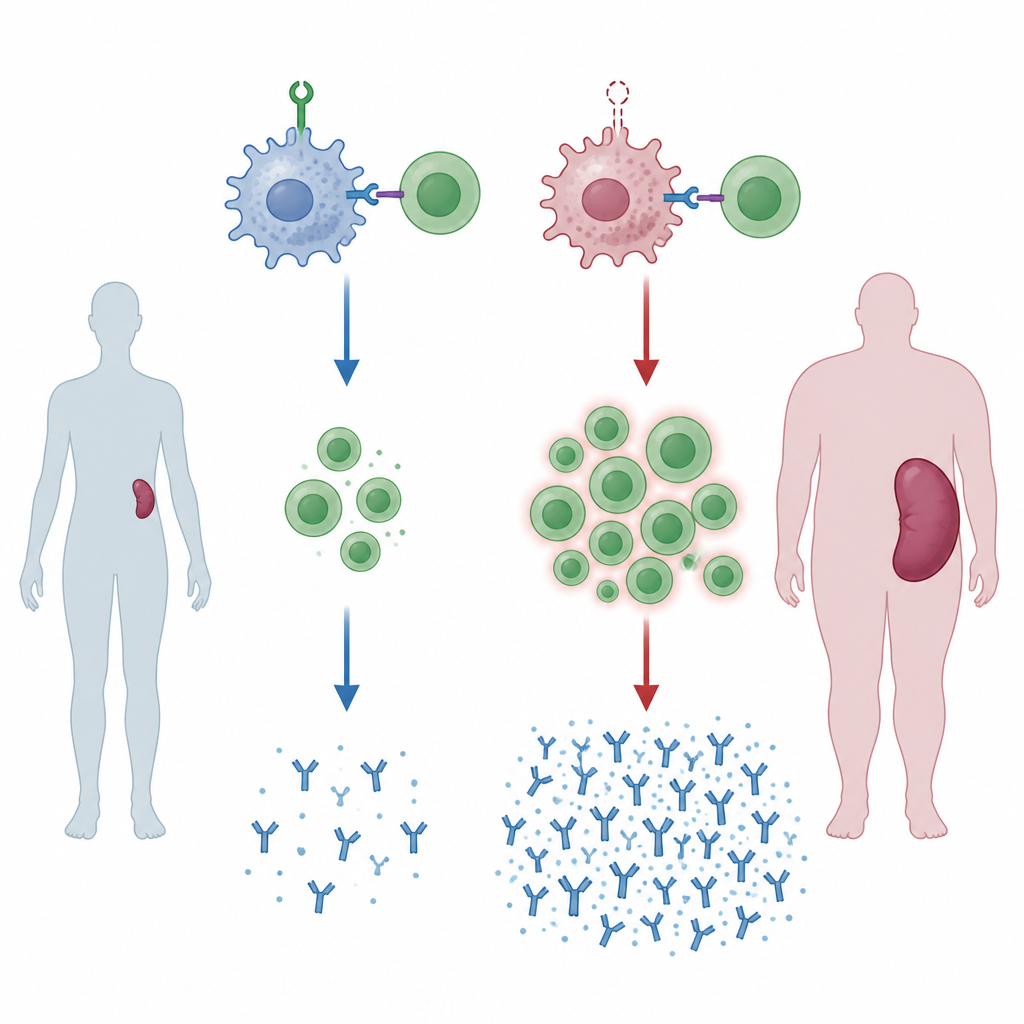
Um guardião ausente leva a baços inchados
A equipe criou camundongos cujas células mieloides, incluindo macrófagos, não têm a proteína ZNRF1. À medida que esses animais envelheceram, seus baços aumentaram de tamanho, um sinal de ativação imune crônica. Quando os animais foram expostos a sangue estranho, simulando uma transfusão de um doador geneticamente diferente, as alterações ficaram mais pronunciadas. Seus baços exibiram regiões expandidas onde células B e T interagem e se multiplicam, e a proporção de células T auxiliares para células T citotóxicas aumentou. Esses camundongos também produziram maiores quantidades de certas classes de anticorpos contra o sangue do doador, indicando que, sem ZNRF1 nas células mieloides, o sistema imune está predisposto a reagir com exagero.
Sinal de superfície bloqueado enquanto carga se acumula internamente
Para entender o que ZNRF1 faz dentro dos macrófagos, os pesquisadores usaram cultura celular. Estimularam macrófagos normais e deficientes em ZNRF1 com componentes bacterianos ou com bactérias vivas e mediram o ligante Fas. Surpreendentemente, as células sem ZNRF1 produziam bastante ligante Fas no total, muitas vezes até mais que as células normais, mas não o exibiam na superfície. Ao microscópio, compartimentos de armazenamento internos marcados pela proteína LAMP1 ainda se moviam em direção à periferia celular em ambos os tipos, mas nas células deficientes em ZNRF1 a carga de ligante Fas não os acompanhava até o córtex e permanecia presa perto do centro. Isso aponta para uma falha tardia na etapa de ancoragem ou fusão, em vez de um problema na produção ou armazenamento inicial do ligante Fas.
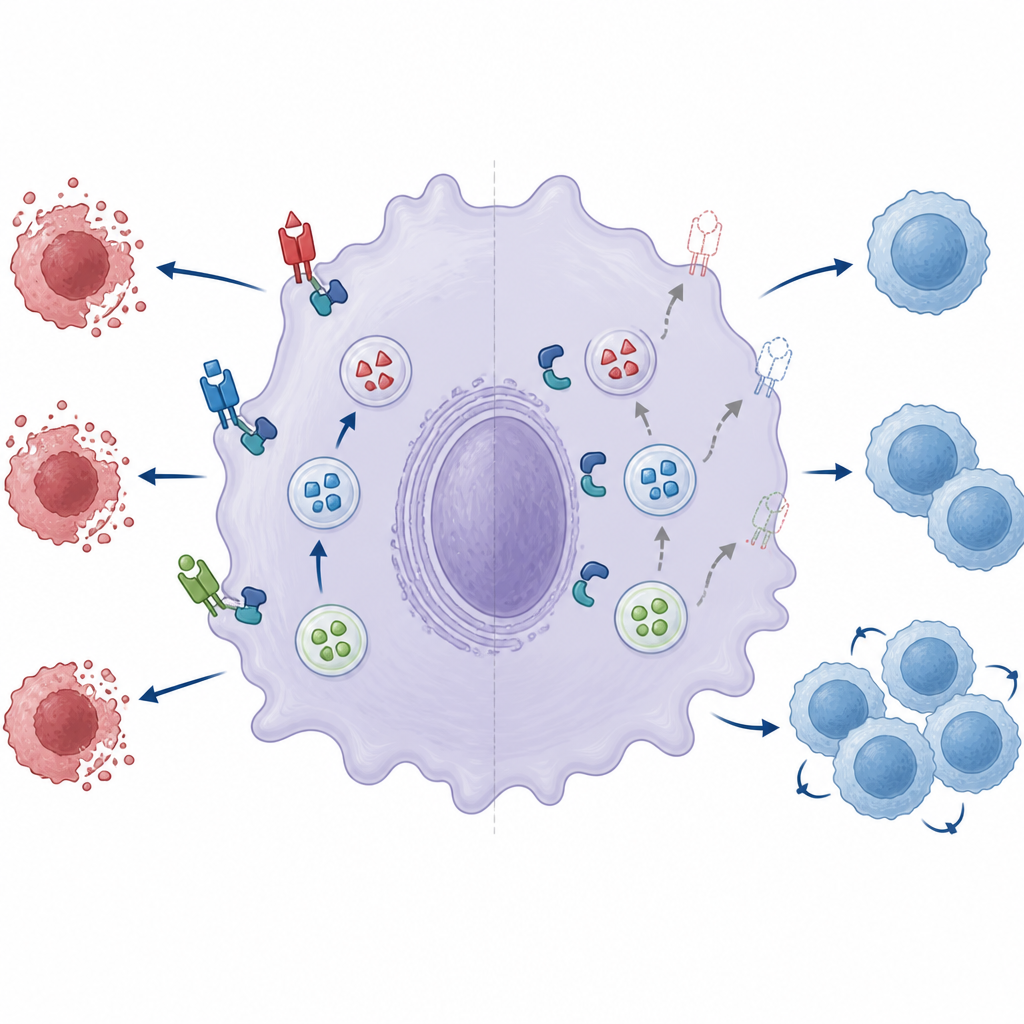
Uma máquina de fusão comprometida enfraquece o freio imune
Os autores então examinaram dois componentes-chave da pequena máquina de fusão que permite que vesículas de armazenamento se fundam com a superfície celular: um par de proteínas chamadas Munc18‑2 e Syntaxin‑3. Em macrófagos normais, esses dois parceiros formam um complexo que ajuda as vesículas a abrir-se e liberar sua carga. Quando ZNRF1 estava ausente, a parceria entre Munc18‑2 e Syntaxin‑3 estava marcadamente mais fraca. Reduzir ainda mais os níveis de Munc18‑2 diminuiu a quantidade de ligante Fas na superfície, ressaltando sua importância. Reintroduzir ZNRF1 funcional em células deficientes melhorou a exibição do ligante Fas, mas uma versão cataliticamente inativa de ZNRF1 não o fez, sugerindo que a atividade enzimática de ZNRF1 é necessária para tornar a máquina de fusão totalmente competente, mesmo que o complexo possa ainda se montar.
Consequências para eliminar células imunes já gastas
Como a função do ligante Fas é desencadear a morte em células ativadas, a equipe testou quão bem os macrófagos conseguiam eliminar células‑alvo. Quando macrófagos normais foram misturados com células T auxiliares ativadas ou com uma linhagem celular altamente sensível a sinais Fas, muitos alvos morreram ao longo do tempo. Em contraste, macrófagos deficientes em ZNRF1 pouparam bem mais dessas células, mesmo quando fortemente estimuladas. Essa capacidade reduzida de matar corrobora os dados dos camundongos: se os macrófagos não conseguem expor eficientemente o ligante Fas na superfície, as células T ativadas sobrevivem por mais tempo, fornecendo mais ajuda às células B e alimentando o aumento do tamanho do baço e a produção ampliada de anticorpos.
O que isso significa para controlar a imunidade descontrolada
Em conjunto, os achados revelam ZNRF1 como um dispositivo de segurança incorporado que liga o movimento interno de pacotes cheios de ligante Fas à sua fusão final com a superfície do macrófago. Quando o ZNRF1 funciona normalmente, o ligante Fas alcança o exterior da célula, permitindo que os macrófagos eliminem células T ativadas e mantenham as reações imunes sob controle. Quando o ZNRF1 está ausente, essa etapa de entrega falha, o ligante Fas de superfície permanece baixo e as células imunes ficam livres para proliferar mais. Embora muito trabalho ainda seja necessário antes que essas descobertas possam ser traduzidas em terapias, o estudo destaca um ponto molecular específico pelo qual o corpo ajusta a fase de desligamento das respostas imunes.
Citação: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Palavras-chave: ligante Fas, macrófagos, homeostase imune, ZNRF1, apoptose de células T