Clear Sky Science · es
La deficiencia de ZNRF1 altera el tráfico del ligando Fas y el equilibrio inmunitario
Por qué importa para nuestra salud inmunitaria
El sistema inmunitario debe mantener un equilibrio delicado: atacar amenazas como microbios y células sanguíneas extrañas, pero apagarse antes de que la respuesta se descontrole. Este estudio descubre un interruptor de control oculto dentro de una célula inmunitaria común, el macrófago, que ayuda a decidir si las células inmunitarias activadas se eliminan discretamente o se les permite seguir multiplicándose. Entender este interruptor podría, a la larga, ayudarnos a manejar mejor condiciones asociadas con inflamación crónica, autoinmunidad o complicaciones por transfusión.
Un semáforo para la autodestrucción inmunitaria
Cuando las células inmunitarias han cumplido su función, muchas se eliminan mediante una señal de autodestrucción que implica una molécula de superficie llamada ligando Fas. El ligando Fas de una célula desencadena la muerte en otra que porta su receptor correspondiente, ayudando a recortar respuestas sobreactivadas. La mayor parte de la investigación se ha centrado en cuánto ligando Fas produce una célula. Aquí, los autores plantearon una pregunta diferente: ¿cómo se transporta el ligando Fas desde compartimentos internos hasta la superficie externa de los macrófagos en el momento justo, y qué ocurre si ese paso de entrega falla?
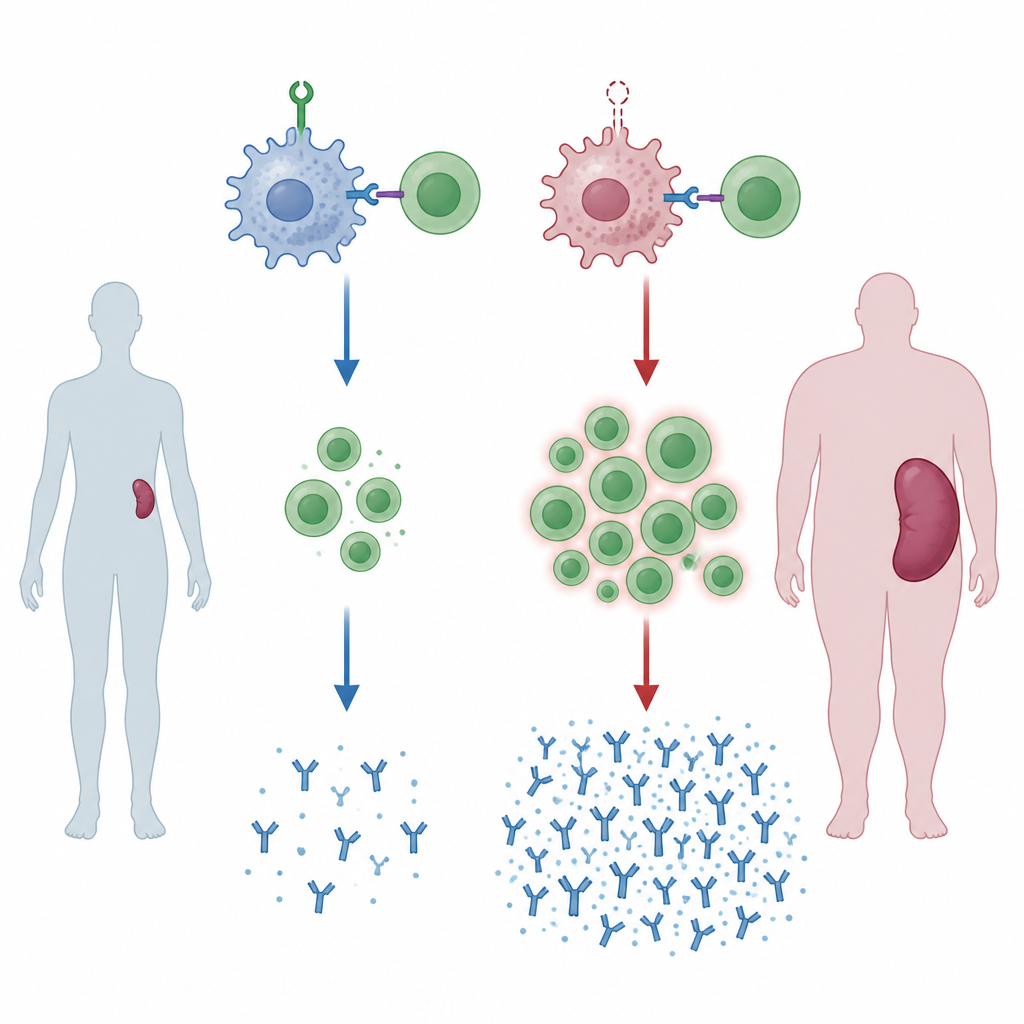
Un guardián ausente provoca bazo agrandado
El equipo generó ratones cuyos células mieloides, incluidos los macrófagos, carecen de una proteína llamada ZNRF1. A medida que estos ratones envejecían, sus bazos se agrandaron, signo de activación inmune crónica. Cuando los animales fueron expuestos a sangre extraña, simulando una transfusión de un donante genéticamente distinto, los cambios fueron más llamativos. Sus bazos mostraron regiones ampliadas donde interactúan y se multiplican células B y T, y la proporción de células T colaboradoras frente a citotóxicas aumentó. Estos ratones también produjeron mayores cantidades de ciertas clases de anticuerpos contra la sangre donada, lo que indica que, sin ZNRF1 en las células mieloides, el sistema inmunitario está predispuesto a responder con demasiada intensidad.
Se bloquea la señal de superficie mientras la carga se acumula en el interior
Para entender qué hace ZNRF1 dentro de los macrófagos, los investigadores recurrieron a cultivos celulares. Estimularon macrófagos normales y deficientes en ZNRF1 con componentes bacterianos o bacterias vivas y midieron el ligando Fas. Sorprendentemente, las células sin ZNRF1 producían mucho ligando Fas en conjunto, a menudo incluso más que las células normales, pero no lo mostraban en su superficie. Al microscopio, los compartimentos de almacenamiento internos marcados por la proteína LAMP1 todavía se movían hacia el borde celular en ambos tipos celulares, pero en las células deficientes en ZNRF1 la carga de ligando Fas no los acompañaba hasta la corteza y permanecía atrapada cerca del centro. Esto apuntó a una falla tardía en el paso de anclaje o fusión más que a un problema en la síntesis o almacenamiento inicial del ligando Fas.
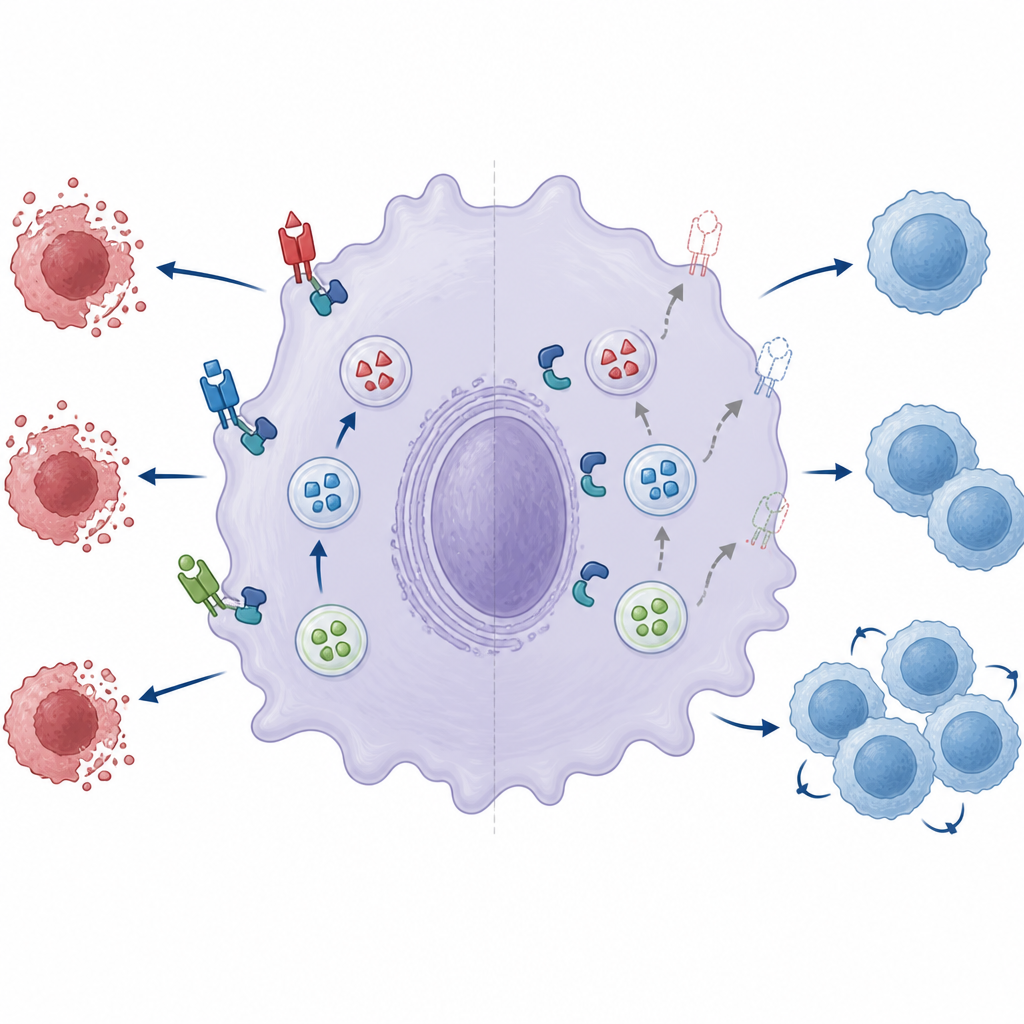
Una máquina de fusión rota debilita el freno inmune
Los autores examinaron entonces dos componentes clave de la pequeña maquinaria de fusión que permite que las vesículas de almacenamiento se integren con la superficie celular: un par de proteínas llamadas Munc18‑2 y Syntaxin‑3. En macrófagos normales, estos dos socios forman un complejo que ayuda a que las vesículas se abran y liberen su carga. Cuando faltaba ZNRF1, la asociación entre Munc18‑2 y Syntaxin‑3 era notablemente más débil. Reducir aún más los niveles de Munc18‑2 disminuyó la cantidad de ligando Fas en la superficie, subrayando su importancia. Reintroducir ZNRF1 normal en las células deficientes mejoró la exposición del ligando Fas, pero una versión catalíticamente inactiva de ZNRF1 no lo hizo, lo que sugiere que la actividad enzimática de ZNRF1 es necesaria para que la maquinaria de fusión sea plenamente competente, incluso si el complejo puede aún ensamblarse.
Consecuencias para eliminar células inmunitarias gastadas
Puesto que la función del ligando Fas es desencadenar la muerte en células activadas, el equipo probó la capacidad de los macrófagos para matar células diana. Cuando macrófagos normales se mezclaron con linfocitos T colaboradores activados o con una línea celular altamente sensible a señales Fas, muchas dianas murieron con el tiempo. En contraste, los macrófagos deficientes en ZNRF1 perdonaron a muchas más de estas células, incluso cuando estaban fuertemente estimuladas. Esta capacidad de muerte reducida concuerda con los datos en ratones: si los macrófagos no pueden exponer eficazmente el ligando Fas en su superficie, los linfocitos T activados sobreviven más tiempo, proporcionan más ayuda a las células B y alimentan el agrandamiento del bazo y el aumento de producción de anticuerpos.
Qué significa esto para controlar una inmunidad desbocada
En conjunto, los hallazgos revelan a ZNRF1 como un dispositivo de seguridad integrado que vincula el movimiento interno de paquetes llenos de ligando Fas con su fusión final en la superficie del macrófago. Cuando ZNRF1 funciona con normalidad, el ligando Fas llega al exterior de la célula, lo que permite a los macrófagos eliminar linfocitos T activados y mantener las reacciones inmunitarias bajo control. Cuando ZNRF1 está ausente, este paso de entrega falla, el ligando Fas en superficie se mantiene bajo y las células inmunitarias quedan libres para proliferar con mayor facilidad. Aunque queda mucho trabajo antes de que estos conocimientos puedan traducirse en terapias, el estudio destaca un punto molecular concreto mediante el cual el organismo ajusta la fase de apagado de las respuestas inmunitarias.
Cita: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Palabras clave: Ligando Fas, macrófagos, homeostasis inmunitaria, ZNRF1, apoptosis de linfocitos T