Clear Sky Science · he
חסר ב‑ZNRF1 משבש מסלול הובלת Fas ligand ומאזן חיסוני
מדוע זה חשוב לבריאות החיסונית שלנו
מערכת החיסון שלנו חייבת לשמור על איזון עדין: עליה לתקוף איומים כמו מיקרובים ותאי דם זרים, אך גם לכבות את עצמה לפני שהתגובה תתפרץ. המחקר הזה מגלה מתג בקרת עומק בתוך תא חיסוני שכיח שנקרא מאקרופאג, המסייע להכריע האם תאי חיסון מנותקים מוסרים בשקט או מורשים להמשיך ולשכפל. הבנת המתג הזה עשויה לעזור בסופו של דבר לנהל טוב יותר מצבים של דלקת כרונית, אוטואימוניות או סיבוכים מהעברות דם.
אור תנועה להשמדה עצמית חיסונית
כשאתרי החיסון השלימו את תפקידם, רבים מהם מוסרים באמצעות סיגנל השמדה עצמי הכולל מולקולה על פני השטח שנקראת Fas ligand. Fas ligand בתא אחד מפעיל מוות בתא אחר הנושא את הקולטן התואם, ועוזר לקצץ תגובות יתר. רוב המחקר התמקד בכמה Fas ligand תא מייצר. כאן, המחברים שאלו שאלה שונה: כיצד Fas ligand מועבר ממחסני הפנימיים אל פני השטח של המאקרופאגים ברגע הנכון, ומה קורה אם שלב ההעברה הזה נכשל?
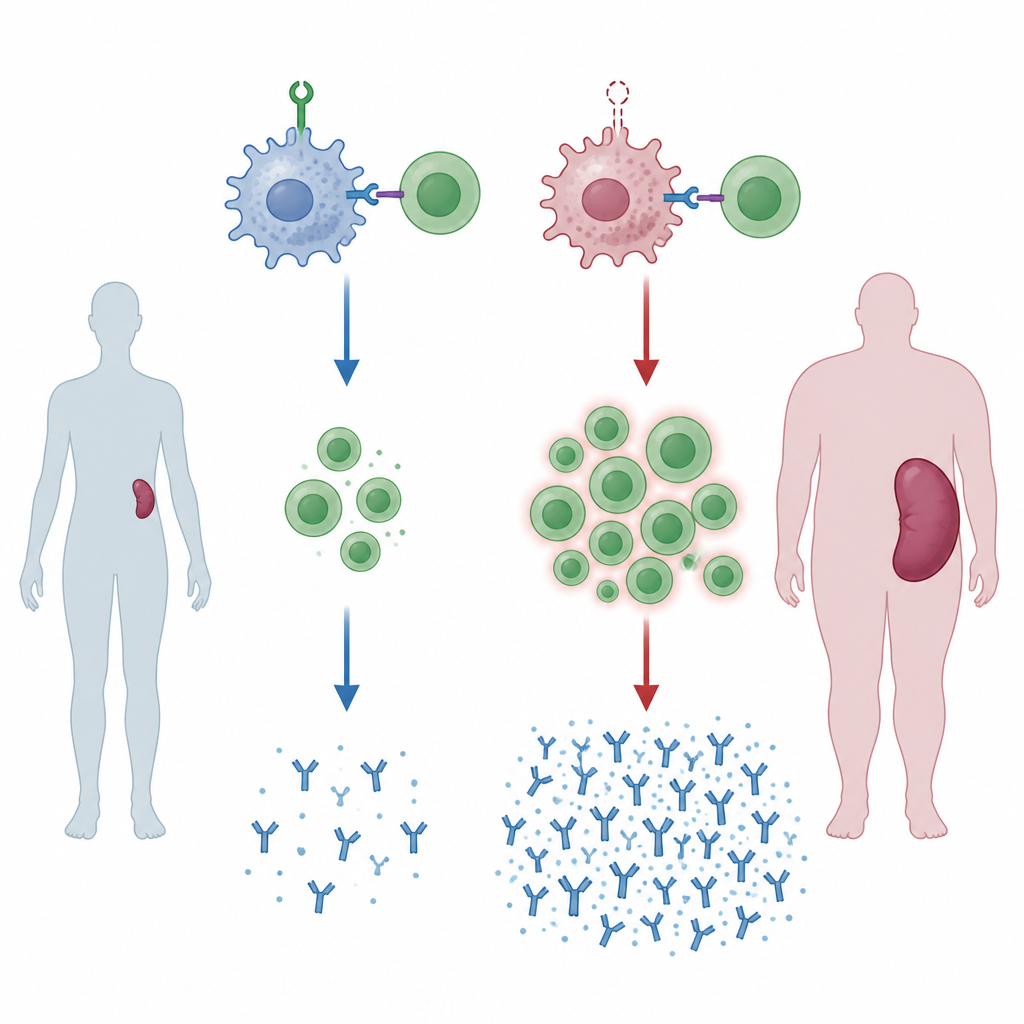
שומר נעדר מוביל לטחולים מוגדלים
הקבוצה הנדסה עכברים שלתאי המיאלואידים שלהם, כולל מאקרופאגים, חסר החלבון ZNRF1. ככל שעכברים אלה התבגרו, טחוליהם התרחבו, סימן להפעלה חיסונית כרונית. כשהחיות נחשפו לדם זר, המדמה העברה ממוריש גנטי שונה, השינויים הפכו בולטים יותר. בחתכי הטחול נראו אזורים מורחבים שבהם תאי B ותאי T מתקשרים ומתרבים, ומאזן תאי העזר מול תאי הקילר הוסט כלפי מעלה. עכברים אלו גם ייצרו כמויות גבוהות יותר של סוגי נוגדנים מסוימים נגד דם התורם, מה שמעיד שבחסר ZNRF1 בתאי מיאלואיד המערכת החיסונית ערוכה להגיב בעוצמה רבה מדי.
סיגנל פני שטח חסום בעוד המטען מצטבר בפנים
כדי להבין מה עושה ZNRF1 בתוך המאקרופאגים, החוקרים פנו לתרבית תאים. הם גירו מאקרופאגים נורמליים וחסרי ZNRF1 ברכיבים חיידקיים או בחיידקים חיים ומדדו Fas ligand. במפתיע, תאים חסרי ZNRF1 ייצרו כמות מספקת של Fas ligand בסך הכל, לעתים אפילו יותר מתאים רגילים, אך נכשלו להצגתו על פני השטח. במיקרוסקופ נראו מחסני פנימיים המסומנים בחלבון LAMP1 שנעים לכיוון שפת התא בשני סוגי התאים, אך בתאים חסרי ZNRF1 מטען ה‑Fas ligand לא נסע איתם אל הקורטקס ונשאר תקוע בקרבה למרכז. הדבר מצביע על כשל מאוחר בשלב העגינה או המיזוג ולא על בעיה בייצור או באחסון הראשוני של Fas ligand.
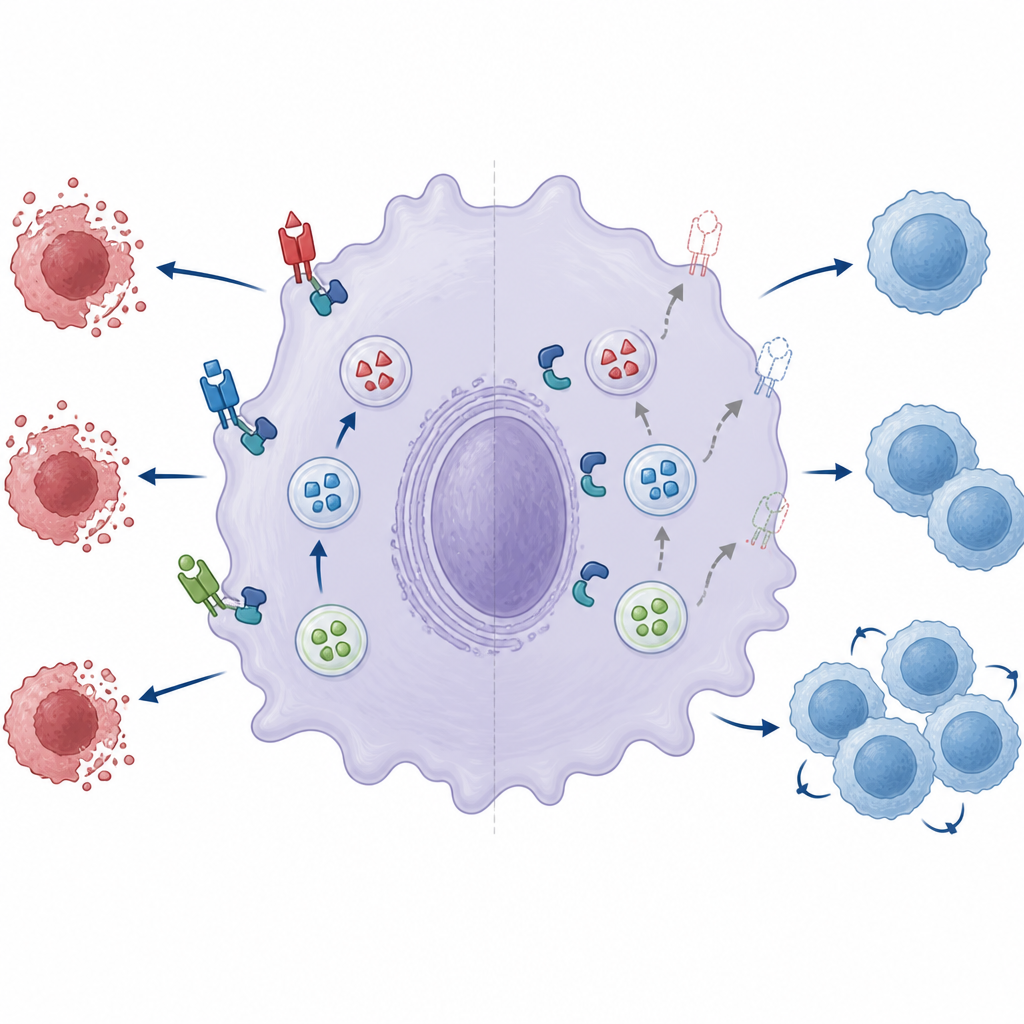
מכונת מיזוג פגומה מחלישה את הבלימה החיסונית
המחברים בחנו אז שני מרכיבים מרכזיים של מכונת המיזוג הקטנה שמאפשרת לווסיקולות האחסון להתמזג עם פני התא: זוג החלבונים Munc18‑2 ו‑Syntaxin‑3. במאקרופאגים נורמליים, שני שותפים אלו יוצרים קומפלקס המסייע לפתיחת הווסיקולות ושחרור המטען. כאשר ZNRF1 נעדר, השותפות בין Munc18‑2 ל‑Syntaxin‑3 הייתה חלשה באופן משמעותי. הקטנת רמות Munc18‑2 עוד הורידה את Fas ligand על פני השטח, מה שמדגיש את חשיבותו. הכנסת ZNRF1 תקין חזרה לתאים חסרים שיפרה את הצגת Fas ligand, אך גרסה קטליטית מושבתת של ZNRF1 לא עשתה כן, דבר המצביע על כך שפעילות האנזימטית של ZNRF1 נחוצה להפוך את מכונת המיזוג לתפקודית אפילו אם הקומפלקס עצמו עדיין יכול להתגבש.
השלכות על השמדת תאי חיסון מותשים
מכיוון ש‑Fas ligand נועד לעורר מוות בתאים מופעלים, הצוות בדק עד כמה מאקרופאגים יכולים להרוג תאים מטרה. כאשר מאקרופאגים נורמליים הוכנסו יחד עם תאי עזר מופעלים או קו תאים רגיש במיוחד לאיתותי Fas, רבים מהמטרות מתו עם הזמן. לעומת זאת, מאקרופאגים חסרי ZNRF1 חסכו הרבה יותר מהתאים הללו, גם כאשר הם קיבלו גירוי חזק. יכולת ההרג המופחתת תואמת את נתוני העכברים: אם מאקרופאגים אינם מסוגלים לחשוף ביעילות Fas ligand על פני השטח, תאי T פעילות שורדות זמן רב יותר, מעניקות יותר סיוע לתאי B ומזינות טחולים מוגדלים והגברת ייצור הנוגדנים.
מה משמעות הדבר לשליטה על תגובות חיסוניות פורצות
ביחד, הממצאים מגלים את ZNRF1 כמנגנון בטיחות מובנה שמקשר את תנועת הפנימית של חבילות מלאות Fas ligand למיזוגן הסופי עם פני המאקרופאג. כשה‑ZNRF1 פועל כראוי, Fas ligand מגיעה לחוץ התא, מאפשרת למאקרופאגים לסלק תאי T מופעלים ולשמור על תגובות חיסוניות בבדיקה. כש‑ZNRF1 נעדר, שלב ההעברה הזה נכשל, Fas ligand על פני השטח נשאר נמוך והתאים החיסוניים נותרו להתרבות בחופשיות רבה יותר. למרות שעבודת תרגום תרופתית עוד דרושה, המחקר מדגיש ידית מולקולרית ספציפית בעזרתה הגוף מייעל את שלב הכיבוי של תגובות החיסוניות.
ציטוט: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
מילות מפתח: Fas ligand, מאקרופאגים, הומיאוסטאזיס חיסוני, ZNRF1, אפופטוזה של תאי T