Clear Sky Science · sv
ZNRF1-brist stör Fas-ligandets transport och immunbalansen
Varför detta spelar roll för vår immunhälsa
Vårt immunsystem måste balansera noga: det ska angripa hot som mikrober och främmande blodceller, men också stänga ner sig innan svaret spårar ur. Denna studie avslöjar en dold kontrollknapp inne i en vanlig immuncell kallad makrofag som hjälper avgöra om aktiverade immunceller tyst tas bort eller får fortsätta dela sig. Att förstå denna knapp kan i förlängningen hjälpa oss att bättre hantera tillstånd med kronisk inflammation, autoimmunitet eller komplikationer vid transfusion.
En trafiksignal för immun självförstörelse
När immunceller gjort sitt jobb elimineras många av dem genom en inbyggd självdestruktionssignal som involverar ett ytmembranprotein kallat Fas-ligand. Fas-ligand på en cell utlöser död i en annan cell som bär dess matchande receptor, vilket hjälper till att trimma ned överaktiva svar. Majoriteten av forskningen har fokuserat på hur mycket Fas-ligand en cell producerar. Här ställde författarna en annan fråga: hur förflyttas Fas-ligand från interna lagringskompartiment till makrofagers yta vid precis rätt tidpunkt, och vad händer om det leveranssteget går fel?
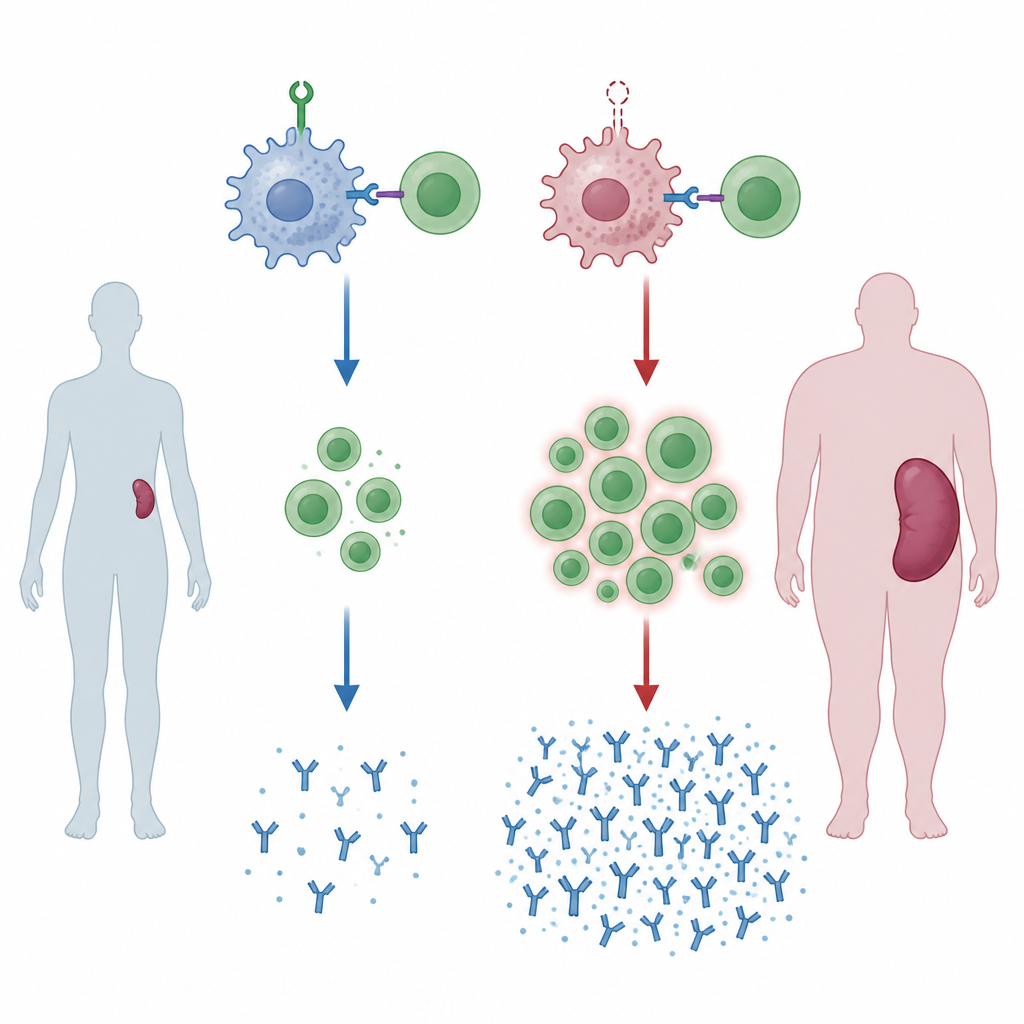
En saknad väktare leder till förstoring av mjälten
Forskargruppen konstruerade möss vars myeloida celler, inklusive makrofager, saknar ett protein kallat ZNRF1. När dessa möss åldrades blev deras mjältar förstorade, ett tecken på kronisk immunaktivering. När djuren utsattes för främmande blod, vilket efterliknar en transfusion från en genetiskt olik donator, blev förändringarna tydligare. Deras mjältar visade utvidgade områden där B‑ och T‑celler interagerar och förökar sig, och förhållandet mellan hjälpar‑T‑celler och cytotoxiska T‑celler försköts uppåt. Dessa möss producerade också högre nivåer av vissa antiklassers antikroppar mot donorblodet, vilket visar att utan ZNRF1 i myeloida celler är immunsystemet inställt på ett för starkt svar.
Ytsignal blockerad medan last hopar sig inne i cellen
För att förstå vad ZNRF1 gör inne i makrofager vände forskarna sig till cellkultur. De stimulerade normala och ZNRF1‑defekta makrofager med bakteriella komponenter eller levande bakterier och mätte Fas-ligand. Överraskande nog tillverkade celler utan ZNRF1 gott om Fas-ligand, ofta mer än normala celler, men de visade det inte på ytan. Under mikroskopet rörde sig interna lagringskompartiment märkta med proteinet LAMP1 fortfarande mot cellytan i båda celltyperna, men i ZNRF1‑defekta celler följde inte Fas-ligandets last med dem till cortex utan fastnade nära centrum. Detta pekar på ett sent haveri i docknings‑ eller fusionssteget snarare än ett problem i produktion eller initial lagring av Fas-ligand.
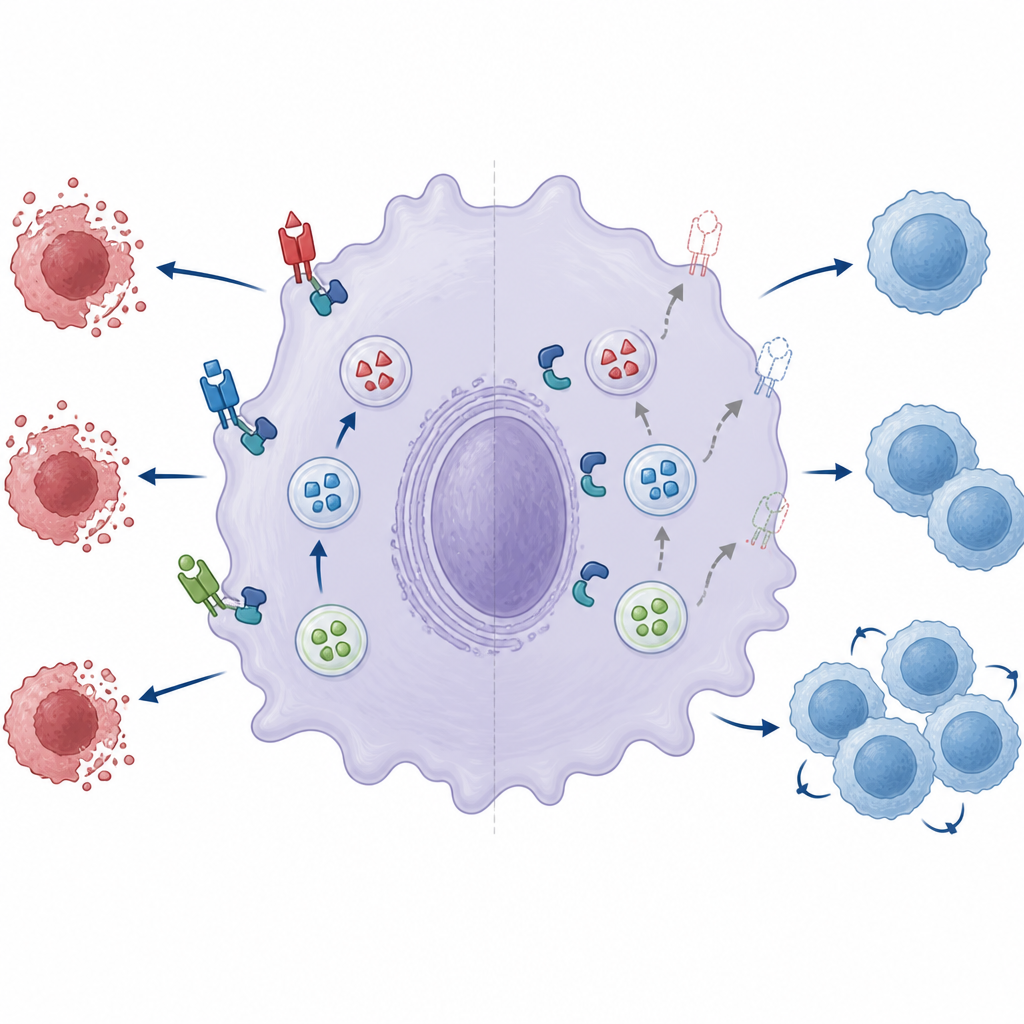
En bruten fusionsmaskin försvagar immunbromsen
Författarna undersökte därefter två nyckelkomponenter i den lilla fusionsmaskin som tillåter lagringsvesiklar att smälta samman med cellens yta: ett par proteiner kallade Munc18‑2 och Syntaxin‑3. I normala makrofager bildar dessa två partners ett komplex som hjälper vesiklar att öppna sig och släppa ut sin last. När ZNRF1 saknades var samarbetet mellan Munc18‑2 och Syntaxin‑3 avsevärt svagare. Att ytterligare minska Munc18‑2‑nivåerna skar ned den ytexponerade Fas‑liganden ytterligare, vilket betonar dess betydelse. Att återinföra normalt ZNRF1 i defekta celler förbättrade Fas‑ligandens visning, men en katalytiskt inaktiv version av ZNRF1 gjorde det inte, vilket tyder på att ZNRF1:s enzymatiska aktivitet behövs för att göra fusionsmaskineriet fullt fungerande även om komplexet i sig fortfarande kan bildas.
Konsekvenser för att döda utarbetade immunceller
Eftersom Fas-ligandets uppgift är att utlösa död i aktiverade celler testade teamet hur väl makrofager kunde döda målceller. När normala makrofager blandades med aktiverade hjälpar‑T‑celler eller med en cellinje som är mycket känslig för Fas‑signaler dog många mål över tid. I kontrast skonar ZNRF1‑defekta makrofager betydligt fler av dessa celler, även när de var starkt stimulerade. Denna minskade dödande förmåga stämmer med mössens data: om makrofager inte effektivt kan exponera Fas-ligand på sin yta överlever aktiverade T‑celler längre, vilket ger mer stöd till B‑celler och driver på förstorade mjältar och ökad antikroppsproduktion.
Vad detta betyder för att kontrollera okontrollerad immunitet
Tillsammans visar resultaten att ZNRF1 är en inbyggd säkerhetsanordning som kopplar den interna förflyttningen av Fas‑ligand‑fyllda paket till deras slutliga fusion med makrofagens yta. När ZNRF1 fungerar normalt når Fas‑ligand cellens utsida, vilket gör det möjligt för makrofager att gallra bort aktiverade T‑celler och hålla immunsvaren i schack. När ZNRF1 saknas misslyckas detta leveranssteg, ytfas‑ligand förblir låg och immunceller får proliferera friare. Mycket arbete återstår innan dessa insikter kan översättas till terapier, men studien lyfter fram ett specifikt molekylärt handtag som kroppen använder för att finjustera avstängningsfasen av immunsvar.
Citering: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Nyckelord: Fas ligand, makrofager, immunhomeostas, ZNRF1, T‑cellsapoptos