Clear Sky Science · it
La carenza di ZNRF1 altera il traffico del ligando Fas e l’equilibrio immunitario
Perché questo è importante per la nostra salute immunitaria
Il nostro sistema immunitario deve percorrere una linea sottile: attaccare le minacce come microbi e cellule ematiche estranee, ma fermarsi prima che la risposta sfugga di mano. Questo studio scopre un interruttore di controllo nascosto all’interno di una cellula immunitaria comune, il macrofago, che aiuta a decidere se le cellule immunitarie attivate vengono rimosse silenziosamente o lasciate proliferare. Comprendere questo interruttore potrebbe in futuro aiutarci a gestire meglio condizioni che coinvolgono infiammazione cronica, autoimmunità o complicazioni da trasfusioni.
Un semaforo per l’autodistruzione immunitaria
Quando le cellule immunitarie hanno svolto il loro compito, molte vengono eliminate tramite un segnale di autodistruzione incorporato che coinvolge una molecola di superficie chiamata ligando Fas. Il ligando Fas su una cellula induce la morte in un’altra cellula che porta il recettore corrispondente, contribuendo a ridurre risposte eccessive. La maggior parte delle ricerche si è concentrata su quanto ligando Fas una cellula produce. Qui, gli autori pongono una domanda diversa: come viene trasferito il ligando Fas dai compartimenti di stoccaggio interni alla superficie esterna dei macrofagi nel momento giusto, e cosa succede se questo passaggio di consegna fallisce?
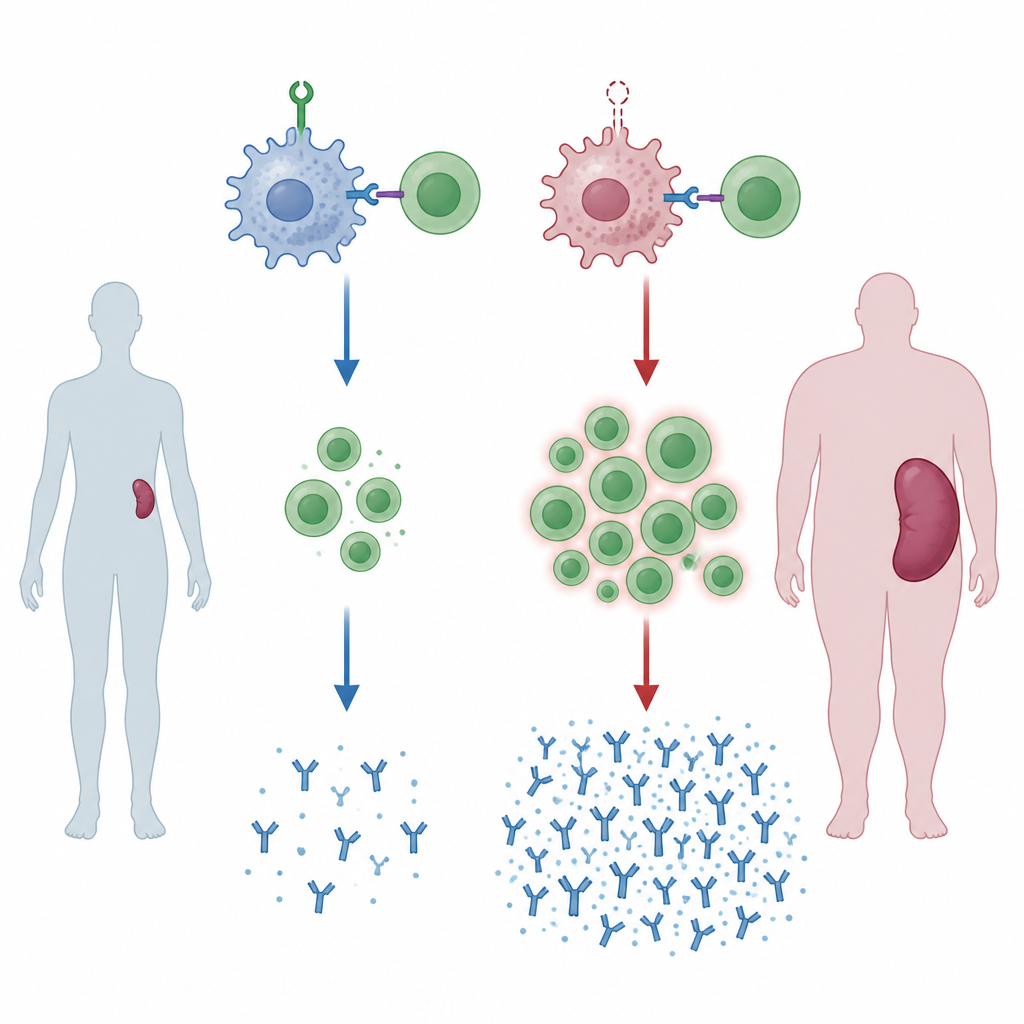
Un guardiano mancante porta a milza ingrossata
Il gruppo ha ingegnerizzato topi i cui elementi mieloidi, compresi i macrofagi, sono privi di una proteina chiamata ZNRF1. Con l’età, in questi topi la milza si è ingrossata, segno di attivazione immunitaria cronica. Quando gli animali sono stati esposti a sangue estraneo, a imitazione di una trasfusione da un donatore geneticamente diverso, i cambiamenti sono diventati più evidenti. Le loro milze hanno mostrato regioni ampliate dove i linfociti B e T interagiscono e si moltiplicano, e il rapporto tra linfociti T helper e linfociti T citotossici è aumentato. Questi topi hanno anche prodotto quantità maggiori di certe classi di anticorpi contro il sangue del donatore, indicando che, in assenza di ZNRF1 nelle cellule mieloidi, il sistema immunitario è predisposto a reagire in modo eccessivo.
Segnale di superficie bloccato mentre il carico si accumula internamente
Per capire cosa fa ZNRF1 all’interno dei macrofagi, i ricercatori si sono rivolti a colture cellulari. Hanno stimolato macrofagi normali e privi di ZNRF1 con componenti batteriche o batteri vivi e hanno misurato il ligando Fas. Sorprendentemente, le cellule senza ZNRF1 producevano molto ligando Fas nel complesso, spesso anche più delle cellule normali, ma non riuscivano a esporlo in superficie. Al microscopio, i compartimenti di stoccaggio interni marcati dalla proteina LAMP1 si muovevano comunque verso il bordo cellulare in entrambi i tipi di cellula, ma nelle cellule carenti di ZNRF1 il carico del ligando Fas non viaggiava con loro fino alla corteccia e rimaneva bloccato vicino al centro. Ciò indica un guasto tardivo nello step di ancoraggio o fusione più che un problema nella produzione o nello stoccaggio iniziale del ligando Fas.
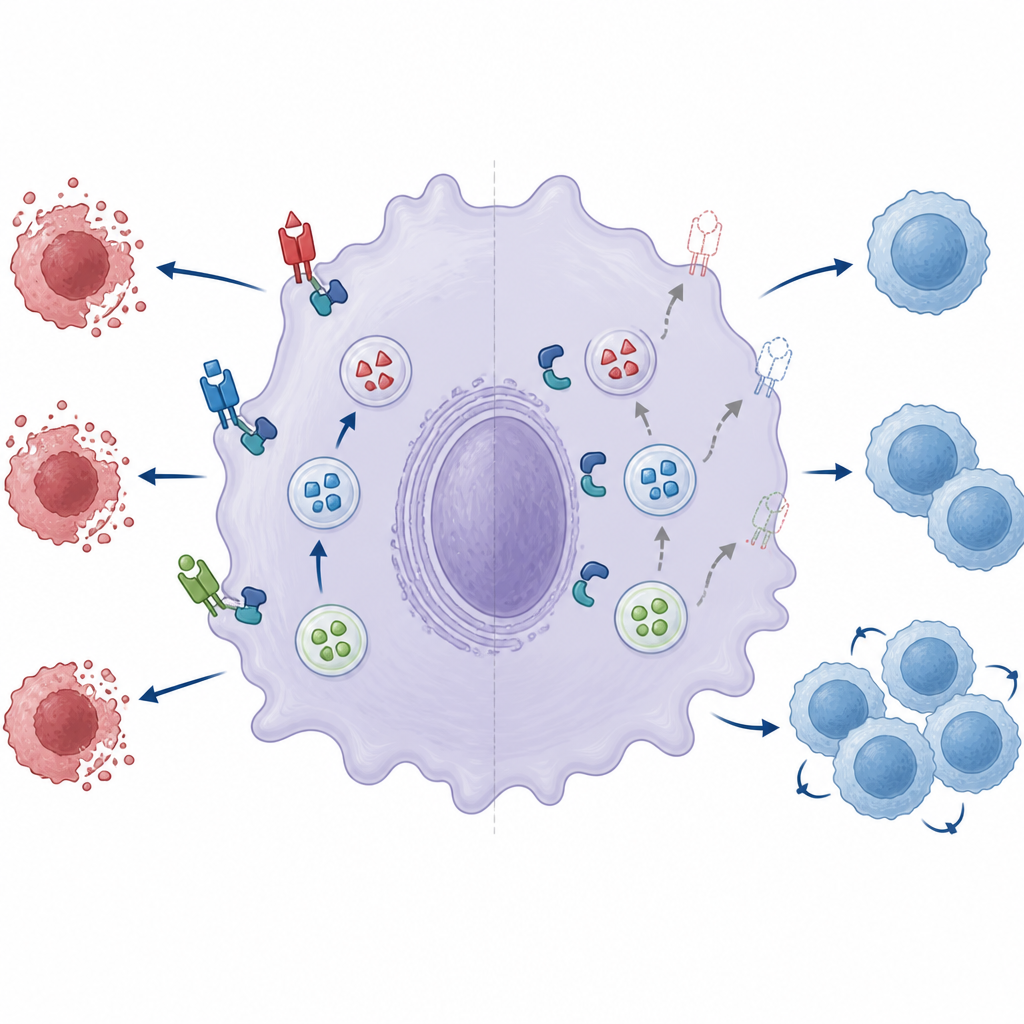
Una macchina di fusione danneggiata indebolisce il freno immunitario
Gli autori hanno quindi esaminato due componenti chiave della piccola macchina di fusione che permette alle vescicole di deposito di fondersi con la superficie cellulare: una coppia di proteine chiamate Munc18‑2 e Syntaxin‑3. Nei macrofagi normali, questi due partner formano un complesso che aiuta le vescicole ad aprirsi e rilasciare il loro carico. Quando ZNRF1 mancava, la partnership tra Munc18‑2 e Syntaxin‑3 risultava notevolmente più debole. Ridurre ulteriormente i livelli di Munc18‑2 riduceva ancora di più il ligando Fas di superficie, sottolineandone l’importanza. Reintrodurre ZNRF1 normale in cellule carenti migliorava l’esposizione del ligando Fas, ma una versione cataliticamente inattiva di ZNRF1 non lo faceva, suggerendo che l’attività enzimatica di ZNRF1 è necessaria per rendere la macchina di fusione pienamente funzionante anche se il complesso può ancora assemblarsi.
Conseguenze per l’eliminazione delle cellule immunitarie esaurite
Poiché il ruolo del ligando Fas è indurre la morte nelle cellule attivate, il gruppo ha testato quanto bene i macrofagi potessero uccidere cellule bersaglio. Quando i macrofagi normali venivano mescolati con linfociti T helper attivati o con una linea cellulare altamente sensibile ai segnali Fas, molte cellule bersaglio morivano nel tempo. Al contrario, i macrofagi privi di ZNRF1 risparmiavano molte più di queste cellule, anche quando erano fortemente stimolate. Questa ridotta capacità di uccidere concorda con i dati nei topi: se i macrofagi non possono esporre efficacemente il ligando Fas in superficie, i linfociti T attivati sopravvivono più a lungo, fornendo più aiuto ai linfociti B e alimentando milza ingrossata e produzione aumentata di anticorpi.
Cosa significa per il controllo di un’immunità sfuggente
Complessivamente, i risultati rivelano ZNRF1 come un dispositivo di sicurezza incorporato che collega il movimento interno dei pacchetti pieni di ligando Fas alla loro fusione finale con la superficie del macrofago. Quando ZNRF1 funziona normalmente, il ligando Fas raggiunge l’esterno della cellula, permettendo ai macrofagi di eliminare i linfociti T attivati e mantenere le reazioni immunitarie sotto controllo. In assenza di ZNRF1, questo passaggio di consegna fallisce, il ligando Fas di superficie resta basso e le cellule immunitarie proliferano più liberamente. Sebbene rimanga molto lavoro prima che queste intuizioni possano tradursi in terapie, lo studio mette in luce una maniglia molecolare specifica con cui l’organismo affina la fase di spegnimento delle risposte immunitarie.
Citazione: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Parole chiave: Ligando Fas, Macrofagi, Omeostasi immunitaria, ZNRF1, Apoptosi dei linfociti T