Clear Sky Science · nl
ZNRF1‑tekort verstoort Fas-ligandverkeer en immuunbalans
Waarom dit belangrijk is voor onze immuungezondheid
Ons immuunsysteem balanceert constant: het moet bedreigingen zoals microben en vreemde bloedcellen bestrijden, maar ook weer stilgezet worden voordat de respons ontspoort. Deze studie brengt een verborgen regelaar aan het licht in een veelvoorkomende immuuncel, de macrofaag, die helpt beslissen of geactiveerde immuuncellen stilletjes worden verwijderd of mogen blijven delen. Inzicht in deze schakel kan uiteindelijk helpen bij het beter beheren van aandoeningen met chronische ontsteking, auto‑immuunziekten of complicaties na transfusie.
Een stoplicht voor immuungerichte zelfvernietiging
Als immuuncellen hun werk hebben gedaan, worden veel van hen uitgeschakeld via een ingebouwd zelfvernietigingssignaal waarbij een oppervlaktemolecuul, Fas‑ligand, betrokken is. Fas‑ligand op de ene cel zorgt ervoor dat een andere cel met de bijpassende receptor afsterft, wat helpt overactieve reacties terug te snoeien. De meeste studies richtten zich op hoeveel Fas‑ligand een cel produceert. De auteurs stelden hier een andere vraag: hoe wordt Fas‑ligand verplaatst van interne opslagcompartimenten naar het celoppervlak van macrofagen op het juiste moment, en wat gebeurt er als die afleveringsstap faalt?
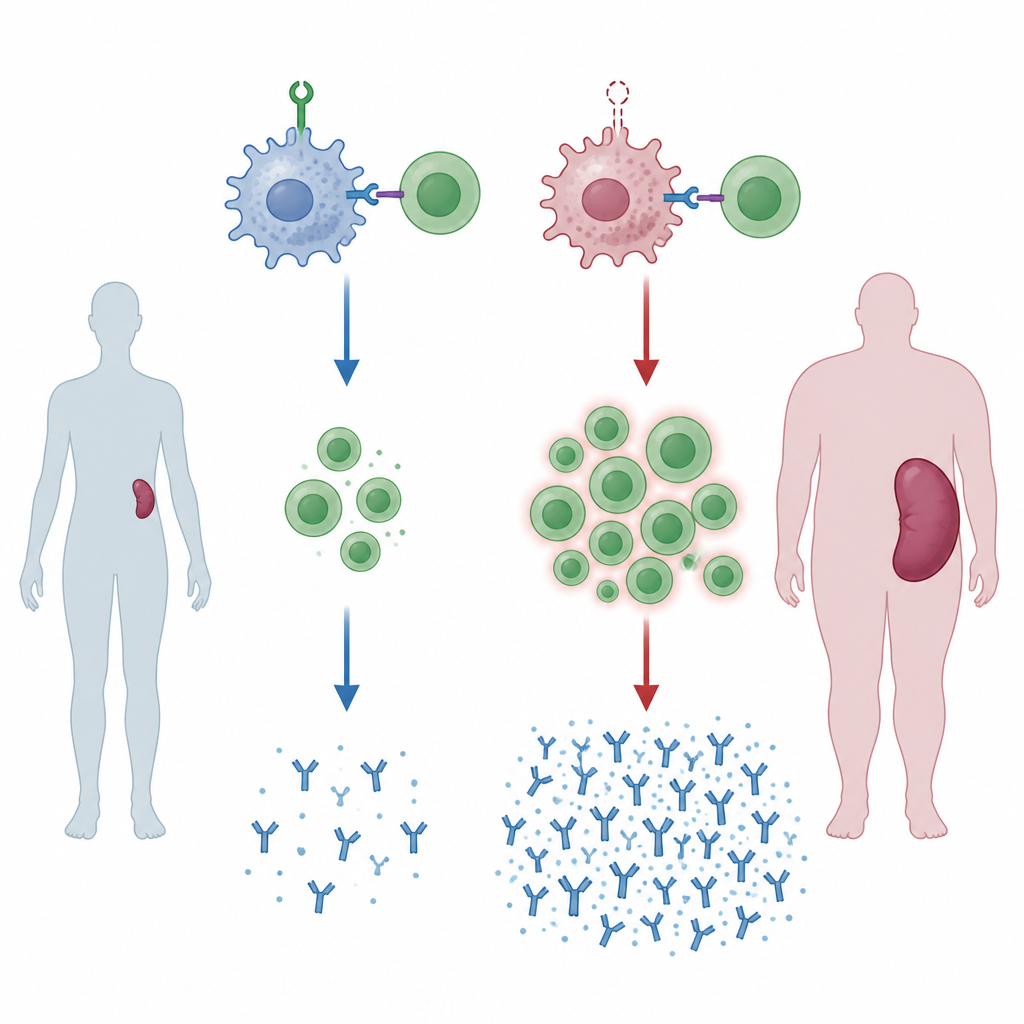
Een ontbrekende bewaker leidt tot vergrote milten
Het team creëerde muizen waarvan myeloïde cellen, waaronder macrofagen, een eiwit genaamd ZNRF1 misten. Naarmate deze muizen ouder werden, werden hun milten vergroot—a een teken van chronische immuunactivatie. Bij blootstelling aan vreemd bloed, als model voor een transfusie van een genetisch verschillende donor, werden de veranderingen nog duidelijker. Hun milten vertoonden uitgebreide gebieden waar B‑ en T‑cellen elkaar ontmoeten en zich delen, en de verhouding helper‑T‑cellen versus killer‑T‑cellen nam toe. Deze muizen produceerden ook meer van bepaalde antiloftklassen tegen het donorbloed, wat aangeeft dat zonder ZNRF1 in myeloïde cellen het immuunsysteem geneigd is te sterk te reageren.
Oppervlaksignaal geblokkeerd terwijl vracht zich ophoopt binnenin
Om te begrijpen wat ZNRF1 in macrofagen doet, onderzochten de onderzoekers cellen in kweek. Ze stimuleerden normale en ZNRF1‑deficiënte macrofagen met bacteriële componenten of levende bacteriën en maten Fas‑ligand. Verrassend genoeg maakten cellen zonder ZNRF1 over het geheel genomen voldoende Fas‑ligand, vaak zelfs meer dan normale cellen, maar ze slaagden er niet in het op hun oppervlak te tonen. Onder de microscoop bewoog het interne opslagcompartiment gemarkeerd door het eiwit LAMP1 in beide celtypes naar de rand, maar in ZNRF1‑deficiënte cellen reisde de Fas‑ligandlading niet met hen mee naar de cortex en bleef dicht bij het centrum vastzitten. Dit wees op een defect in een late docking‑ of fusie stap, eerder dan een probleem bij de productie of initiële opslag van Fas‑ligand.
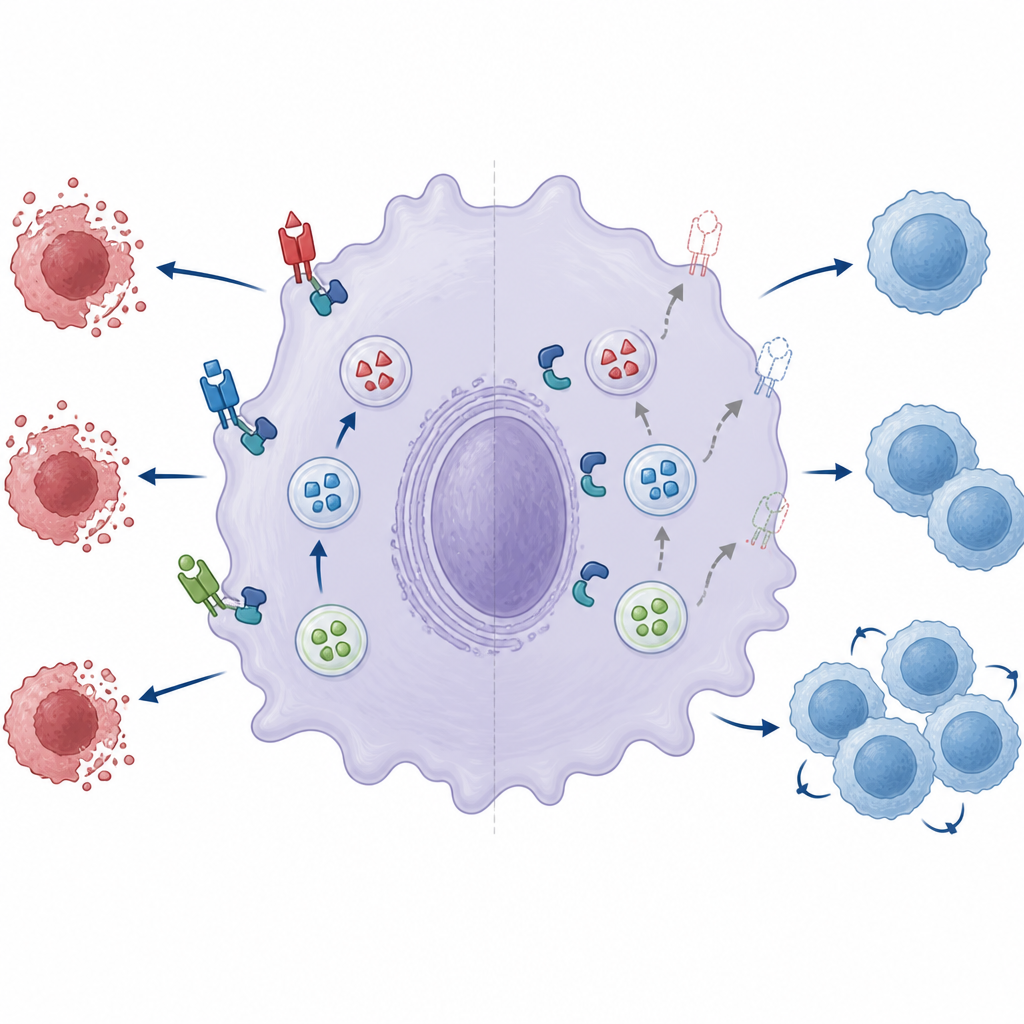
Een kapot fusieapparaat verzwakt de rem op het immuunsysteem
De auteurs onderzochten vervolgens twee sleutelcomponenten van het kleine fusieapparaat dat opslagvesikels met het celoppervlak laat versmelten: een paar eiwitten genaamd Munc18‑2 en Syntaxin‑3. In normale macrofagen vormen deze partners een complex dat vesikels helpt openen en hun vracht vrijgeven. Wanneer ZNRF1 ontbrak, was de samenwerking tussen Munc18‑2 en Syntaxin‑3 duidelijk verzwakt. Het verder verlagen van Munc18‑2‑niveaus verminderde de hoeveelheid Fas‑ligand op het oppervlak nog meer, wat het belang ervan onderstreept. Het opnieuw introduceren van normale ZNRF1 in deficiënte cellen verbeterde de weergave van Fas‑ligand, maar een catalytisch inactieve versie van ZNRF1 deed dat niet, wat suggereert dat de enzymatische activiteit van ZNRF1 nodig is om het fusieapparaat volledig functioneel te maken, ook al kan het complex zelf nog steeds assembleren.
Gevolgen voor het doden van uitgewerkte immuuncellen
Aangezien de taak van Fas‑ligand is geactiveerde cellen te doden, testte het team hoe goed macrofagen doelcellen konden elimineren. Wanneer normale macrofagen werden gemengd met geactiveerde helper‑T‑cellen of met een cellijn die sterk gevoelig is voor Fas‑signalen, stierven veel doelen in de loop van de tijd. In contrast spaarden ZNRF1‑deficiënte macrofagen veel meer van deze cellen, zelfs bij sterke stimulatie. Deze verminderde doding komt overeen met de muizendata: als macrofagen Fas‑ligand niet efficiënt op hun oppervlak kunnen tonen, overleven geactiveerde T‑cellen langer, geven ze meer hulp aan B‑cellen en stimuleren ze vergrote milten en verhoogde antistofproductie.
Wat dit betekent voor het beheersen van uit de hand lopende immuniteit
Gezamenlijk onthullen de bevindingen ZNRF1 als een ingebouwd veiligheidsmechanisme dat de interne verplaatsing van met Fas‑ligand gevulde pakketjes koppelt aan hun uiteindelijke fusie met het macrophageoppervlak. Wanneer ZNRF1 normaal functioneert, bereikt Fas‑ligand het celoppervlak, waardoor macrofagen geactiveerde T‑cellen kunnen verwijderen en immuunreacties onder controle kunnen houden. Wanneer ZNRF1 ontbreekt, faalt deze afleveringsstap, blijft oppervlakkige Fas‑ligand laag en mogen immuuncellen vrijer prolifereren. Hoewel er nog veel werk nodig is voordat deze inzichten naar therapieën vertaald kunnen worden, benadrukt de studie een specifiek moleculair aanknopingspunt waarmee het lichaam de afsluitende fase van immuunreacties fijn afstemt.
Bronvermelding: Lai, TY., Chang, YC., Lin, YS. et al. ZNRF1 deficiency disrupts Fas ligand trafficking and immune balance. Cell Death Dis 17, 422 (2026). https://doi.org/10.1038/s41419-026-08566-8
Trefwoorden: Fas ligand, macrofagen, immuunhomeostase, ZNRF1, T‑cel apoptose