Clear Sky Science · tr
BCR::ABL1 tirozin kinaz inhibitörleri ribozom çarpışmalarını tetikleyerek kronik miyeloid lösemide ZAK-bağımlı ribotoksik stres ve apoptozu aktive eder
Kanser İlaçları Hücrenin Protein Fabrikalarıyla Konuştuğunda
Kronik miyeloid lösemi (KML), sıklıkla BCR::ABL1 adlı kanseri tetikleyen bir enzimi kapatan hedefe yönelik ilaçlarla kontrol altında tutulur. Yine de bazı hastalar agresif bir aşamaya ilerler veya tedaviye direnç geliştirir. Bu çalışma, bu ilaçların kanser hücrelerini nasıl öldürdüğüne dair şaşırtıcı bir rolü araştırıyor: hücrenin kendi protein üreten makineleri olan ribozomlar. Bu makineler sıkışıp çarpıştığında neler olduğunu izleyerek, yazarlar KML hücrelerinin hem büyümesine yardımcı olan hem de ilaç tedavisi altında onları yok etmeye katkıda bulunan bir stres yolunu ortaya koyuyorlar.
Kan Hücresi İçinde Gizli Bir Stres Alarmı
Ribozomlar genellikle iyi zamanlanmış montaj hatları gibi çalışır; genetik mesajları okur ve proteinleri birleştirir. Ancak stres altında ribozomlar duraksayabilir ve birbirine çarpabilir, hücre içinde bir "ribotoksik" alarm sistemini tetikleyebilir. Araştırmacılar, bir stres sinyal zincirinin tepesinde yer alan ZAK adlı bir sensör proteine odaklandı. Yaklaşık 200 KML hastasından alınan örnekleri analiz ederek, ZAK ve ilgili birkaç kalite kontrol faktörünün hastalığı tehlikeli blast fazına ilerlemiş hastalarda çok daha bol olduğunu ve daha yüksek ZAK düzeylerinin daha yüksek oranda olgunlaşmamış kanser kan hücresi ile ilişkilendiğini buldular. Bu, KML kötüleştikçe hücrelerin ZAK-bağlantılı yollara giderek daha fazla dayandığını düşündürdü.
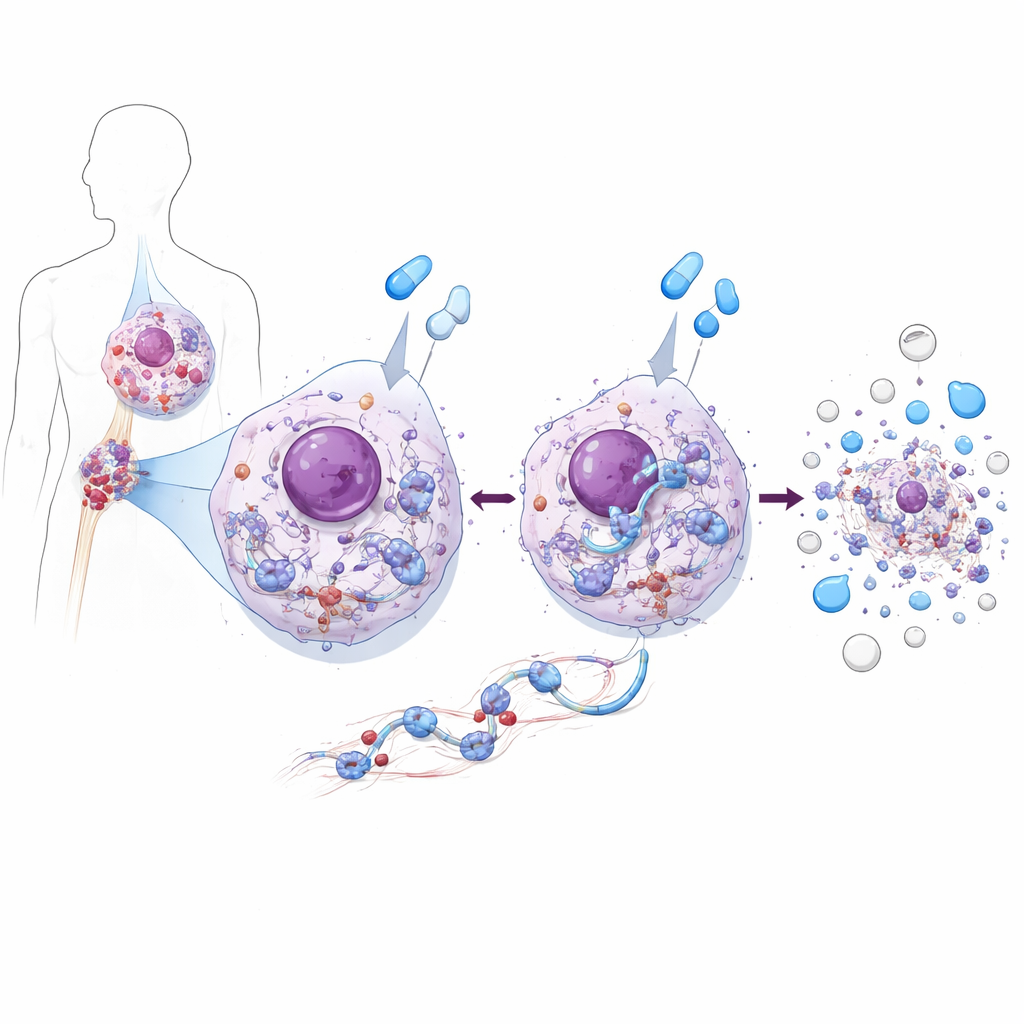
Hem Besleyen Hem de Öldüren Tek Bir Protein
KML hücre hatları ve hastadan türetilmiş hücreleri kullanarak ekip, ZAK'ın çift kişiliğe sahip olduğunu keşfetti. Tedavi edilmeyen KML hücrelerinde ZAK büyümeyi destekliyor. AKT–mTOR yolakları gibi ana bir büyümeyi teşvik eden zincirin aktivitesini artırıyor; bu da protein üretimini ve hücre bölünmesini sürüklüyor. ZAK kaldırıldığında veya engellendiğinde, bu büyüme yolu zayıfladığı için lösemi hücreleri daha yavaş bölündü. Ancak aynı hücreler imatinib veya asciminib gibi BCR::ABL1'i bloke eden ilaçlarla muamele edildiğinde ZAK ters bir rol oynadı: ilaçların etkili hücre ölümünü tetiklemesi için ZAK gerekliydi. ZAK olmadan, bu ilaçlar hedef enzimlerini yine hedef alıyordu ama lösemi hücreleri, doğrudan KML hastalarından alınan örneklerde bile, apoptozise çok daha az yatkındı.
İlaç‑Yavaşlatılmış Protein Üretimi Ribozom Yığılmalarına Nasıl Yol Açar
Yazarlar ardından BCR::ABL1'in kapatılmasının ZAK aktivasyonuna nasıl yol açtığını sordular. BCR::ABL1'in normalde mTOR yolunu açık tuttuğunu ve böylece hızlı protein üretimini sürdürdüğünü buldular. İlaçlar BCR::ABL1'i bloke ettiğinde mTOR aktivitesi düştü. Bu değişiklik, ribozomların RNA şablonları boyunca hareketini yavaşlatan aşağı akış anahtarlarını tetikledi. Yeni yapılan proteinlerin ölçümleri çevirinin yavaşladığını doğruladı ve özel gradyan deneyleri ilaçla muamele edilmiş hücrelerde ribozomların sıkışıp çarpışmaya meyilli kümeler oluşturduğunu gösterdi. Bu tıkanmış ribozomlar nükleazlarla parçalanmaya karşı alışılmadık derecede dirençliydi ve EDF1 ve ZAK gibi çarpışma sensörleriyle yüklüydü; bu, hücrenin protein fabrikalarının mekanik stres altında olduğuna dair açık işaretlerdi.
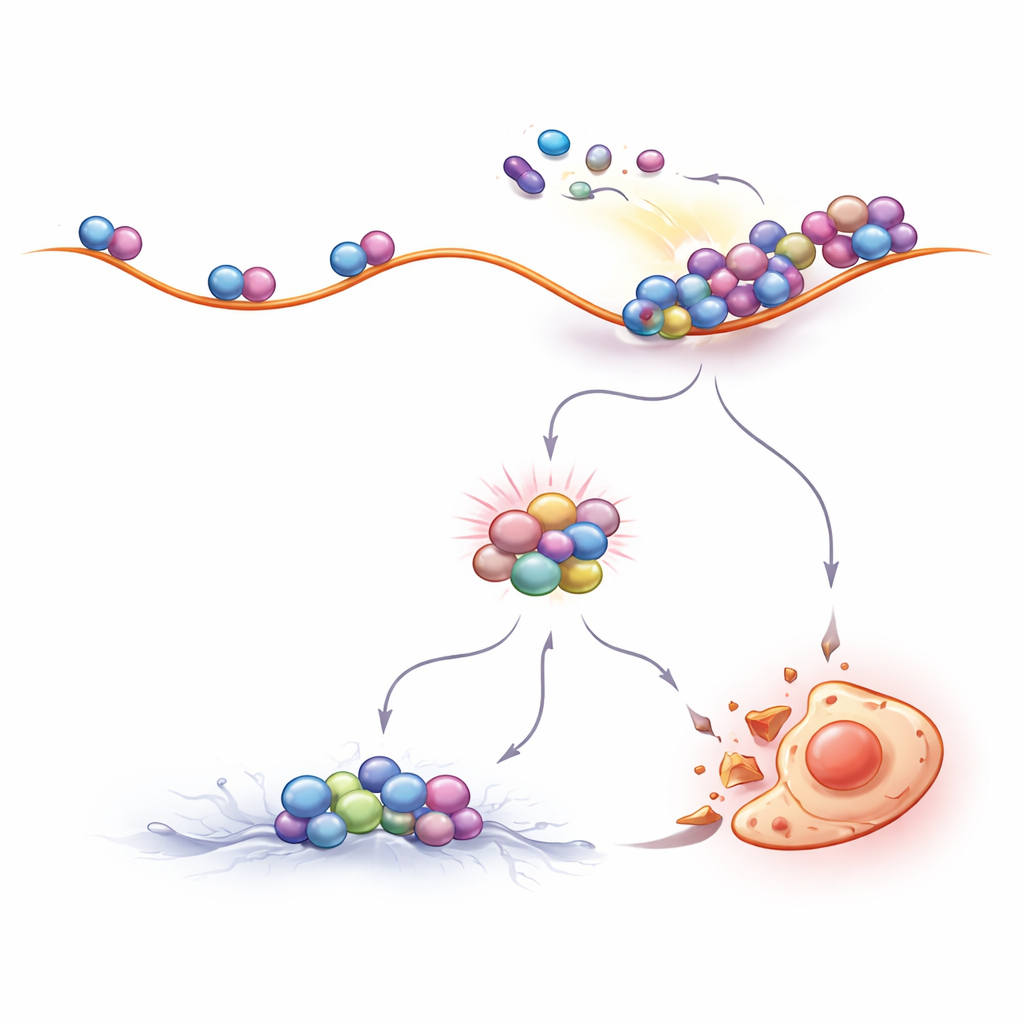
Tedaviyi Daha Etkili Kılmak İçin Ribozom Trafiğini Ayarlamak
Eğer ribozom çarpışmaları KML ilaçlarının çalışma mekanizmasının merkezindeyse, o zaman ribozom trafiğini kasten değiştirmek ilaç duyarlılığını da değiştirmeliydi. Araştırmacıların gözlemlediği tam olarak buydu. Yeni protein zincirlerine başlayan ribozom sayısını azaltan bileşikler çarpışma olasılığını düşürdü ve KML hücrelerini imatinib kaynaklı ölümden korudu. Buna karşın ribozomların RNA boyunca adım adım hareketini hafifçe yavaşlatan veya hücre içinde aynı yavaşlatma mekanizmasını aktive eden ilaçlar çarpışmaları artırdı ve BCR::ABL1 inhibitörleriyle KML hücrelerinin öldürülmesini büyük oranda güçlendirdi. Önemli olarak, bu etki yalnızca laboratuvar hücre hatlarında değil, aynı zamanda hastalardan alınan primer hücrelerde de görüldü; bu da etkinin klinik açıdan önem taşıyabileceğini vurguluyor.
Bu Hastalar ve Gelecek Tedaviler İçin Ne Anlama Geliyor
Uzman olmayan biri için ana mesaj şudur: KML ilaçları sadece hatalı bir enzimi kapatmaktan daha fazlasını yapar; aynı zamanda kanser hücresinin protein montaj hatlarını tıkar ve ribozomların çarpışmasına neden olur. Bu çarpışmalar ZAK'ı uyandırır; ZAK, büyümeyi destekleyen bir faktörden hücre intiharıyla sonuçlanan bir stres yolunu tetikleyen bir cellata dönüşür. Ribozom hızını—doğru şekilde hızlandırıp yavaşlatarak—ince ayarlamayı öğrenerek, doktorlar mevcut KML ilaçlarının etkinliğini artırabilir veya direnci aşabilir. Çalışma, sadece üretilen protein miktarının değil, ribozomların fiziksel davranışının da lösemide ve potansiyel olarak diğer kanserlerde güçlü ve ilaçlanabilir bir zaaf olduğunu öne sürüyor.
Atıf: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Anahtar kelimeler: kronik miyeloid lösemi, ribozom çarpışmaları, ZAK stres kinazı, BCR-ABL inhibitörleri, protein sentezi