Clear Sky Science · ru
Ингибиторы тирозинкиназы BCR::ABL1 вызывают столкновения рибосом для активации ZAK‑зависимого риботоксического стресса и апоптоза при хроническом миелоидном лейкозе
Когда противораковые лекарства говорят с белковых фабрик клетки
Хронический миелоидный лейкоз (ХМЛ) часто контролируется таргетными препаратами, которые выключают запускающий опухоль фермент BCR::ABL1. Тем не менее у некоторых пациентов болезнь прогрессирует в агрессивную стадию или развивается резистентность к лечению. В этом исследовании изучается неожиданный участник того, как эти препараты убивают раковые клетки: собственные белковые машины клетки — рибосомы. Наблюдая, что происходит, когда эти машины застревают и сталкиваются, авторы обнаружили стрессовый путь, который одновременно поддерживает рост клеток ХМЛ и при лечении препаратами способствует их разрушению.
Скрытый сигнал тревоги внутри клеток крови при раке
Рибосомы обычно работают как хорошо слаженные конвейеры: читают генетические сообщения и собирают белки. Однако при стрессе рибосомы могут останавливаться и сталкиваться друг с другом, вызывая «риботоксическую» систему тревоги внутри клетки. Исследователи сосредоточились на сенсорном белке ZAK, который стоит во главе цепочки сигнального ответа на стресс. Проанализировав образцы почти 200 пациентов с ХМЛ, они обнаружили, что ZAK и несколько связанных с ним факторов контроля качества значительно более выражены у пациентов, у которых болезнь перешла в опасную бластную фазу, и что повышенные уровни ZAK коррелировали с большей долей незрелых раковых клеток крови. Это указывало на то, что по мере ухудшения ХМЛ клетки сильнее зависят от путей, связанных с ZAK.
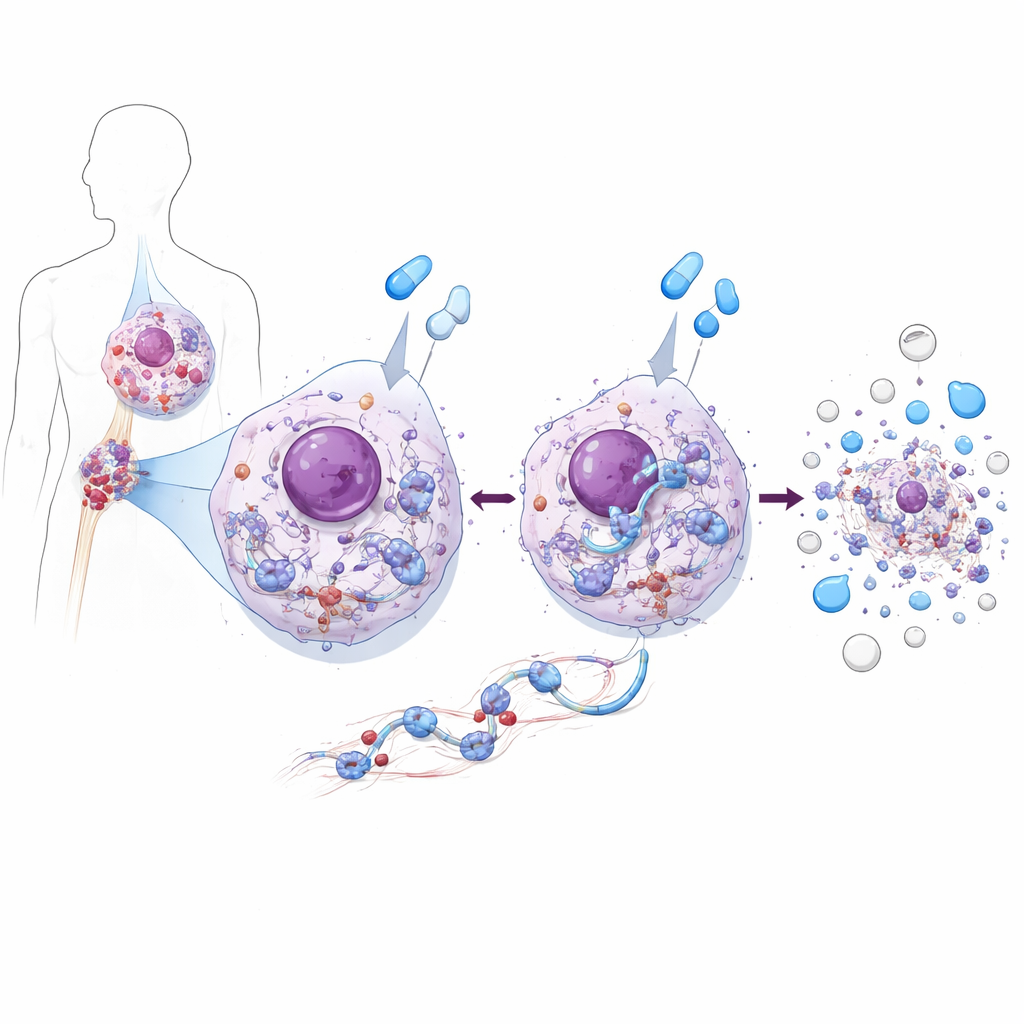
Один белок, который и питает, и убивает клетки лейкемии
Используя клеточные линии ХМЛ и клетки, полученные от пациентов, команда обнаружила двойственность роли ZAK. В нелеченых клетках ХМЛ ZAK поддерживает рост. Он усиливает активность важного ростоподдерживающего каскада AKT–mTOR, который, в свою очередь, стимулирует синтез белка и деление клеток. При удалении или блокаде ZAK клетки лейкемии делились медленнее из‑за ослабления этого ростового пути. Но при лечении тех же клеток ингибиторами BCR::ABL1, такими как иматиниб или асциминиб, ZAK проявлял противоположную роль: он был необходим, чтобы препараты эффективно вызывали гибель клеток. Без ZAK эти препараты по‑прежнему поразили целевой фермент, но вероятность апоптоза в клетках лейкемии существенно снижалась, даже в образцах, взятых непосредственно у пациентов с ХМЛ.
Как замедление синтеза белка лекарством вызывает скопления рибосом
Авторы затем спросили, как выключение BCR::ABL1 приводит к активации ZAK. Они выяснили, что BCR::ABL1 обычно поддерживает активность пути mTOR, который обеспечивает быстрый синтез белка. При блокаде BCR::ABL1 активность mTOR падала. Это изменение переключало вниз каскады, замедлявшие продвижение рибосом вдоль молекул РНК. Измерения вновь синтезируемых белков подтвердили замедление трансляции, а специальные градиентные эксперименты показали, что в обработанных лекарством клетках рибосомы стали тесно расположены и образовывали кластеры, склонные к столкновениям. Эти застрявшие рибосомы были необычно устойчивы к расщеплению нуклеазами и были насыщены датчиками столкновений, такими как EDF1 и ZAK — явные признаки механического стресса в белковых фабриках клетки.
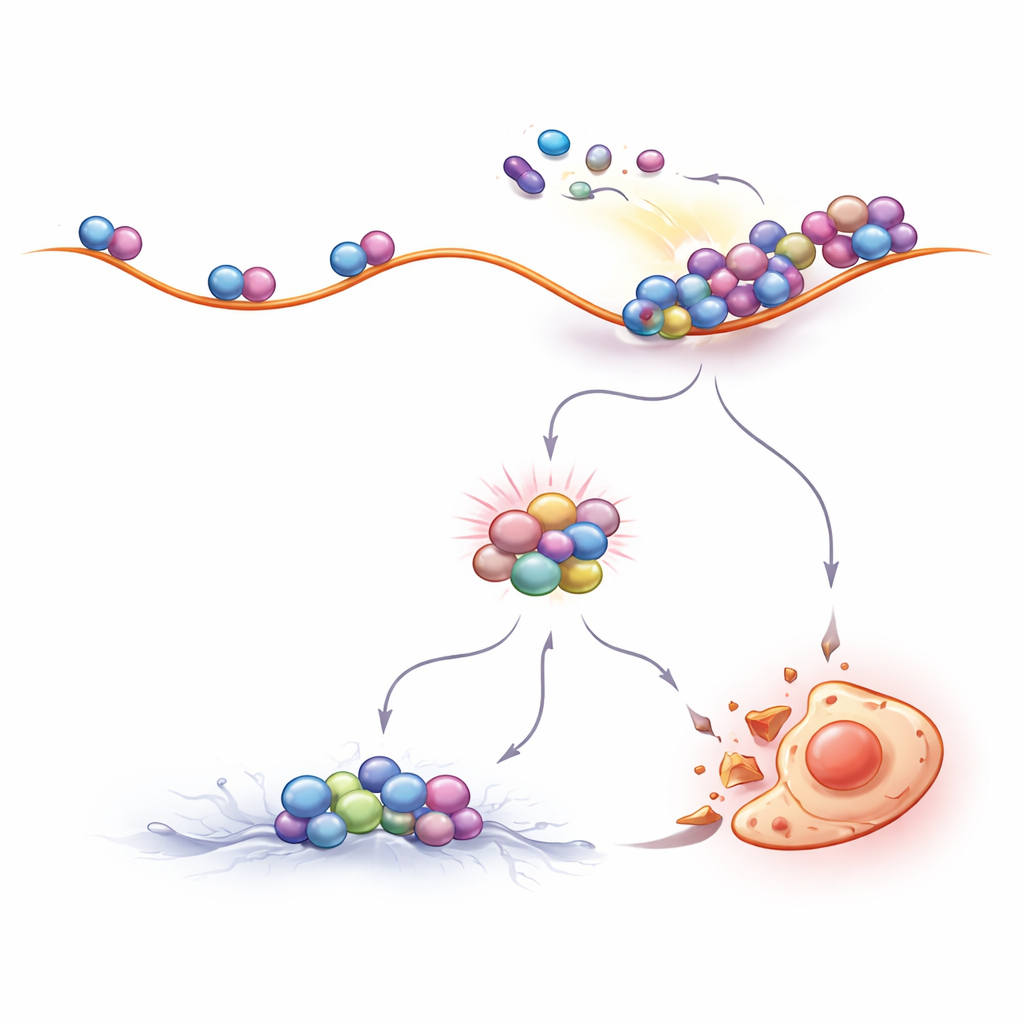
Регулировка трафика рибосом, чтобы усилить эффект лечения
Если столкновения рибосом имеют решающее значение для действия препаратов при ХМЛ, то целенаправленное изменение «трафика» рибосом должно менять чувствительность к лекарствам. Именно это и увидели исследователи. Соединения, которые уменьшали число рибосом, начинающих новые белковые цепи, снижали вероятность столкновений и защищали клетки ХМЛ от гибели, вызванной иматинибом. Напротив, препараты, которые слегка замедляли поэтапное продвижение рибосом вдоль РНК, либо активировали тот же замедляющий механизм внутри клетки, усиливали столкновения и значительно повышали убивающий эффект ингибиторов BCR::ABL1. Важно, что этот эффект наблюдался не только в лабораторных клеточных линиях, но и в первичных клетках, взятых у пациентов, что подчеркивает его потенциальную клиническую значимость.
Что это значит для пациентов и будущих терапий
Для неспециалиста главный вывод таков: препараты от ХМЛ делают не только одно — выключают сбойный фермент; они также заклинивают конвейеры сборки белков в раковых клетках, вызывая столкновения рибосом. Эти столкновения пробуждают ZAK, который переключается от помощника роста в роль «палача», активируя стрессовый путь, завершающийся самоубийством клетки. Поняв, как тонко настраивать скорость рибосом — ускоряя или замедляя её в нужном направлении — врачи в будущем смогут повысить эффективность существующих препаратов от ХМЛ или преодолеть резистентность. Исследование указывает, что физическое поведение рибосом, а не только объём синтезируемого ими белка, представляет собой мощную и поддающуюся медикаментозному вмешательству уязвимость при лейкемии и, возможно, при других видах рака.
Цитирование: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Ключевые слова: хронический миелоидный лейкоз, столкновения рибосом, киназа стресса ZAK, ингибиторы BCR‑ABL, синтез белка