Clear Sky Science · es
Los inhibidores de la tirosina quinasa BCR::ABL1 inducen colisiones ribosómicas para activar estrés ribotóxico dependiente de ZAK y apoptosis en la leucemia mieloide crónica
Cuando los fármacos contra el cáncer hablan con las fábricas de proteínas de la célula
La leucemia mieloide crónica (LMC) suele controlarse con fármacos dirigidos que inactivan una enzima oncogénica denominada BCR::ABL1. Sin embargo, algunos pacientes progresan a una fase agresiva o desarrollan resistencia al tratamiento. Este estudio explora un actor sorprendente en la manera en que estos fármacos matan a las células cancerosas: las propias máquinas de producir proteínas de la célula, los ribosomas. Al observar qué ocurre cuando estas máquinas se atascan y colisionan, los autores identifican una vía de estrés que tanto ayuda al crecimiento de las células de LMC como, bajo tratamiento farmacológico, contribuye a su destrucción.
Una alarma de estrés oculta dentro de las células de la leucemia
Los ribosomas suelen funcionar como líneas de ensamblaje bien sincronizadas, leyendo mensajes genéticos y ensamblando proteínas. Bajo estrés, sin embargo, los ribosomas pueden detenerse y chocar entre sí, desencadenando un sistema de alarma “ribotóxico” dentro de la célula. Los investigadores se centraron en una proteína sensor llamada ZAK que se sitúa en la parte superior de una cadena de señalización del estrés. Al analizar muestras de casi 200 pacientes con LMC, hallaron que ZAK y varios factores relacionados con el control de calidad eran mucho más abundantes en pacientes cuya enfermedad había avanzado a la peligrosa fase blastífica, y que niveles más altos de ZAK se correlacionaban con una mayor proporción de células sanguíneas cancerosas inmaduras. Esto sugiere que, a medida que la LMC empeora, sus células dependen en gran medida de las vías vinculadas a ZAK.
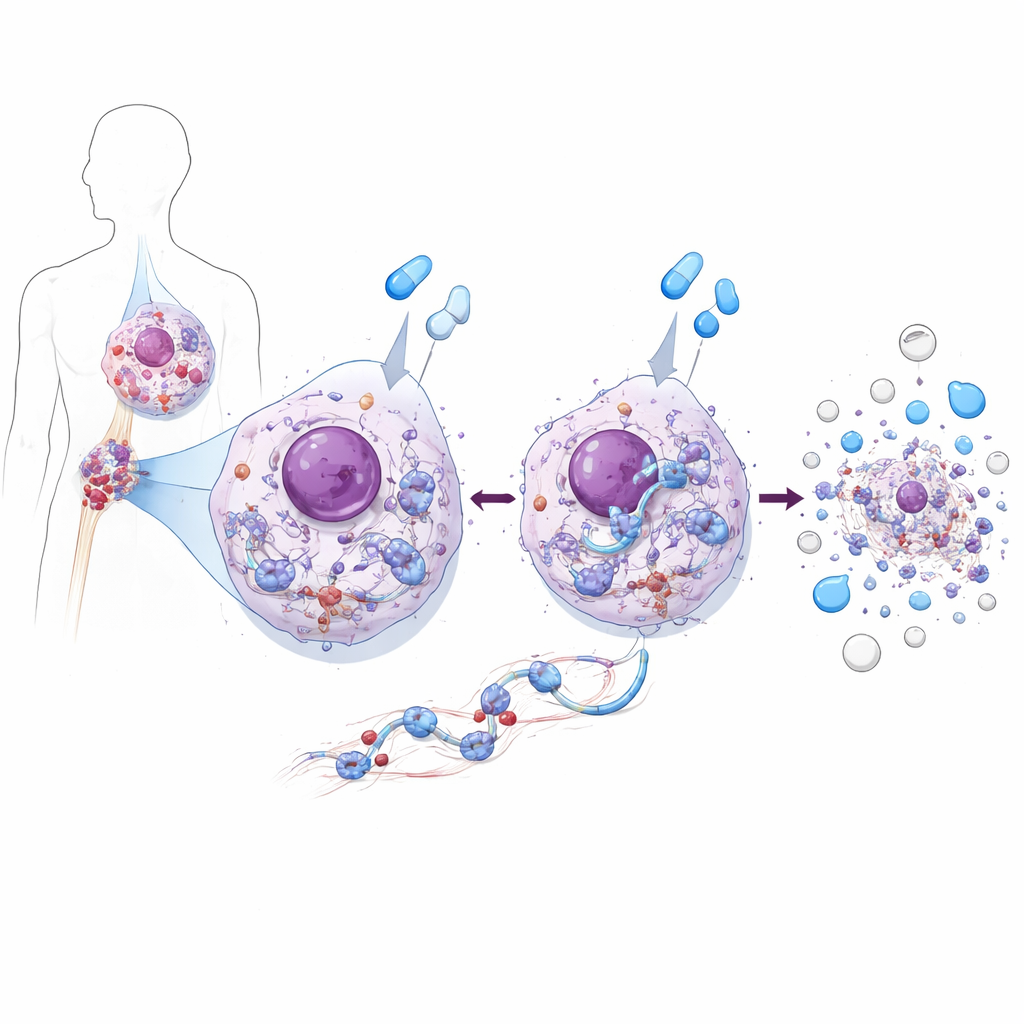
Una proteína que a la vez alimenta y mata a las células leucémicas
Usando líneas celulares de LMC y células derivadas de pacientes, el equipo descubrió que ZAK tiene una doble personalidad. En células de LMC no tratadas, ZAK favorece el crecimiento. Potencia la actividad de una vía principal promotora del crecimiento, la vía AKT–mTOR, que a su vez impulsa la producción de proteínas y la división celular. Cuando ZAK se eliminó o inhibió, las células leucémicas se dividieron más lentamente porque esta vía de crecimiento se debilitó. Pero cuando las mismas células se trataron con fármacos que bloquean BCR::ABL1, como imatinib o asciminib, ZAK desempeñó el papel opuesto: fue necesario para que los fármacos desencadenaran una apoptosis eficaz. Sin ZAK, estos fármacos seguían golpeando su enzima objetivo, pero las células leucémicas eran mucho menos propensas a entrar en apoptosis, incluso en muestras tomadas directamente de pacientes con LMC.
Cómo la ralentización de la traducción por fármacos provoca acumulaciones de ribosomas
Los autores se preguntaron entonces cómo la inhibición de BCR::ABL1 conduce a la activación de ZAK. Descubrieron que BCR::ABL1 mantiene normalmente la vía mTOR activada, lo que sostiene una producción rápida de proteínas. Cuando los fármacos bloquearon BCR::ABL1, la actividad de mTOR cayó. Este cambio activó interruptores aguas abajo que reducen la velocidad de los ribosomas a lo largo de sus moldes de ARN. Mediciones de proteínas recién sintetizadas confirmaron que la traducción se ralentizó, y experimentos especializados de gradiente mostraron que los ribosomas en células tratadas con fármaco se volvieron más numerosos y formaron cúmulos propensos a colisiones. Estos ribosomas atascados fueron inusualmente resistentes a la degradación por nucleasas y estaban cargados con sensores de colisión como EDF1 y ZAK, señales claras de que las fábricas de proteínas de la célula estaban sometidas a estrés mecánico.
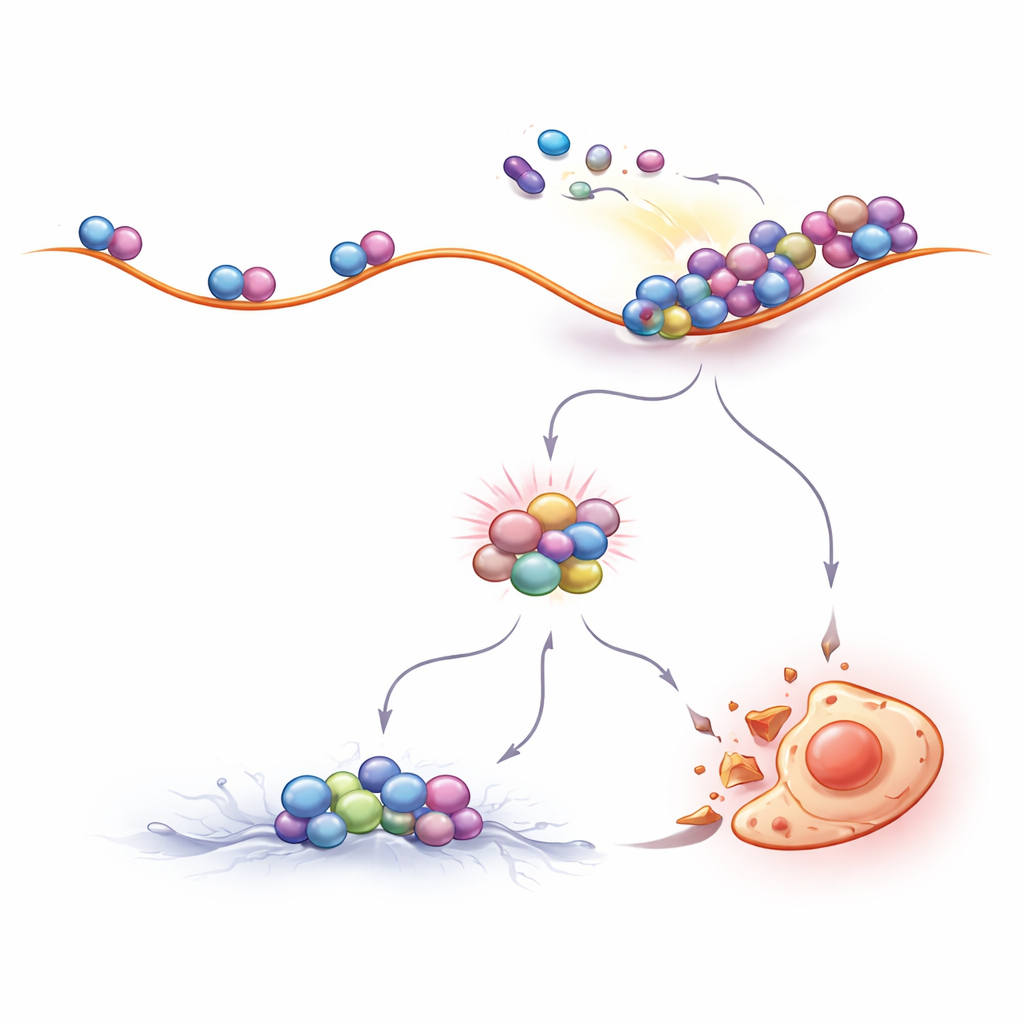
Ajustar el tráfico ribosómico para mejorar el tratamiento
Si las colisiones ribosómicas son centrales para la acción de los fármacos contra la LMC, entonces cambiar deliberadamente el tráfico ribosómico debería alterar la sensibilidad al fármaco. Esto es exactamente lo que observaron los investigadores. Compuestos que redujeron el número de ribosomas que inician nuevas cadenas proteicas hicieron que las colisiones fueran menos probables y protegieron a las células de LMC de la muerte inducida por imatinib. En contraste, fármacos que ralentizaron ligeramente el movimiento paso a paso de los ribosomas a lo largo del ARN, o que activaron el mismo mecanismo de ralentización dentro de la célula, aumentaron las colisiones y potenciaron en gran medida la eliminación de células de LMC por los inhibidores de BCR::ABL1. Es importante que este efecto se observó no solo en líneas celulares de laboratorio sino también en células primarias tomadas de pacientes, lo que subraya su potencial relevancia clínica.
Qué significa esto para los pacientes y futuras terapias
Para un público no especializado, el mensaje clave es que los fármacos contra la LMC hacen más que apagar una enzima rebelde; también bloquean las líneas de ensamblaje proteico de la célula cancerosa, provocando colisiones ribosómicas. Estas colisiones despiertan a ZAK, que cambia de ser un ayudante del crecimiento a actuar como verdugo al activar una vía de estrés que culmina en el suicidio celular. Al aprender a afinar la velocidad de los ribosomas —acelerándola o ralentizándola de manera adecuada— los médicos podrían en el futuro aumentar la eficacia de los fármacos existentes contra la LMC o superar la resistencia. El estudio sugiere que el comportamiento físico de los ribosomas, no solo la cantidad de proteína que sintetizan, es una vulnerabilidad potente y farmacológicamente accesible en la leucemia y, potencialmente, en otros cánceres.
Cita: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Palabras clave: leucemia mieloide crónica, colisiones ribosómicas, quinasa de estrés ZAK, inhibidores de BCR-ABL, síntesis de proteínas