Clear Sky Science · pl
Inhibitory kinazy tyrozynowej BCR::ABL1 wywołują kolizje rybosomów, aktywując ZAK‑zależny stres ribotoksyny i apoptozę w przewlekłej białaczce szpikowej
Kiedy leki przeciwnowotworowe rozmawiają z komórkowymi fabrykami białek
Przewlekła białaczka szpikowa (CML) często jest kontrolowana przez leki celowane, które wyłączają onkogenną enzymatyczną aktywność BCR::ABL1. Mimo to u niektórych pacjentów choroba przechodzi w agresywny etap albo rozwija się oporność na terapię. W tej pracy badacze odkrywają zaskakujący element odpowiedzi na leczenie: własne maszyny komórkowe produkujące białka — rybosomy. Obserwując, co się dzieje, gdy te „linie montażowe” zacinają się i zderzają, autorzy odsłaniają szlak stresowy, który zarówno wspiera wzrost komórek CML, jak i — pod wpływem leków — przyczynia się do ich eliminacji.
Ukryty alarm stresowy w komórkach nowotworu krwi
Rybosomy zazwyczaj działają jak dobrze zsynchronizowane taśmy produkcyjne, odczytując informacje genetyczne i łącząc aminokwasy w białka. Pod wpływem stresu mogą jednak zastać się i zderzać, uruchamiając wewnątrzkomórkowy alarm „ribotoksyczny”. Badacze skupili się na białku‑sensorze ZAK, które stoi na szczycie łańcucha sygnalizacyjnego stresu. Analiza próbek od prawie 200 pacjentów z CML wykazała, że ZAK i kilka powiązanych czynników kontroli jakości występowały w znacznie większej ilości u pacjentów, u których choroba przeszła w niebezpieczną fazę blastyczną, a wyższy poziom ZAK korelował z większym odsetkiem niedojrzałych komórek nowotworowych. Sugeruje to, że wraz z pogarszaniem się CML komórki silniej polegają na ścieżkach związanych z ZAK.
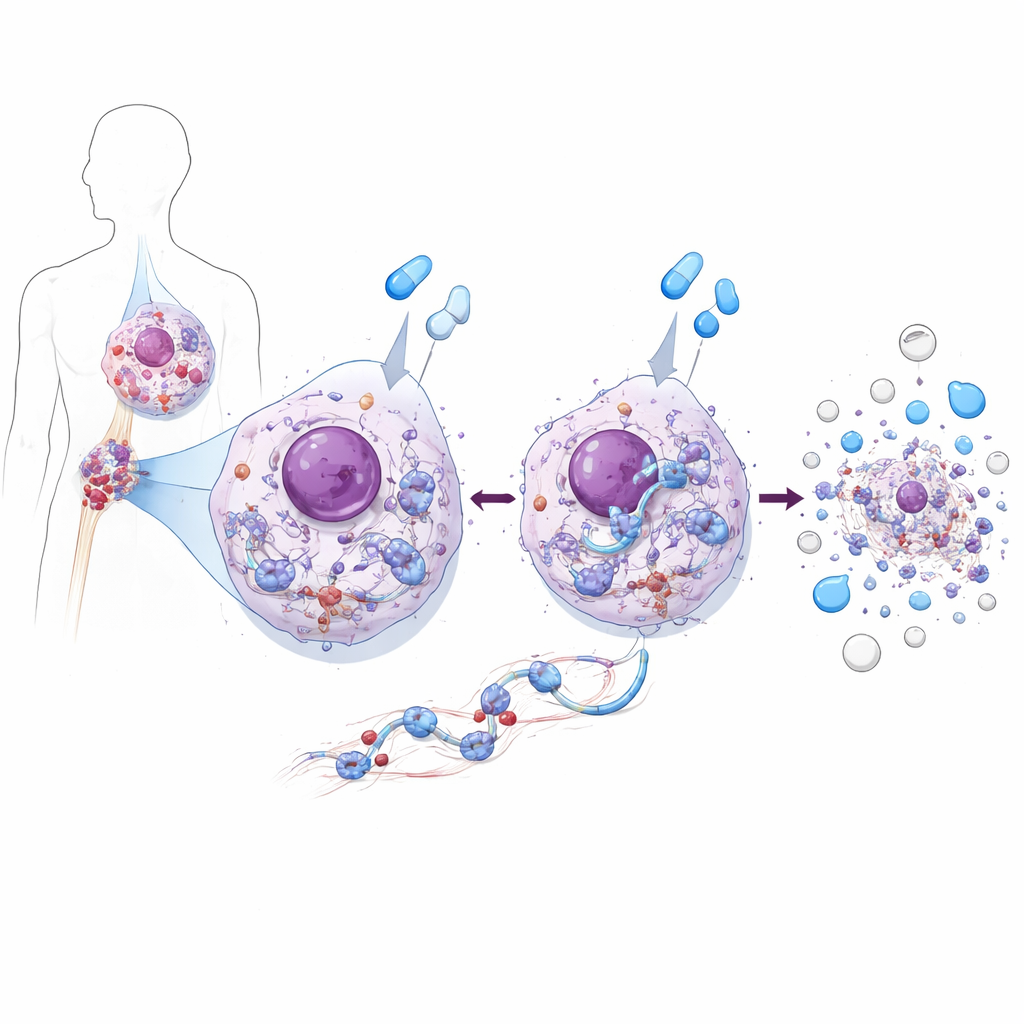
Jedno białko, które zarazem karmi i zabija komórki białaczki
Na modelach linii komórkowych CML i komórkach pobranych od pacjentów zespół odkrył, że ZAK ma podwójną naturę. W nieleczonych komórkach CML ZAK wspiera wzrost — pobudza aktywność głównego szlaku promującego wzrost, AKT–mTOR, co z kolei napędza syntezę białek i podziały komórkowe. Usunięcie lub zablokowanie ZAK spowalniało podziały leukemicznych komórek, ponieważ osłabiał się ten szlak wzrostowy. Jednak po zastosowaniu leków blokujących BCR::ABL1, takich jak imatinib czy asciminib, ZAK odgrywał odwrotną rolę: był niezbędny do skutecznego wywołania śmierci komórkowej przez te leki. Bez ZAK leki nadal trafiały swój enzymowy cel, ale komórki białaczkowe dużo rzadziej przechodziły apoptozę, także w próbkach pobranych bezpośrednio od pacjentów z CML.
Jak spowolniona przez leki produkcja białek powoduje zator rybosomów
Autorzy pytali dalej, jak wyłączenie BCR::ABL1 prowadzi do aktywacji ZAK. Odkryli, że BCR::ABL1 utrzymuje normalnie aktywny szlak mTOR, który zapewnia szybkie tempo syntezy białek. Zablokowanie BCR::ABL1 przez leki obniżało aktywność mTOR. Ta zmiana przełączała końcowe regulatory, które zwalniały ruch rybosomów wzdłuż matryc RNA. Pomiar nowo syntetyzowanych białek potwierdził spowolnienie translacji, a specjalistyczne eksperymenty gradientowe wykazały, że w komórkach traktowanych lekami rybosomy gromadziły się i tworzyły skupiska podatne na kolizje. Te zablokowane rybosomy były wyjątkowo odporne na rozkład przez nukleazy i były obciążone sensorami kolizji, takimi jak EDF1 i ZAK — wyraźne sygnały mechanicznego stresu w „fabrykach” białek komórki.
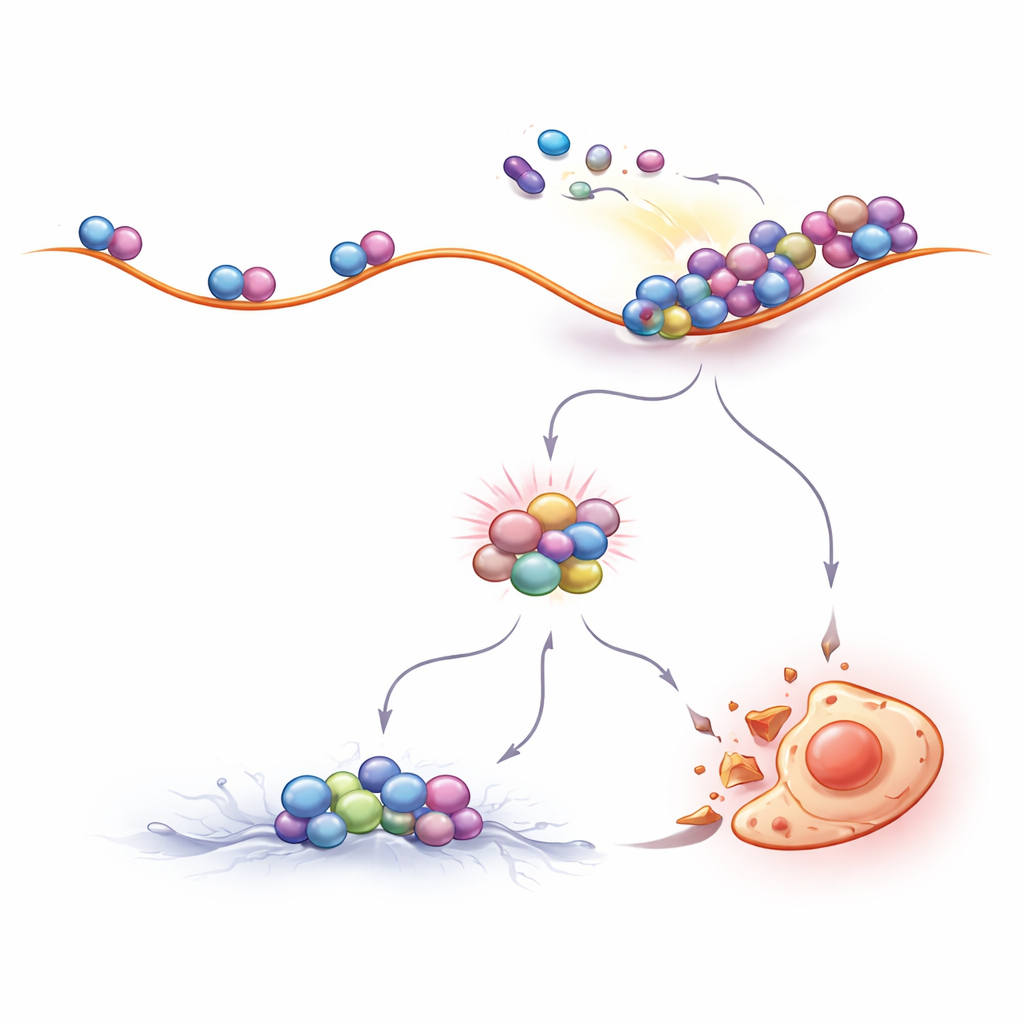
Dostrajanie ruchu rybosomów, żeby polepszyć terapię
Jeśli kolizje rybosomów są kluczowe dla działania leków przeciw CML, to celowe zmiany w ruchu rybosomów powinny zmieniać wrażliwość na terapię. I właśnie to zaobserwowali badacze. Związki zmniejszające liczbę rybosomów inicjujących nowe łańcuchy białkowe redukowały prawdopodobieństwo kolizji i chroniły komórki CML przed śmiercią wywołaną imatinibem. W przeciwieństwie do tego, leki, które nieznacznie spowalniały krokowy ruch rybosomów wzdłuż RNA lub aktywowały ten sam mechanizm hamujący w komórce, zwiększały kolizje i znacząco nasilały eliminację komórek CML przez inhibitory BCR::ABL1. Co ważne, efekt ten obserwowano nie tylko w liniach komórkowych w laboratorium, ale także w komórkach pierwotnych pobranych od pacjentów, co podkreśla jego potencjalne znaczenie kliniczne.
Co to oznacza dla pacjentów i przyszłych terapii
Dla nietechnicznego odbiorcy kluczowy wniosek jest taki, że leki na CML robią więcej niż tylko wyłączają wadliwy enzym — zakłócają też taśmy montażowe białek w komórce, powodując kolizje rybosomów. Te zderzenia aktywują ZAK, który przełącza się z roli pomocnika wzrostu w rolę wykonawcy, uruchamiając szlak stresowy kończący się samobójczą śmiercią komórki. Nauka, jak precyzyjnie dostroić prędkość rybosomów — przyspieszając lub zwalniając ją we właściwy sposób — może w przyszłości zwiększyć skuteczność istniejących leków na CML lub przełamać oporność. Badanie sugeruje, że fizyczne zachowanie rybosomów, a nie tylko ilość wytwarzanych białek, stanowi silną i możliwą do zaadresowania podatność w białaczce i prawdopodobnie w innych nowotworach.
Cytowanie: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Słowa kluczowe: przewlekła białaczka szpikowa, kolizje rybosomów, kinaza stresu ZAK, inhibitory BCR‑ABL, synteza białek