Clear Sky Science · nl
BCR::ABL1-tyrosinekinaseremmers veroorzaken ribosoombotsingen om ZAK-afhankelijke ribotoxische stress en apoptose in chronische myeloïde leukemie te activeren
Wanneer kankergeneesmiddelen met de eiwitfabrieken van de cel praten
Chronische myeloïde leukemie (CML) wordt vaak onder controle gehouden door gerichte geneesmiddelen die een kankerveroorzakend enzym, BCR::ABL1, uitschakelen. Toch verloopt de ziekte bij sommige patiënten naar een agressieve fase of ontwikkelen ze resistentie tegen de behandeling. Deze studie belicht een verrassende schakelaar in hoe deze geneesmiddelen kankercellen doden: de eiwitproducerende machines van de cel zelf, de ribosomen. Door te observeren wat er gebeurt wanneer deze machines vastlopen en op elkaar botsen, onthullen de auteurs een stressroute die zowel het groeien van CML-cellen ondersteunt als — onder medicamenteuze behandeling — bijdraagt aan hun vernietiging.
Een verborgen stressalarm in bloedkankercellen
Ribosomen functioneren meestal als goed getimede assemblagelijnen: ze lezen genetische boodschappen en zetten die om in eiwitten. Onder stress kunnen ribosomen echter vastlopen en in elkaar botsen, waardoor een "ribotoxisch" alarmsysteem in de cel wordt geactiveerd. De onderzoekers richtten zich op een sensorsproteïne genaamd ZAK, dat bovenaan een stress‑signaleringcascade zit. Door monsters van bijna 200 CML‑patiënten te analyseren, vonden zij dat ZAK en meerdere gerelateerde kwaliteitscontroledomeinen veel overvloediger aanwezig waren bij patiënten van wie de ziekte was gevorderd naar de gevaarlijke blastfase, en dat hogere ZAK‑niveaus samenhing met een groter aandeel onrijpe kankercellen in het bloed. Dit suggereert dat CML‑cellen naarmate de ziekte verergert sterk leunen op ZAK‑gekoppelde routes.
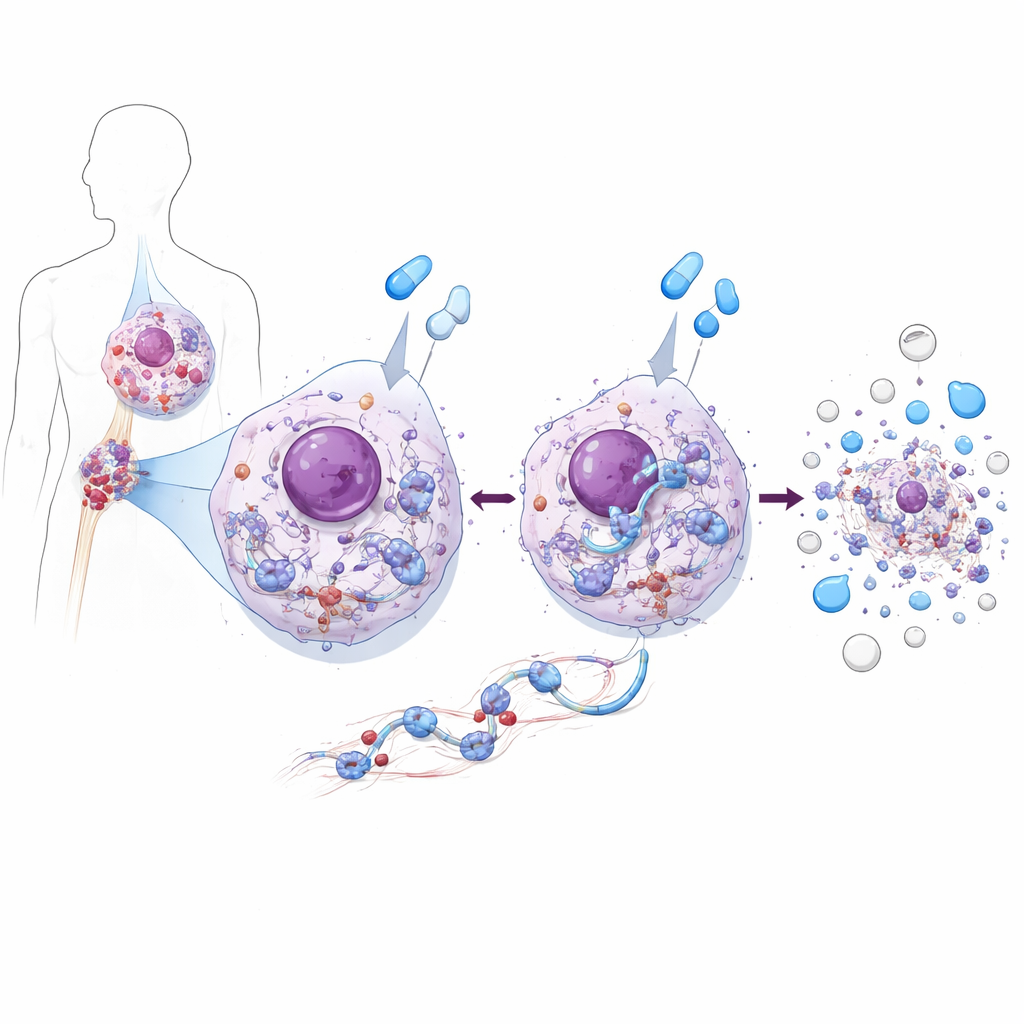
Eén eiwit dat zowel voedt als doodt in leukemiecellen
Met CML-cel-lijnen en patiëntafgeleide cellen ontdekte het team dat ZAK een dubbelrol vervult. In onbehandelde CML‑cellen ondersteunt ZAK de groei. Het verhoogt de activiteit van een belangrijke groeibevorderende keten, het AKT–mTOR‑pad, dat op zijn beurt eiwitproductie en celdeling stimuleert. Wanneer ZAK werd verwijderd of geremd, deelden leukemiecellen langzamer omdat dit groeipad verzwakte. Maar wanneer dezelfde cellen werden behandeld met BCR::ABL1‑blokkerende middelen zoals imatinib of asciminib, nam ZAK juist de tegenovergestelde rol aan: het was nodig om te zorgen dat de middelen efficiënte celdood teweegbrachten. Zonder ZAK raakten de geneesmiddelen wel hun doelenzym, maar waren de leukemiecellen veel minder geneigd tot apoptose, zelfs in monsters direct afkomstig van CML‑patiënten.
Hoe door geneesmiddelen vertraagde eiwitproductie tot ribosoomopstoppingen leidt
De auteurs vroegen zich vervolgens af hoe het uitschakelen van BCR::ABL1 leidt tot ZAK‑activatie. Ze ontdekten dat BCR::ABL1 normaal gesproken het mTOR‑pad actief houdt, wat zorgt voor snelle eiwitproductie. Wanneer de geneesmiddelen BCR::ABL1 blokkeerden, daalde de mTOR‑activiteit. Deze verandering schakelde downstreammechanismen om die de voortgang van ribosomen langs hun RNA‑sjablonen vertraagden. Metingen van nieuw gemaakte eiwitten bevestigden dat de translatie vertraagde, en gespecialiseerde gradientexperimenten toonden aan dat ribosomen in geneesmiddelbehandelde cellen dicht opeen kwamen te staan en botsingsgevoelige clusters vormden. Deze vastgelopen ribosomen waren ongewoon resistent tegen afbraak door nucleasen en waren beladen met collision‑sensoren zoals EDF1 en ZAK — duidelijke kenmerken dat de eiwitfabrieken van de cel mechanische stress ondervonden.
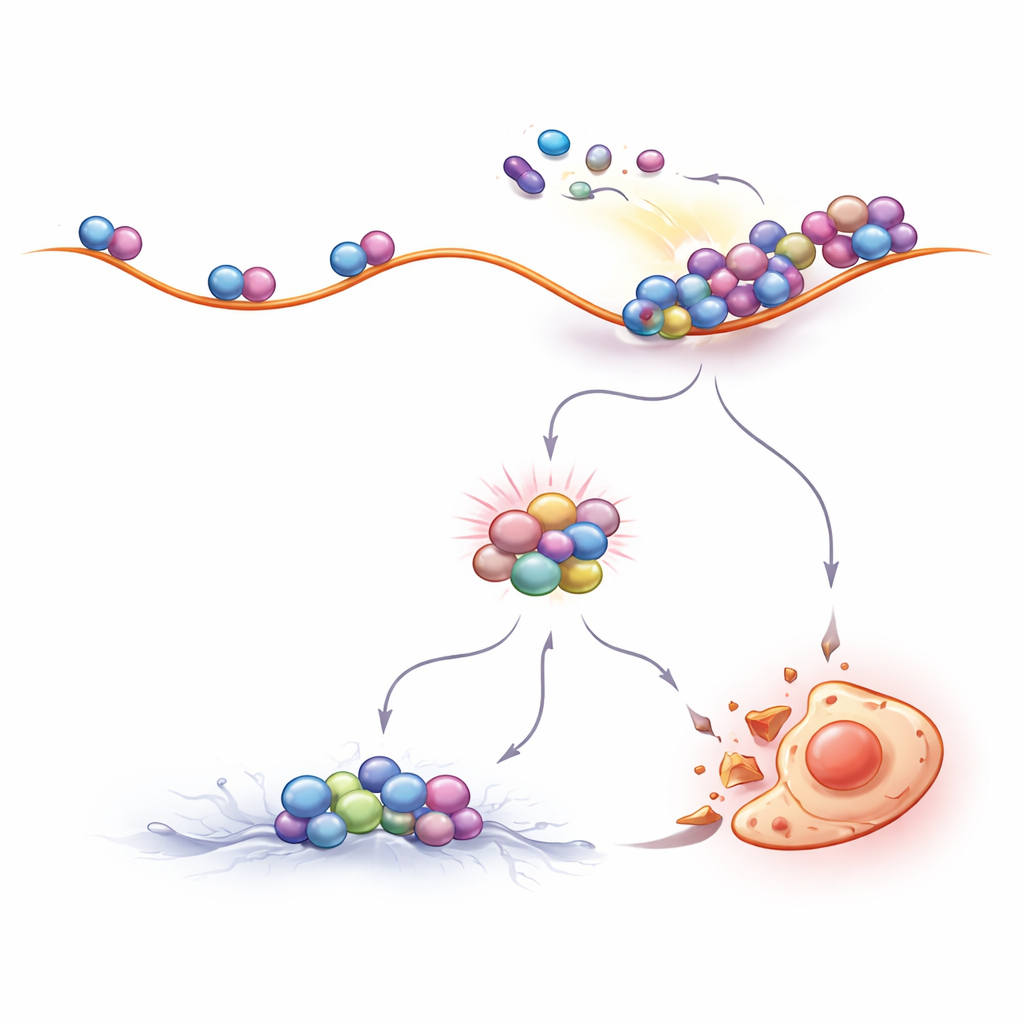
Ribosoomverkeer bijsturen om de behandeling effectiever te maken
Als ribosoombotsingen centraal staan in de werking van CML‑middelen, dan zou het opzettelijk wijzigen van het ribosoomverkeer de gevoeligheid voor geneesmiddelen moeten veranderen. Precies dat zagen de onderzoekers. Verbindingen die het aantal ribosomen dat nieuwe eiwitketens start verminderden, maakten botsingen minder waarschijnlijk en beschermden CML‑cellen tegen imatinib‑geïnduceerde dood. Daarentegen versterkten middelen die de stapsgewijze voortgang van ribosomen langs RNA licht vertraagden, of die hetzelfde vertragingsmechanisme in de cel activeerden, de botsingen en verhoogden ze sterk de effectiviteit van BCR::ABL1‑remmers bij het doden van CML‑cellen. Belangrijk is dat dit effect niet alleen in laboratoriumcellijnen werd gezien, maar ook in primaire cellen van patiënten, wat wijst op potentiële klinische relevantie.
Wat dit betekent voor patiënten en toekomstige therapieën
Voor niet‑specialisten is de kernboodschap dat CML‑middelen meer doen dan alleen een losgeslagen enzym uitschakelen; ze veroorzaken ook opstoppingen in de eiwitassemblagelijnen van de kankercel, waardoor ribosomen op elkaar botsen. Deze botsingen wekken ZAK, dat verandert van groeibevorderaar in uitvoerder door een stressroute te activeren die uitmondt in celdood. Door te leren hoe de snelheid van ribosomen fijn af te stemmen — ze op de juiste manier te versnellen of te vertragen — kunnen artsen mogelijk de effectiviteit van bestaande CML‑geneesmiddelen vergroten of resistentie overwinnen. De studie suggereert dat het fysieke gedrag van ribosomen, en niet alleen de hoeveelheid eiwit die zij maken, een krachtige en pharmaceutisch aan te pakken kwetsbaarheid is in leukemie en mogelijk andere vormen van kanker.
Bronvermelding: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Trefwoorden: chronische myeloïde leukemie, ribosoombotsingen, ZAK stresskinase, BCR-ABL-remmers, eiwitsynthese