Clear Sky Science · it
Inibitori della tirosina chinasi BCR::ABL1 inducono collisioni dei ribosomi per attivare lo stress ribotossico dipendente da ZAK e l’apoptosi nella leucemia mieloide cronica
Quando i farmaci antitumorali parlano alle fabbriche cellulari di proteine
La leucemia mieloide cronica (LMC) è spesso contenuta da farmaci mirati che spengono un enzima che guida il cancro chiamato BCR::ABL1. Tuttavia alcuni pazienti progrediscono comunque a una fase aggressiva o sviluppano resistenza alla terapia. Questo studio esplora un attore sorprendente nel modo in cui questi farmaci uccidono le cellule tumorali: le stesse macchine cellulari che fabbricano le proteine, i ribosomi. Osservando cosa accade quando queste macchine si bloccano e collidono, gli autori scoprono una via di stress che da un lato favorisce la crescita delle cellule di LMC e, sotto trattamento farmacologico, le porta alla distruzione.
Un allarme di stress nascosto nelle cellule del sangue tumorali
I ribosomi in genere funzionano come linee di montaggio ben sincronizzate, leggendo i messaggi genetici e assemblando le proteine. Sotto stress, però, i ribosomi possono incepparsi e urtarsi l’un l’altro, scatenando un sistema d’allarme “ribotossico” all’interno della cellula. I ricercatori si sono concentrati su una proteina sensore chiamata ZAK che sta in cima a una catena di segnalazione dello stress. Analizzando campioni di quasi 200 pazienti con LMC, hanno scoperto che ZAK e diversi fattori di controllo qualità correlati erano molto più abbondanti nei pazienti la cui malattia era progredita alla pericolosa fase blastica, e che livelli più alti di ZAK correla-vano con una maggiore proporzione di cellule ematiche tumorali immature. Ciò suggerisce che col peggiorare della LMC, le sue cellule fanno forte affidamento su vie legate a ZAK.
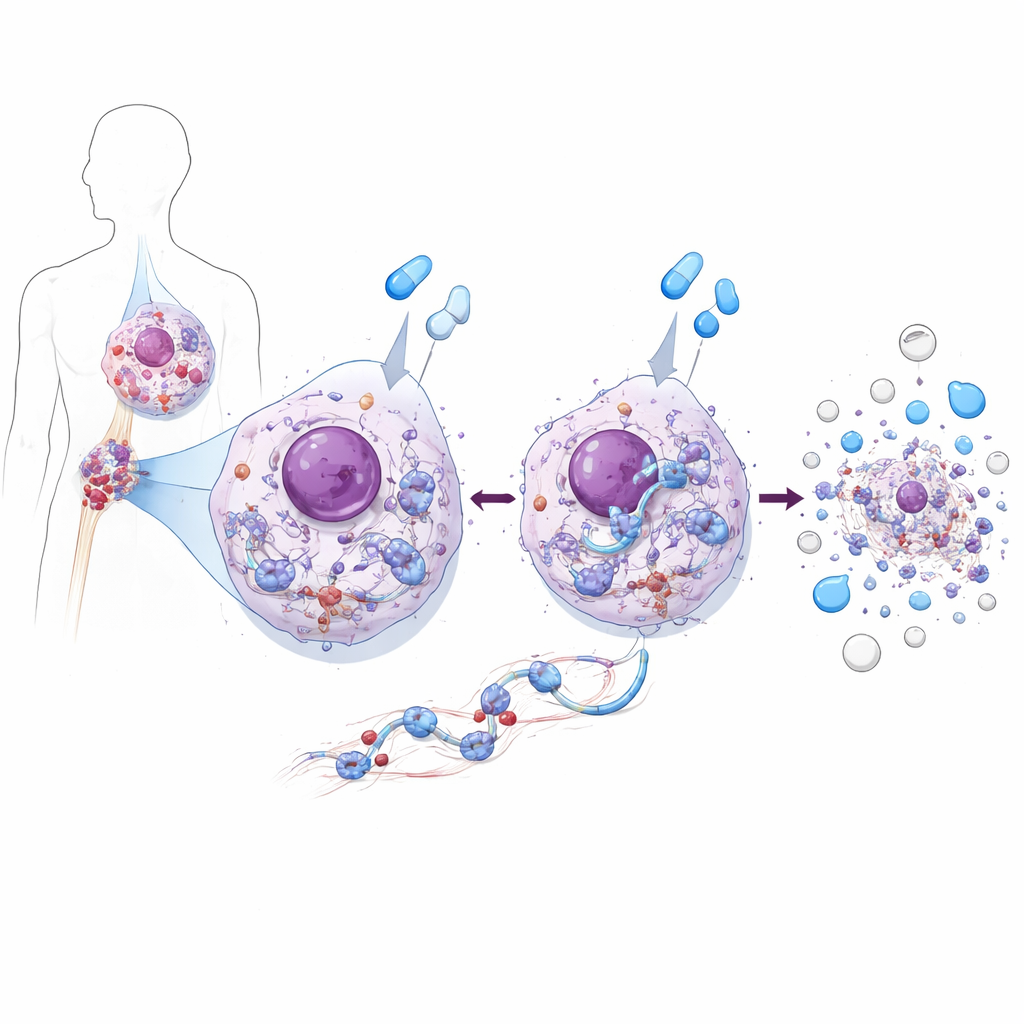
Una proteina che nutre e uccide le cellule leucemiche
Utilizzando linee cellulari di LMC e cellule derivate da pazienti, il gruppo ha scoperto che ZAK ha una doppia personalità. Nelle cellule di LMC non trattate, ZAK sostiene la crescita. Potenzia l’attività di una importante catena promuovente la crescita, la via AKT–mTOR, che a sua volta guida la produzione proteica e la divisione cellulare. Quando ZAK è stato rimosso o bloccato, le cellule leucemiche si dividevano più lentamente perché questa via di crescita veniva indebolita. Ma quando le stesse cellule sono state trattate con farmaci che bloccano BCR::ABL1 come imatinib o asciminib, ZAK ha svolto il ruolo opposto: era necessario affinché i farmaci innescassero una morte cellulare efficiente. Senza ZAK, questi farmaci colpivano comunque il loro enzima bersaglio ma le cellule leucemiche avevano molte meno probabilità di andare incontro ad apoptosi, anche nei campioni prelevati direttamente da pazienti con LMC.
Come la riduzione della sintesi proteica da farmaci causa ammassi di ribosomi
Gli autori si sono poi chiesti come lo spegnimento di BCR::ABL1 conduca all’attivazione di ZAK. Hanno scoperto che BCR::ABL1 mantiene normalmente la via mTOR attivata, che sostiene una rapida produzione proteica. Quando i farmaci bloccano BCR::ABL1, l’attività di mTOR cala. Questo cambiamento aziona interruttori a valle che rallentano il movimento dei ribosomi lungo i loro modelli di RNA. Le misure delle proteine neoformate hanno confermato che la traduzione rallentava, e esperimenti con gradienti specializzati hanno mostrato che nei cellule trattate il numero di ribosomi aumentava e si formavano ammassi soggetti a collisione. Questi ribosomi inceppati erano insolitamente resistenti alla degradazione da parte delle nucleasi e erano caricati di sensori di collisione come EDF1 e ZAK, firme chiare che le fabbriche proteiche della cellula erano sotto stress meccanico.
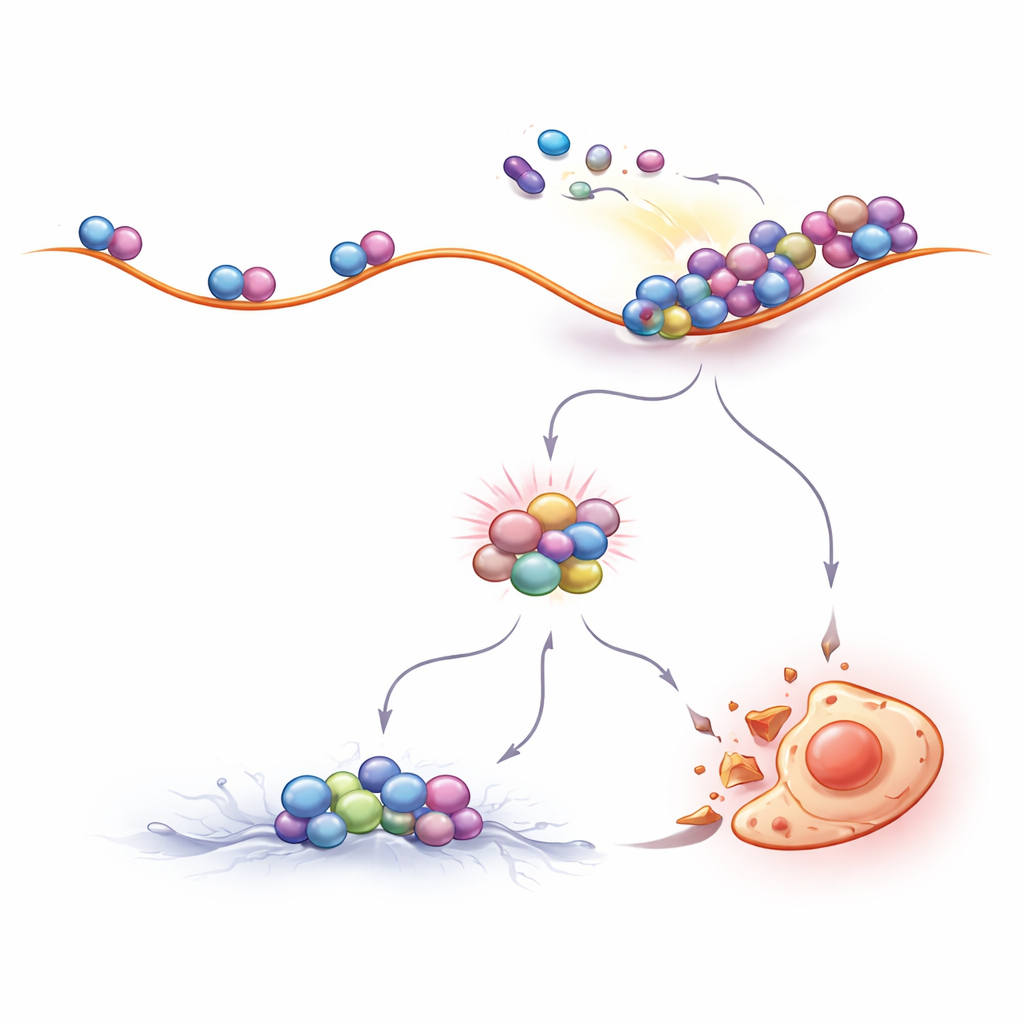
Regolare il traffico dei ribosomi per rendere il trattamento più efficace
Se le collisioni dei ribosomi sono centrali per il modo in cui funzionano i farmaci per la LMC, allora modificare deliberatamente il traffico dei ribosomi dovrebbe alterare la sensibilità ai farmaci. Questo è esattamente ciò che i ricercatori hanno osservato. Composti che riducevano il numero di ribosomi che iniziavano nuove catene proteiche rendevano le collisioni meno probabili e proteggevano le cellule di LMC dalla morte indotta da imatinib. Al contrario, farmaci che rallentavano leggermente il movimento passo dopo passo dei ribosomi lungo l’RNA, o che attivavano lo stesso meccanismo di rallentamento all’interno della cellula, aumentavano le collisioni e potenziavano notevolmente l’uccisione delle cellule di LMC da parte degli inibitori di BCR::ABL1. Importante, questo effetto è stato osservato non solo in linee cellulari da laboratorio ma anche in cellule primarie prelevate dai pazienti, sottolineandone la possibile rilevanza clinica.
Cosa significa per i pazienti e le terapie future
Per un non specialista, il messaggio chiave è che i farmaci per la LMC fanno più che spegnere un enzima deviato; bloccano anche le linee di assemblaggio proteico delle cellule tumorali, causando collisioni tra i ribosomi. Queste collisioni risvegliano ZAK, che passa dall’essere un fattore di crescita a comportarsi come un esecutore attivando una via di stress che termina nel suicidio cellulare. Imparando a modulare la velocità dei ribosomi — accelerandola o rallentandola nel modo giusto — i medici potrebbero alla fine migliorare l’efficacia dei farmaci esistenti per la LMC o superare la resistenza. Lo studio suggerisce che il comportamento fisico dei ribosomi, non solo la quantità di proteina che producono, è una vulnerabilità potente e farmacologicamente sfruttabile nella leucemia e, potenzialmente, in altri tumori.
Citazione: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Parole chiave: leucemia mieloide cronica, collisioni dei ribosomi, chinasi di stress ZAK, inibitori BCR-ABL, sintesi proteica