Clear Sky Science · ar
مثبطات كيناز التيروزين BCR::ABL1 تُحدث تصادمات في الريبوسومات لتنشيط الإجهاد الريبوزومي المعتمد على ZAK وإحداث الموت المبرمج في اللوكيميا النخاعية المزمنة
عندما تتحدث أدوية السرطان مع مصانع البروتين داخل الخلية
غالباً ما تُكبَح اللوكيميا النخاعية المزمنة (CML) بأدوية مستهدفة تُوقف إنزيماً دافعاً للسرطان يُدعى BCR::ABL1. ومع ذلك، ما يزال بعض المرضى يتقدم لديهم المرض إلى مرحلة عدوانية أو يطوّرون مقاومة للعلاج. تستكشف هذه الدراسة لاعباً مفاجئاً في كيفية قتل هذه الأدوية للخلايا السرطانية: آلات صنع البروتين داخل الخلية، الريبوسومات. من خلال مراقبة ما يحدث عندما تتعطل هذه الآلات وتتصادم، يكشف الباحثون عن مسار إجهادي يساعد خلايا CML على النمو، ولكنه تحت تأثير الدواء يساهم في تدميرها.
إنذار إجهادي مخفي داخل خلايا سرطان الدم
تعمل الريبوسومات عادة كخطوط تجميع متزامنة، تقرأ الرسائل الجينية وتربط الأحماض الأمينية لتكوين البروتينات. تحت الإجهاد، ومع ذلك، يمكن أن تتعطل الريبوسومات وتتصادم مع بعضها، مطلقة نظام إنذار "ريبوتوكسي" داخل الخلية. ركز الباحثون على بروتين حساس يُدعى ZAK يجلس في قمة سلسلة إشارات الإجهاد. بتحليل عينات من ما يقرب من 200 مريض بـ CML، وجدوا أن ZAK وعدداً من عوامل مراقبة الجودة ذات الصلة كانت أكثر وفرة بكثير في المرضى الذين تقدم مرضهم إلى الطور الانفجاري الخطير، وأن مستويات ZAK الأعلى ارتبطت بنسبة أكبر من الخلايا الدموية السرطانية غير الناضجة. وهذا يشير إلى أنه مع تفاقم CML، تتكئ خلاياها بقوة على المسارات المرتبطة بـ ZAK.
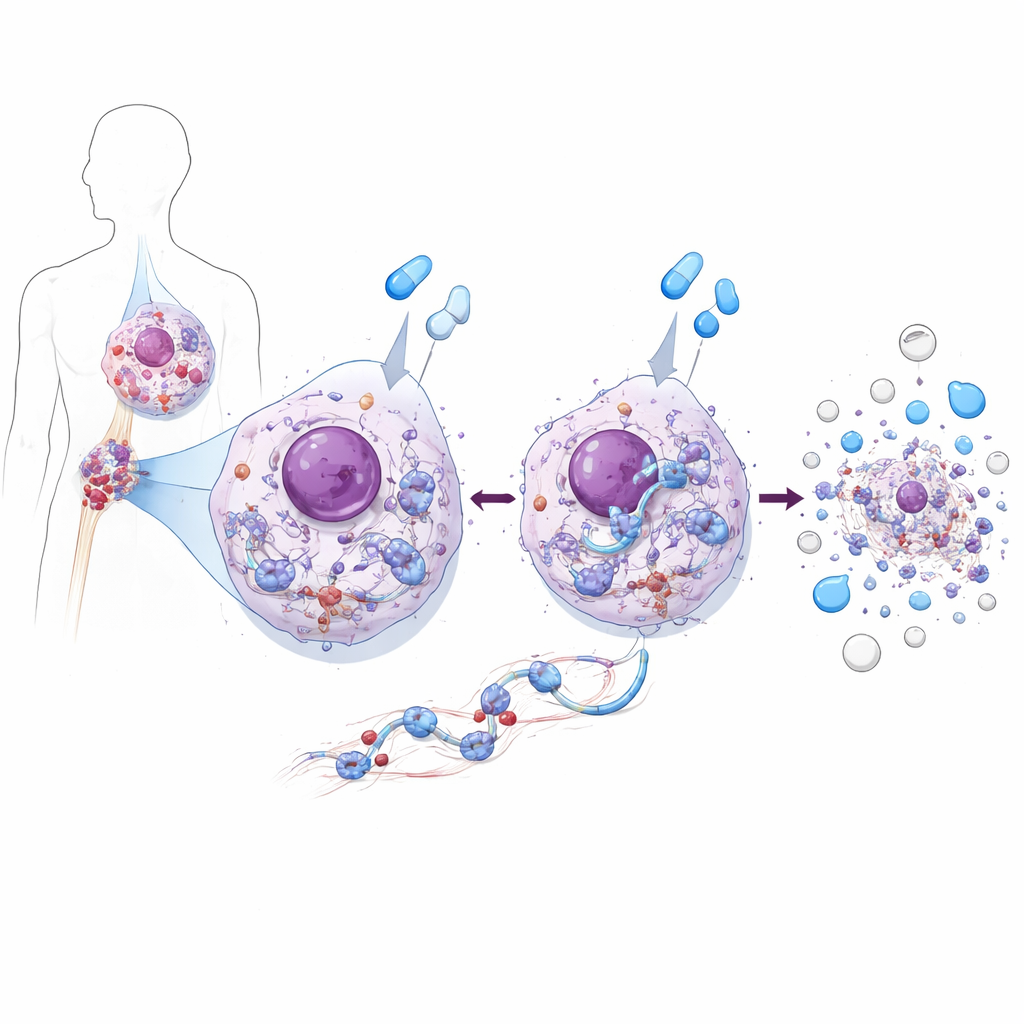
بروتين واحد يطعّم ويقتل خلايا اللوكيميا في آنٍ واحد
باستخدام خطوط خلايا CML وخلايا مأخوذة من مرضى، اكتشف الفريق أن ZAK له شخصية مزدوجة. في خلايا CML غير المعالجة، يدعم ZAK النمو. يعزز نشاط سلسلة رئيسية محفزة للنمو، مسار AKT–mTOR، الذي بدوره يدفع إنتاج البروتين وانقسام الخلايا. عندما أُزيل ZAK أو تم تثبيطه، انقسمت خلايا اللوكيميا ببطء أكبر لأن هذا المسار المحفز للنمو ضعُف. لكن عندما عولجت نفس الخلايا بأدوية تُثبط BCR::ABL1 مثل الإيماتينيب أو الأسيمينيب، لعب ZAK دوراً معاكساً: أصبح ضرورياً لكي تُحدث الأدوية موت الخلايا بكفاءة. بدون ZAK، ما زالت هذه الأدوية تضرب إنزيم الهدف لكنها جعلت خلايا اللوكيميا أقل ميلاً للخضوع للموت المبرمج، حتى في عينات مأخوذة مباشرة من مرضى CML.
كيف يسبب إبطاء تخليق البروتين بفعل الدواء تكدس الريبوسومات
ثم تساءل المؤلفون كيف يؤدي إيقاف BCR::ABL1 إلى تنشيط ZAK. وجدوا أن BCR::ABL1 يحافظ عادةً على تشغيل مسار mTOR، الذي يحافظ على إنتاج بروتين سريع. عندما حجبت الأدوية BCR::ABL1 ، انخفض نشاط mTOR. هذا التغير قلب مفاتيح لاحقة تُبطئ حركة الريبوسومات على قوالب الـ RNA. أكدت قياسات البروتينات الحديثة أن الترجمة تباطأت، وأظهرت تجارب تدرج متخصصة أن الريبوسومات في الخلايا المعالجة بالدواء أصبحت مزدحمة وشكلت تجمعات عرضة للتصادم. كانت هذه الريبوسومات العالقة مقاومة بشكل غير معتاد للتحلل بالنوكليازات ومحمّلة بأجهزة استشعار التصادم مثل EDF1 وZAK، وهي علامات واضحة أن مصانع البروتين داخل الخلية تتعرض لإجهاد ميكانيكي.
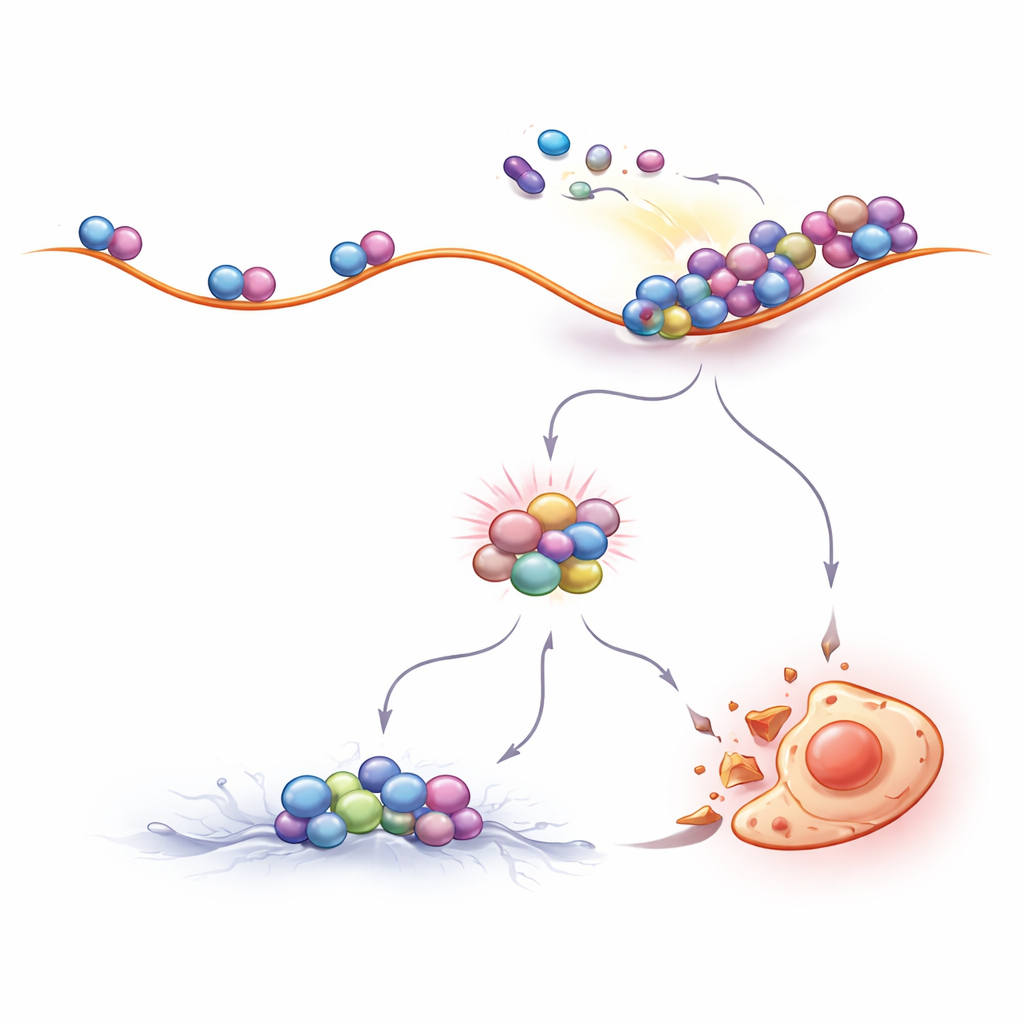
ضبط حركة الريبوسومات لتحسين فعالية العلاج
إذا كانت تصادمات الريبوسومات مركزية لآلية عمل أدوية CML، فالتلاعب عمداً بحركة الريبوسومات ينبغي أن يغير حساسية العلاج. وهذا بالضبط ما لاحظه الباحثون. المركبات التي خفّضت عدد الريبوسومات التي تبدأ سلاسل بروتينية جديدة جعلت التصادمات أقل احتمالاً وحمت خلايا CML من موت ناجم عن الإيماتينيب. في المقابل، الأدوية التي أبطأت قليلاً حركة الريبوسومات خطوة بخطوة على الـ RNA، أو التي نشطت نفس آلية الإبطاء داخل الخلية، زادت التصادمات وعززت بشكل كبير قتل خلايا CML بواسطة مثبطات BCR::ABL1. ومن المهم أن هذا التأثير لوحظ ليس فقط في خطوط الخلايا المختبرية بل أيضاً في خلايا أولية مأخوذة من مرضى، مما يبرز أهميته السريرية المحتملة.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
لغير المتخصص، الرسالة الرئيسية هي أن أدوية CML تفعل أكثر من مجرد إيقاف إنزيم منحرف؛ فهي أيضاً تُعيق خطوط تجميع البروتين في الخلية السرطانية، مما يسبب تصادم الريبوسومات. توقظ هذه التصادمات ZAK، الذي يتحول من مساعد للنمو إلى منفذ للأمر عبر تفعيل مسار إجهادي ينتهي بانتحار الخلية مبرمجاً. من خلال تعلّم كيفية ضبط سرعة الريبوسومات—تسريعها أو إبطاءها بالطريقة المناسبة—قد يتمكن الأطباء في نهاية المطاف من تعزيز فعالية أدوية CML الحالية أو التغلب على المقاومة. تشير الدراسة إلى أن السلوك الفيزيائي للريبوسومات، وليس فقط كمية البروتين الذي تصنعه، هو نقطة ضعف قوية وقابلة للاستهداف بالأدوية في اللوكيميا وربما سرطانات أخرى.
الاستشهاد: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
الكلمات المفتاحية: اللوكيميا النخاعية المزمنة, تصادمات الريبوسومات, كيناز الإجهاد ZAK, مثبطات BCR-ABL, تخليق البروتين