Clear Sky Science · de
BCR::ABL1-Tyrosinkinase-Inhibitoren verursachen Ribosomenkollisionen und aktivieren ZAK‑abhängigen ribotoxischen Stress sowie Apoptose bei chronischer myeloischer Leukämie
Wenn Krebsmedikamente mit den Proteinfabriken der Zelle sprechen
Die chronische myeloische Leukämie (CML) wird häufig durch zielgerichtete Medikamente kontrolliert, die ein krebsförderndes Enzym namens BCR::ABL1 abschalten. Dennoch schreiten bei einigen Patientinnen und Patienten die Erkrankung in eine aggressive Phase voran oder es entwickelt sich eine Resistenz gegen die Behandlung. Diese Studie untersucht einen überraschenden Akteur im Wirkmechanismus dieser Medikamente: die körpereigenen Proteinproduktionsmaschinen, die Ribosomen. Indem die Forscher beobachteten, was passiert, wenn diese Maschinen blockieren und zusammenstoßen, entdeckten sie einen Stressweg, der sowohl das Wachstum von CML‑Zellen unterstützt als unter Medikamenteneinfluss deren Zerstörung fördert.
Ein verborgenes Stressalarm‑System in Blutkrebszellen
Ribosomen arbeiten normalerweise wie gut getaktete Fließbänder: Sie lesen genetische Botschaften und verknüpfen Aminosäuren zu Proteinen. Unter Stress können Ribosomen jedoch ins Stocken geraten und aufeinanderprallen, wodurch ein „ribotoxischer“ Alarm im Inneren der Zelle ausgelöst wird. Die Forschenden konzentrierten sich auf ein Sensorprotein namens ZAK, das an der Spitze einer Stress‑Signalkaskade steht. Anhand von Proben aus fast 200 CML‑Patientinnen und ‑Patienten fanden sie, dass ZAK und mehrere damit verbundene Qualitätskontrollfaktoren in Fällen, in denen die Krankheit in die gefährliche Blastenphase übergegangen war, deutlich stärker exprimiert waren. Höhere ZAK‑Werte korrelierten zudem mit einem höheren Anteil unreifer krebsartiger Blutzellen. Das deutet darauf hin, dass CML‑Zellen mit Fortschreiten der Erkrankung zunehmend auf ZAK‑verknüpfte Wege angewiesen sind.
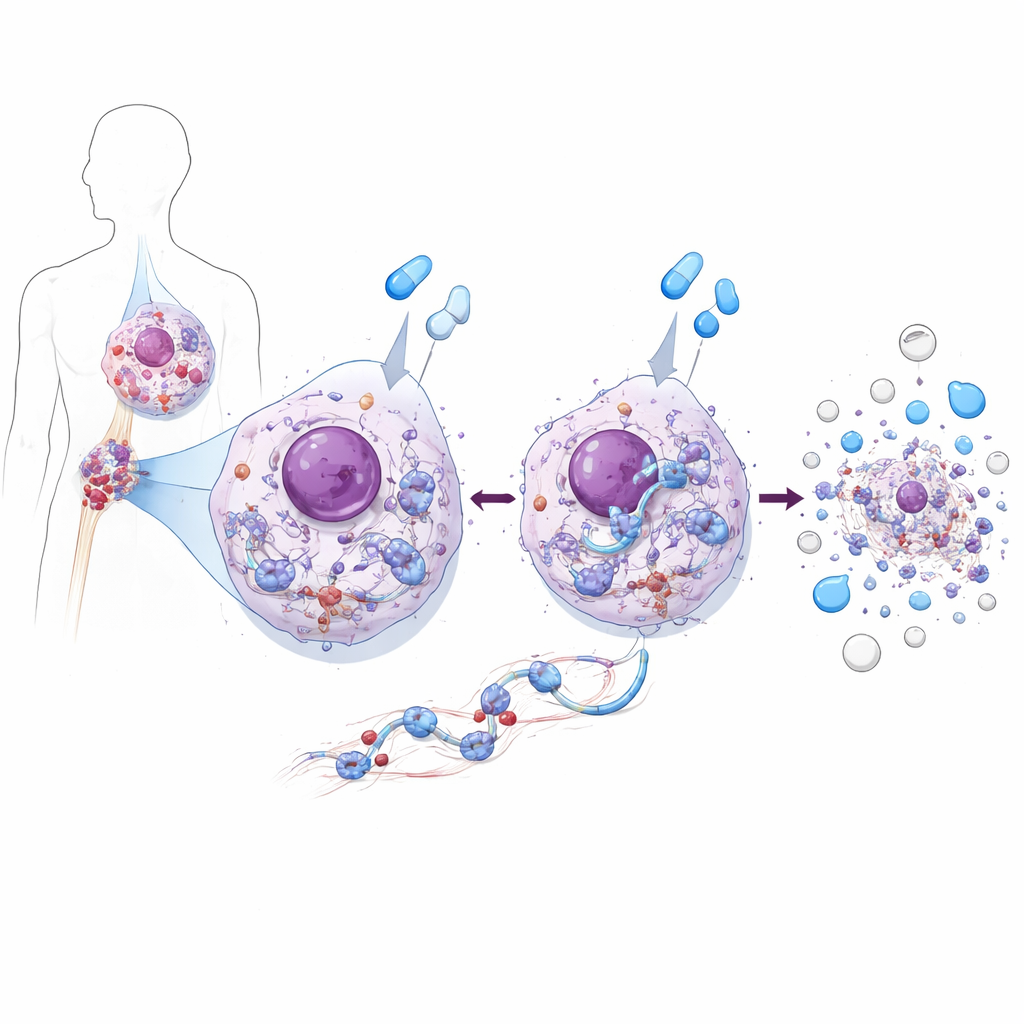
Ein Protein, das Leukämiezellen sowohl nährt als auch tötet
Anhand von CML‑Zelllinien und patientenabgeleiteten Zellen entdeckte das Team, dass ZAK eine Doppelfunktion besitzt. In unbehandelten CML‑Zellen unterstützt ZAK das Wachstum: Es fördert die Aktivität einer wichtigen wachstumsfördernden Kaskade, des AKT–mTOR‑Wegs, der wiederum die Proteinproduktion und Zellteilung antreibt. Wird ZAK entfernt oder blockiert, teilen sich die Leukämiezellen langsamer, weil dieser Wachstumsweg abgeschwächt ist. Behandelt man dieselben Zellen jedoch mit BCR::ABL1‑blockierenden Medikamenten wie Imatinib oder Asciminib, übernimmt ZAK die entgegengesetzte Rolle: Es ist erforderlich, damit die Medikamente einen effizienten Zelltod auslösen. Ohne ZAK treffen die Medikamente zwar weiterhin ihr Zielenzym, doch die Leukämiezellen durchlaufen deutlich seltener Apoptose — dies galt auch für Proben direkt von CML‑Patientinnen und ‑Patienten.
Wie medikamentös verlangsamte Proteinsynthese Ribosom‑Staus verursacht
Die Autorinnen und Autoren fragten dann, wie das Abschalten von BCR::ABL1 zur Aktivierung von ZAK führt. Sie fanden heraus, dass BCR::ABL1 normalerweise den mTOR‑Weg aktiviert hält, der eine schnelle Proteinsynthese aufrechterhält. Blockieren die Medikamente BCR::ABL1, fällt die mTOR‑Aktivität ab. Diese Veränderung schaltet nachgeschaltete Mechanismen um, die die Bewegung der Ribosomen entlang ihrer RNA‑Vorlagen verlangsamen. Messungen neu gebildeter Proteine bestätigten, dass die Translation langsamer wurde, und spezielle Gradientenexperimente zeigten, dass sich in medikamentös behandelten Zellen Ribosomen stauten und kollisionsanfällige Cluster bildeten. Diese blockierten Ribosomen waren ungewöhnlich resistent gegenüber dem Abbau durch Nukleasen und mit Kollisionssensoren wie EDF1 und ZAK beladen — eindeutige Signale dafür, dass die Proteinfabriken der Zelle mechanischem Stress ausgesetzt sind.
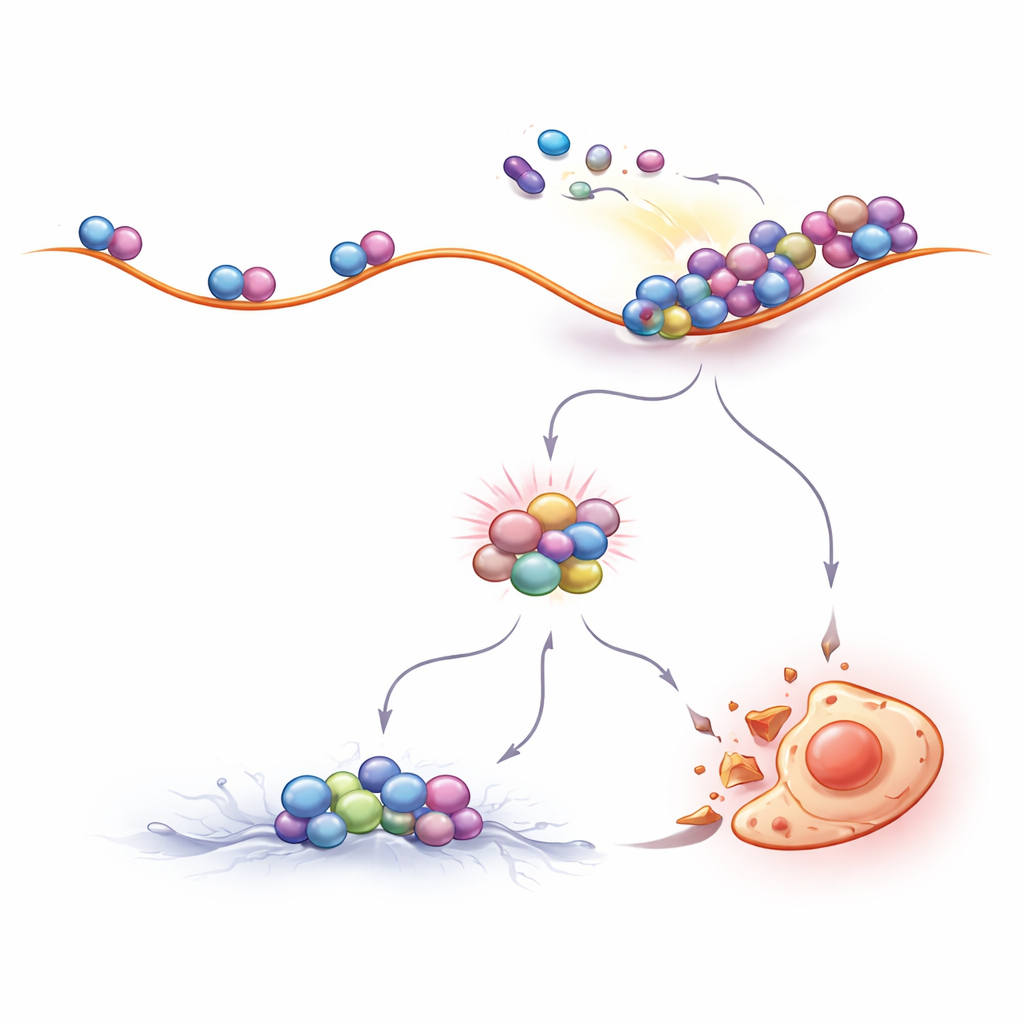
Ribosomalen Verkehr steuern, um die Behandlung zu verbessern
Wenn Ribosomenkollisionen zentral für die Wirksamkeit von CML‑Medikamenten sind, sollte eine gezielte Veränderung des Ribosomenverkehrs die Empfindlichkeit gegenüber den Medikamenten beeinflussen. Genau das beobachteten die Forschenden. Verbindungen, die die Zahl der Ribosomen reduzierten, die neue Proteinketten starten, machten Kollisionen weniger wahrscheinlich und schützten CML‑Zellen vor dem durch Imatinib induzierten Zelltod. Im Gegensatz dazu verstärkten Substanzen, die den schrittweisen Vorschub der Ribosomen entlang der RNA leicht verlangsamten, oder die denselben Verzögerungsmechanismus in der Zelle aktivierten, die Kollisionen und erhöhten deutlich die Abtötung von CML‑Zellen durch BCR::ABL1‑Inhibitoren. Wichtig ist, dass dieser Effekt nicht nur in Laborzelllinien, sondern auch in primären Zellen von Patientinnen und Patienten beobachtet wurde, was seine potenzielle klinische Relevanz unterstreicht.
Was das für Patientinnen und Patienten sowie künftige Therapien bedeutet
Für Nicht‑Spezialisten ist die Kernbotschaft: CML‑Medikamente schalten nicht nur ein fehlgeleitetes Enzym aus; sie verstopfen außerdem die Proteinmontagelinien der Krebszelle, wodurch Ribosomen kollidieren. Diese Kollisionen wecken ZAK, das seine Rolle vom Wachstumsunterstützer zum Vollstrecker wechselt, indem es einen Stressweg aktiviert, der in den Zelltod mündet. Indem man lernt, die Geschwindigkeit der Ribosomen fein zu justieren — sie an der richtigen Stelle zu beschleunigen oder zu verlangsamen — könnten Ärztinnen und Ärzte künftig die Wirksamkeit bestehender CML‑Medikamente erhöhen oder Resistenzen überwinden. Die Studie legt nahe, dass das physikalische Verhalten von Ribosomen, nicht nur die Menge an hergestelltem Protein, eine mächtige und pharmakologisch angreifbare Verwundbarkeit bei Leukämien und möglicherweise anderen Krebserkrankungen darstellt.
Zitation: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Schlüsselwörter: chronische myeloische Leukämie, Ribosomenkollisionen, ZAK-Stresskinase, BCR-ABL-Inhibitoren, Proteinsynthese