Clear Sky Science · fr
Les inhibiteurs de la tyrosine kinase BCR::ABL1 provoquent des collisions de ribosomes pour activer le stress ribotoxique dépendant de ZAK et l’apoptose dans la leucémie myéloïde chronique
Quand les médicaments anticancéreux s’adressent aux usines à protéines de la cellule
La leucémie myéloïde chronique (LMC) est souvent contrôlée par des médicaments ciblés qui désactivent une enzyme oncogénique nommée BCR::ABL1. Pourtant, certains patients progressent vers un stade agressif ou développent une résistance au traitement. Cette étude explore un acteur surprenant dans la manière dont ces médicaments tuent les cellules cancéreuses : les propres machines de fabrication des protéines de la cellule, les ribosomes. En observant ce qui se passe lorsque ces machines se bloquent et se percutent, les auteurs mettent au jour une voie de stress qui aide à la fois la croissance des cellules de LMC et, sous traitement, leur destruction.
Une alarme de stress cachée à l’intérieur des cellules hématologiques cancéreuses
Les ribosomes fonctionnent habituellement comme des chaînes d’assemblage bien cadencées, lisant les messages génétiques et assemblant les protéines. Sous stress, cependant, des ribosomes peuvent s’arrêter et se heurter les uns aux autres, déclenchant un système d’alarme « ribotoxique » à l’intérieur de la cellule. Les chercheurs se sont concentrés sur une protéine détectrice appelée ZAK qui occupe le sommet d’une cascade de signalisation de stress. En analysant des échantillons d’environ 200 patients atteints de LMC, ils ont constaté que ZAK et plusieurs facteurs de contrôle qualité associés étaient beaucoup plus abondants chez les patients dont la maladie avait évolué vers la phase blastique dangereuse, et que des niveaux plus élevés de ZAK corrélaient avec une proportion plus importante de cellules sanguines cancéreuses immatures. Cela suggère qu’à mesure que la LMC s’aggrave, ses cellules s’appuient fortement sur les voies liées à ZAK.
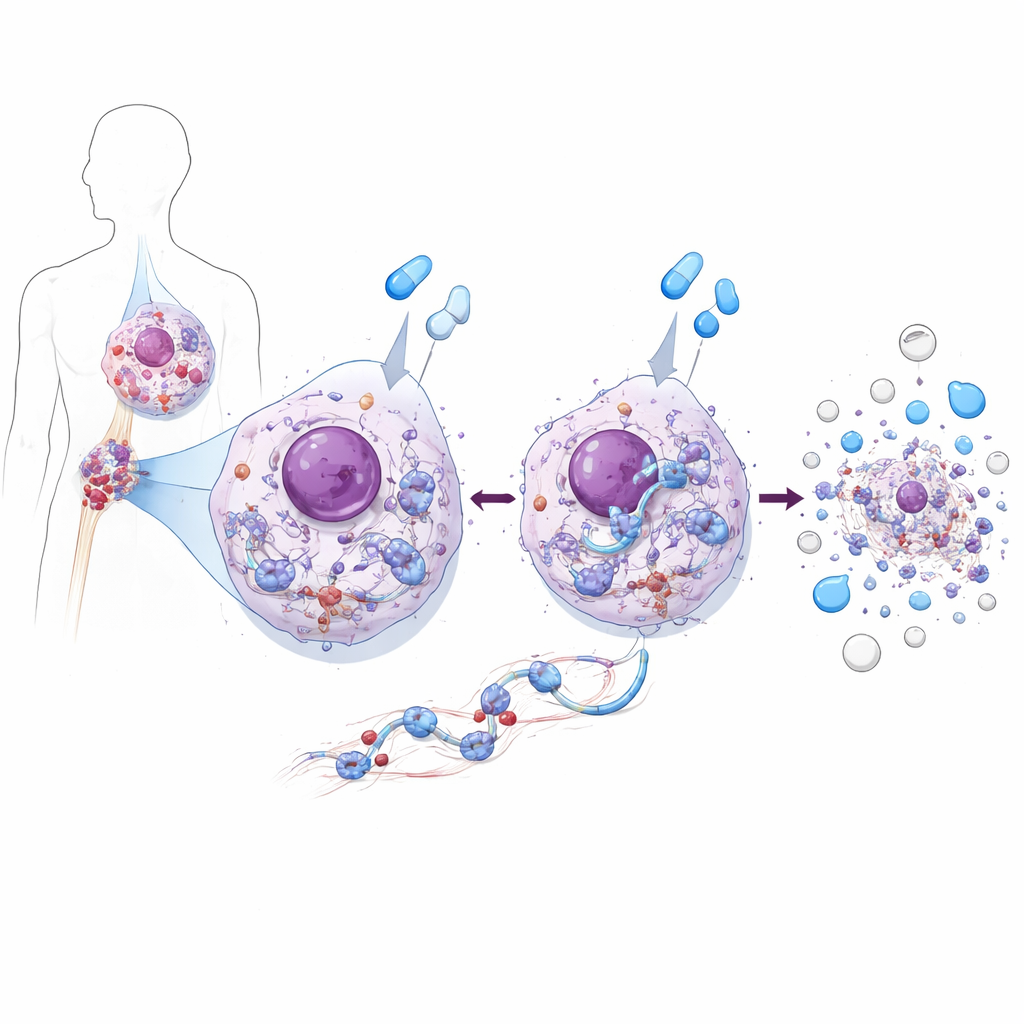
Une protéine qui à la fois nourrit et tue les cellules leucémiques
À l’aide de lignées cellulaires de LMC et de cellules issues de patients, l’équipe a découvert que ZAK a une double personnalité. Dans les cellules de LMC non traitées, ZAK soutient la croissance. Il augmente l’activité d’une chaîne majeure promotrice de croissance, la voie AKT–mTOR, qui stimule à son tour la production de protéines et la division cellulaire. Lorsque ZAK était éliminé ou bloqué, les cellules leucémiques se divisaient plus lentement parce que cette voie de croissance s’affaiblissait. Mais lorsque les mêmes cellules étaient traitées par des inhibiteurs de BCR::ABL1 tels que l’imatinib ou l’asciminib, ZAK jouait le rôle inverse : il était nécessaire pour que ces médicaments déclenchent une mort cellulaire efficace. Sans ZAK, ces médicaments atteignaient toujours leur enzyme cible mais les cellules leucémiques avaient beaucoup moins de chances de subir l’apoptose, y compris dans des échantillons directement prélevés chez des patients atteints de LMC.
Comment l’arrêt de la synthèse protéique par le médicament provoque des embouteillages de ribosomes
Les auteurs se sont ensuite demandé comment l’inhibition de BCR::ABL1 conduit à l’activation de ZAK. Ils ont constaté que BCR::ABL1 maintient normalement la voie mTOR activée, assurant une production protéique rapide. Lorsque les médicaments bloquent BCR::ABL1, l’activité de mTOR diminue. Ce changement modifie les régulateurs en aval qui ralentissent le déplacement des ribosomes le long de leurs matrices d’ARN. Des mesures des protéines nouvellement synthétisées ont confirmé que la traduction ralentissait, et des expériences par gradients spécialisées ont montré que les ribosomes dans les cellules traitées devenaient encombrés et formaient des amas susceptibles de collision. Ces ribosomes bloqués étaient inhabituellement résistants à la dégradation par les nucléases et étaient chargés de capteurs de collision tels qu’EDF1 et ZAK, signatures claires que les usines protéiques de la cellule étaient soumises à un stress mécanique.
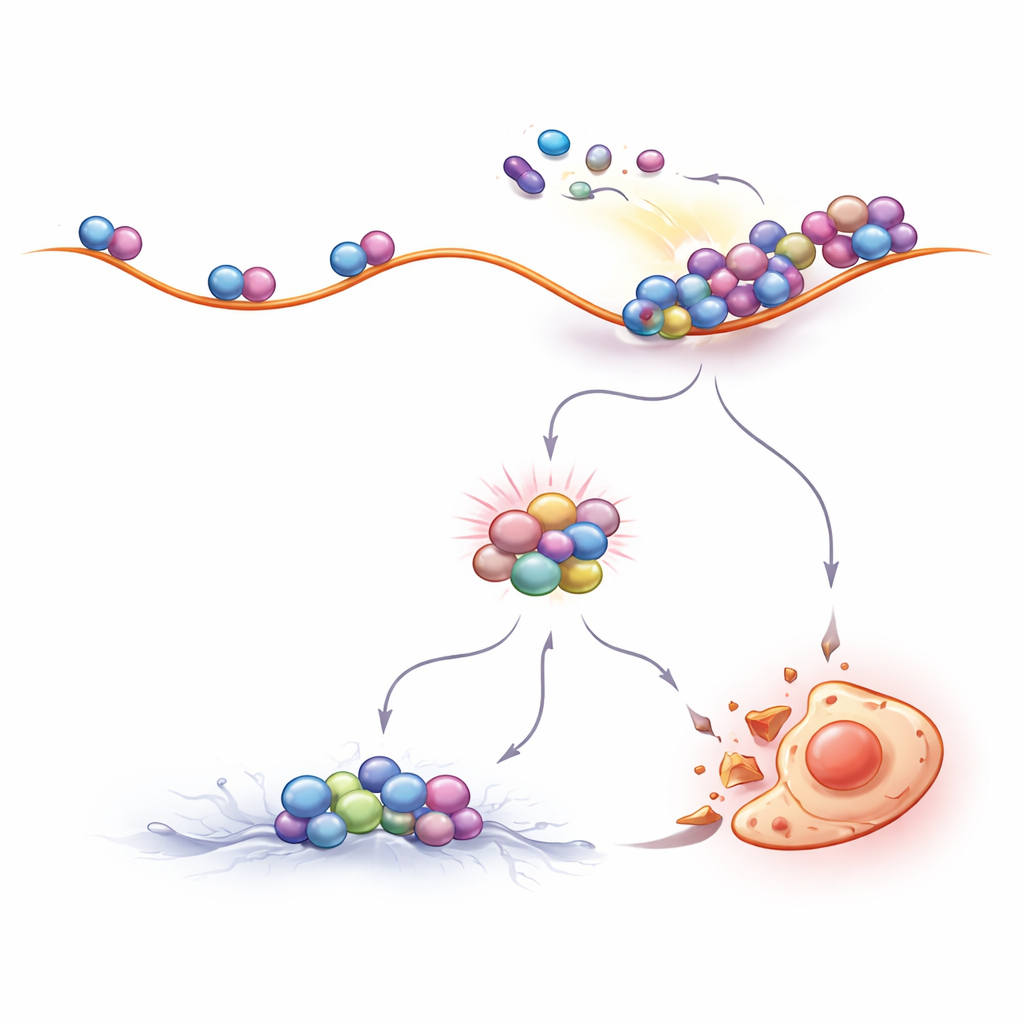
Moduler le trafic des ribosomes pour améliorer l’efficacité du traitement
Si les collisions de ribosomes sont centrales à l’action des médicaments contre la LMC, alors modifier délibérément le trafic des ribosomes devrait altérer la sensibilité aux médicaments. C’est exactement ce que les chercheurs ont observé. Des composés qui réduisaient le nombre de ribosomes initiant de nouvelles chaînes protéiques rendaient les collisions moins probables et protégeaient les cellules de LMC de la mort induite par l’imatinib. En revanche, des médicaments qui ralentissaient légèrement le mouvement pas à pas des ribosomes le long de l’ARN, ou qui activaient le même mécanisme de ralentissement à l’intérieur de la cellule, augmentaient les collisions et renforçaient fortement l’élimination des cellules de LMC par les inhibiteurs de BCR::ABL1. Fait important, cet effet a été observé non seulement dans des lignées cellulaires en laboratoire mais aussi dans des cellules primaires prélevées chez des patients, ce qui souligne sa pertinence clinique potentielle.
Ce que cela signifie pour les patients et les thérapies futures
Pour un non‑spécialiste, le message clé est que les médicaments contre la LMC font plus que simplement éteindre une enzyme défaillante ; ils bloquent aussi les chaînes d’assemblage protéique des cellules cancéreuses, provoquant des collisions de ribosomes. Ces collisions réveillent ZAK, qui passe d’un rôle d’aide à la croissance à un rôle d’exécuteur en déclenchant une voie de stress qui aboutit au suicide cellulaire. En apprenant à régler la vitesse des ribosomes — l’accélérer ou la ralentir de la manière appropriée — les médecins pourraient à terme améliorer l’efficacité des traitements existants contre la LMC ou surmonter la résistance. L’étude suggère que le comportement physique des ribosomes, et pas seulement la quantité de protéines qu’ils produisent, constitue une vulnérabilité puissante et pharmacologiquement exploitable dans la leucémie et potentiellement dans d’autres cancers.
Citation: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Mots-clés: leucémie myéloïde chronique, collisions de ribosomes, kinase de stress ZAK, inhibiteurs BCR-ABL, synthèse protéique