Clear Sky Science · sv
BCR::ABL1-tyrosinkinasinhibitorer orsakar ribosomkollisioner för att aktivera ZAK-beroende ribotoxisk stress och apoptos vid kronisk myeloisk leukemi
När cancerläkemedel talar med cellens proteinfabriker
Kronisk myeloisk leukemi (KML) hålls ofta i schack med riktade läkemedel som slår av ett cancerdrivande enzym kallat BCR::ABL1. Ändå utvecklar vissa patienter en aggressivare sjukdom eller blir resistenta mot behandlingen. Denna studie undersöker en oväntad aktör i hur dessa läkemedel dödar cancerceller: cellens egna proteinproducerande maskiner, ribosomerna. Genom att iaktta vad som händer när dessa maskiner fastnar och kolliderar avslöjar författarna en stressväg som både stödjer KML‑cellernas tillväxt och, under läkemedelsbehandling, bidrar till att förgöra dem.
En dold stresslarm inne i blodcancerceller
Ribosomer fungerar vanligtvis som välkoordinerade löpande band, läser genetiska budskap och fogar samman proteiner. Under stress kan ribosomer däremot stanna upp och krascha in i varandra, vilket utlöser ett ”ribotoxiskt” larmsystem inne i cellen. Forskarna fokuserade på ett sensorsprotein kallat ZAK som sitter högst upp i en stress‑signalväg. Genom att analysera prover från nästan 200 KML‑patienter fann de att ZAK och flera relaterade kvalitetskontrollfaktorer var mycket mer rikligt förekommande hos patienter vars sjukdom avancerat till den farliga blastfasen, och att högre ZAK‑nivåer korrelerade med en större andel omogna cancerceller i blodet. Detta antyder att när KML försämras, förlitar sig cellerna i hög grad på ZAK‑kopplade vägar.
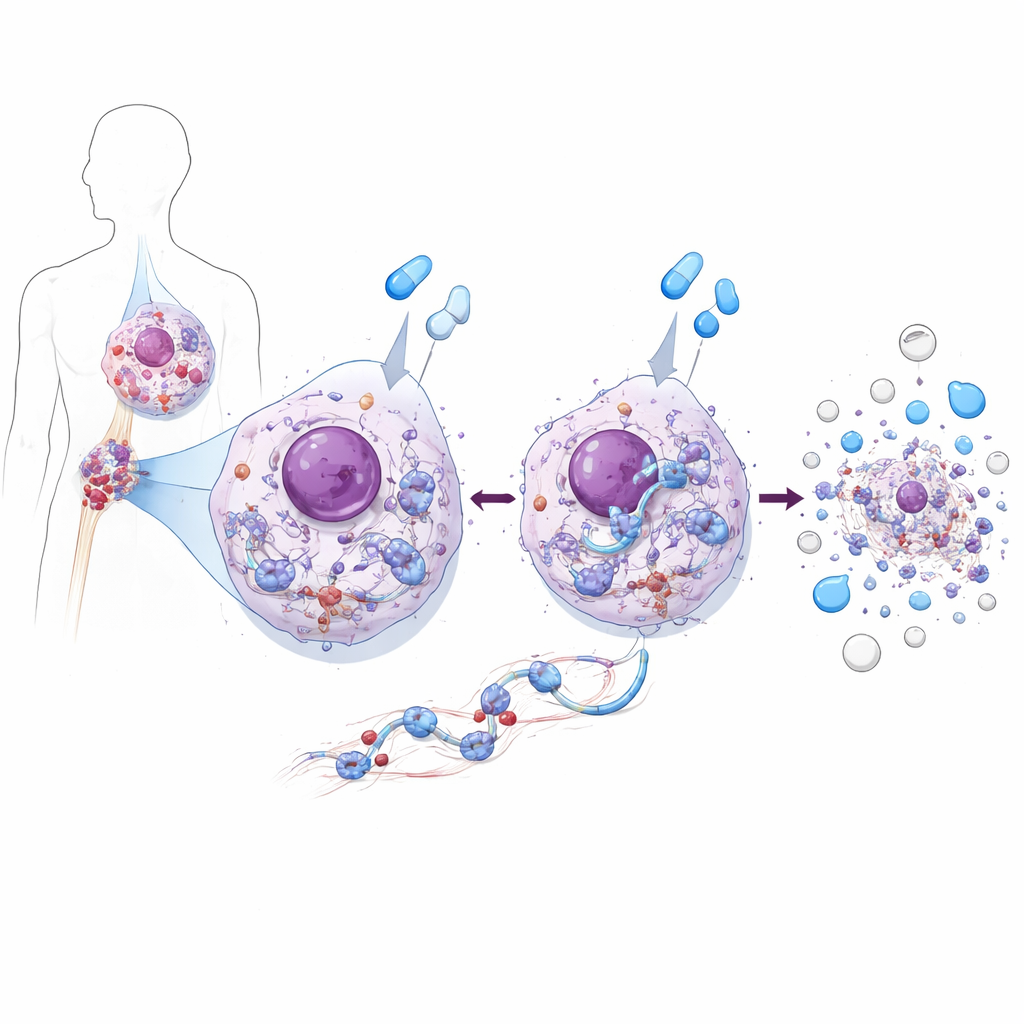
Ett protein som både matar och dödar leukemiceller
Med hjälp av KML‑cellinjer och celler härledda från patienter upptäckte teamet att ZAK har en dubbel natur. I obehandlade KML‑celler stödjer ZAK tillväxt. Det ökar aktiviteten i en viktig tillväxtfrämjande kedja, AKT–mTOR‑vägen, som i sin tur driver proteinsyntes och celldelning. När ZAK togs bort eller blockerades delade leukemicellerna långsammare eftersom denna tillväxtväg försvagades. Men när samma celler behandlades med BCR::ABL1‑blockerande läkemedel som imatinib eller asciminib spelade ZAK motsatt roll: det krävdes för att läkemedlen skulle utlösa effektiv celldöd. Utan ZAK slog dessa läkemedel fortfarande mot sitt målenzym, men leukemicellerna var mycket mindre benägna att genomgå apoptos, även i prover tagna direkt från KML‑patienter.
Hur läkemedelsinducerad långsammare proteinsyntes orsakar ribosomupphopningar
Författarna frågade sedan hur avstängning av BCR::ABL1 leder till ZAK‑aktivering. De fann att BCR::ABL1 normalt håller mTOR‑vägen igång, vilket upprätthåller snabb proteinsyntes. När läkemedlen blockerade BCR::ABL1 sjönk mTOR‑aktiviteten. Denna förändring vek om nedströmsbrytare som saktar ner ribosomernas rörelse längs deras RNA‑mallar. Mätningar av nybildade proteiner bekräftade att translationen fördröjdes, och specialiserade gradientexperiment visade att ribosomer i läkemedelsbehandlade celler blev trängda och bildade grupper benägna att kollidera. Dessa fastkilade ribosomer var ovanligt motståndskraftiga mot nedbrytning av nukleaser och var fyllda med kollisionsensorer som EDF1 och ZAK — tydliga signaturer på att cellens proteinfabriker utsattes för mekanisk stress.
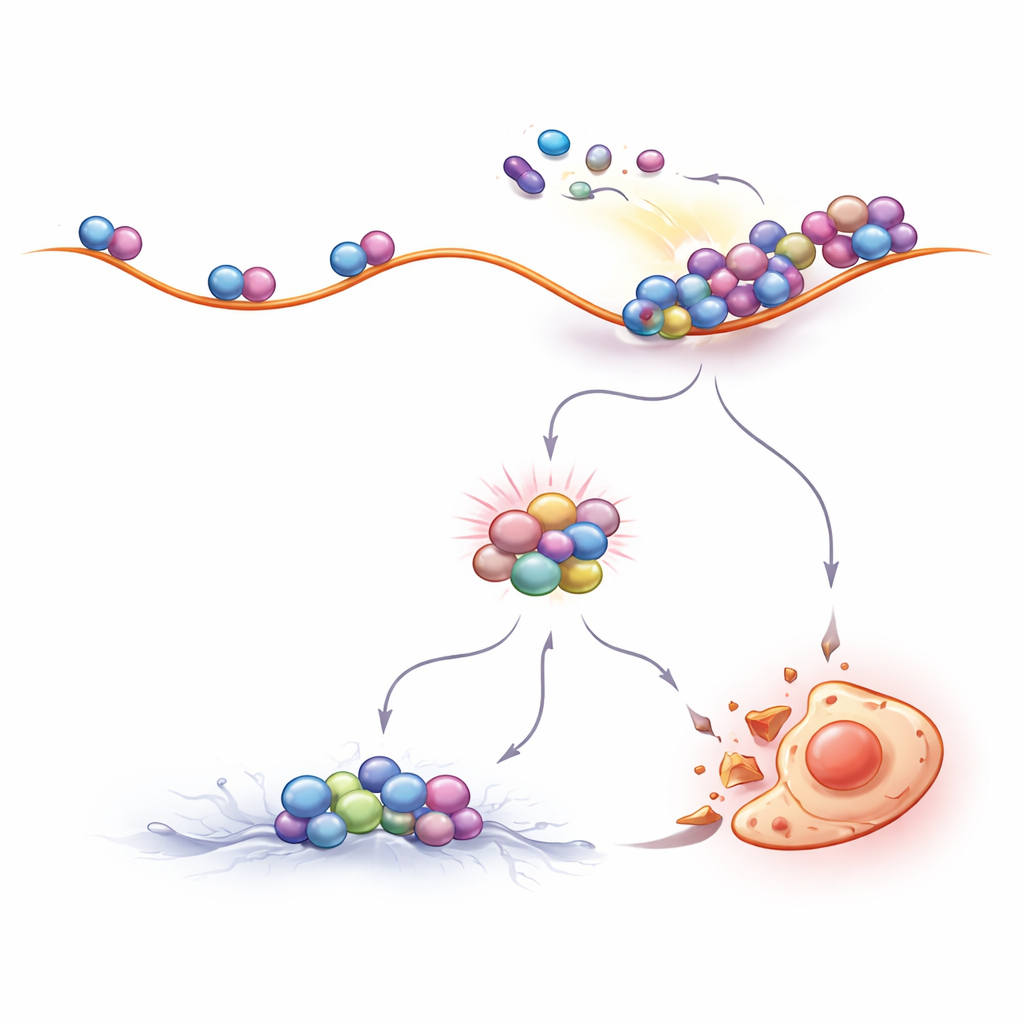
Justera ribosomtrafiken för att förbättra behandlingseffekten
Om ribosomkollisioner är centrala för hur KML‑läkemedel fungerar, borde avsiktliga förändringar i ribosomtrafiken ändra läkemedelskänsligheten. Det är precis vad forskarna observerade. Föremål som minskade antalet ribosomer som startade nya proteinkedjor gjorde kollisioner mindre sannolika och skyddade KML‑celler från imatinib‑inducerad död. I kontrast ökade läkemedel som lätt bromsade ribosomernas stegvisa rörelse längs RNA, eller som aktiverade samma inre bromsmekanism i cellen, antalet kollisioner och förhöjde kraftigt dödligheten av KML‑celler vid behandling med BCR::ABL1‑hämmare. Viktigt är att denna effekt sågs inte bara i laboratoriecellinjer utan också i primära celler tagna från patienter, vilket understryker dess potentiella kliniska relevans.
Vad detta innebär för patienter och framtida terapier
För en icke‑specialist är huvudbudskapet att KML‑läkemedel gör mer än att stänga av ett felaktigt enzym; de fastar också cancercellens proteinmonteringsband, vilket orsakar att ribosomer kolliderar. Dessa kollisioner väcker ZAK, som går från att vara en tillväxthjälpare till att agera som bödel genom att utlösa en stressväg som slutar i celldöd. Genom att lära sig hur man finjusterar ribosomernas hastighet — att öka eller minska den på rätt sätt — kan läkare så småningom förstärka effekten av befintliga KML‑läkemedel eller övervinna resistens. Studien antyder att ribosomernas fysiska beteende, inte bara mängden protein de producerar, är en kraftfull och läkbar sårbarhet i leukemi och potentiellt i andra cancerformer.
Citering: Park, J., Kim, SH., Park, J. et al. BCR::ABL1 tyrosine kinase inhibitors induce ribosome collisions to activate ZAK-dependent ribotoxic stress and apoptosis in chronic myeloid leukemia. Leukemia 40, 955–969 (2026). https://doi.org/10.1038/s41375-026-02916-3
Nyckelord: kronisk myeloisk leukemi, ribosomkollisioner, ZAK stresskinas, BCR-ABL-hämmare, proteinsyntes