Clear Sky Science · tr
B-hücre reseptörü ile NOTCH1 arasındaki fonksiyonel işbirliği: kronik lenfositik lösemide metabolik yeniden programlamanın düzenlenmesi
Hastalar ve aileleri için bunun önemi
Kronik lenfositik lösemi (KLL), erişkinlerde en sık görülen lösemidir; birçok kişi yıllarca bu hastalıkla yaşasa da bazı olgular agresifleşir ve tedaviye dirençli hale gelir. Bu çalışma basit ama kritik bir soruyu soruyor: bazı KLL hücrelerini daha hızlı büyüten ve tedaviye dayanıklı kılan nedir ve bu zayıflık tersine çevrilip hedef alınabilir mi? Araştırmacılar, lösemi hücrelerindeki iki anahtar anahtarın hücrelerin enerji kullanımını nasıl birlikte yeniden düzenlediğini ortaya koyuyor; bu durum hem büyüme üstünlüğü sağlıyor hem de doktorların hedefleyebileceği gizli bir metabolik Aşil topuğu oluşturuyor.
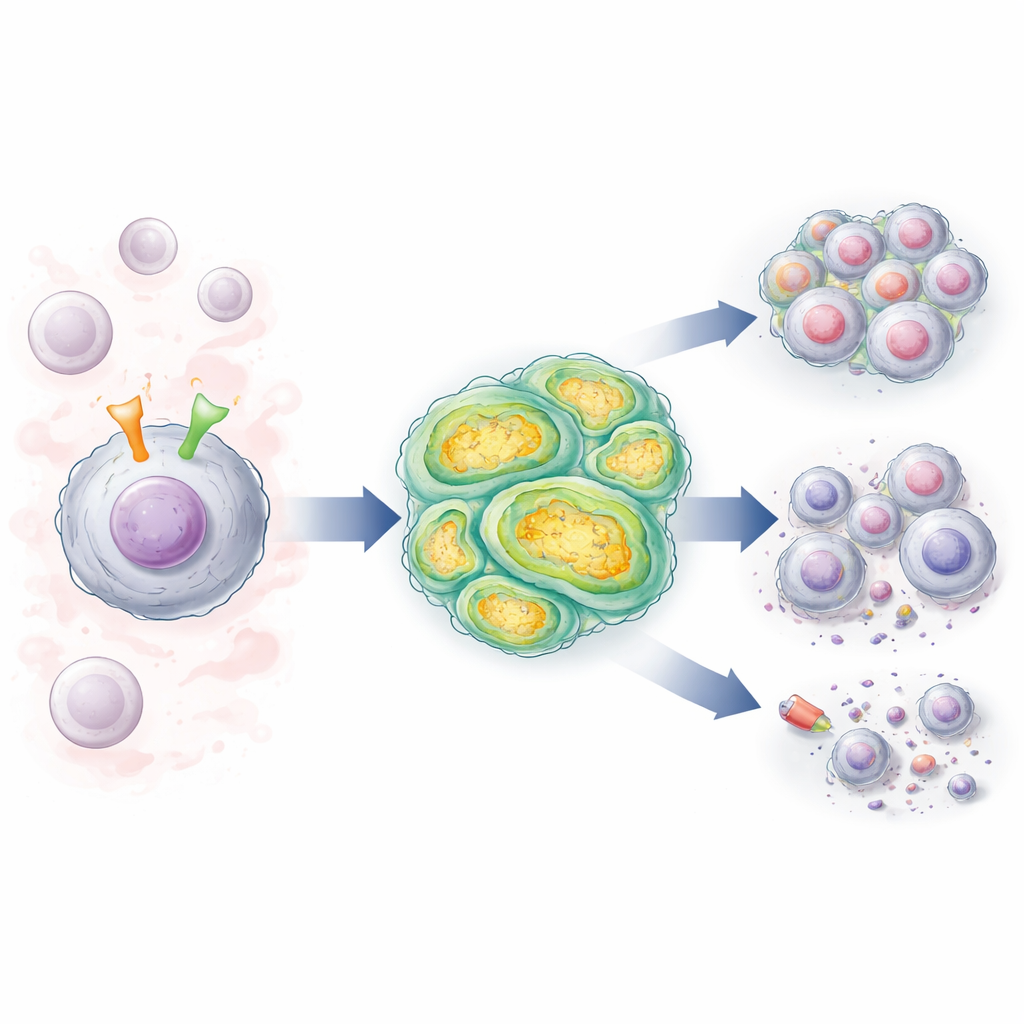
Birbirleriyle iletişim kuran iki hücresel anahtar
KLL hücrelerinin yüzeyinde, kandaki ve lenf düğümlerindeki sinyalleri algılayan ve hücreleri hayatta kalmaya ve bölünmeye iten B-hücre reseptörü (BCR) adlı bir anten bulunur. Birçok hastada ayrıca NOTCH1 adlı bir genin değişiklikleri vardır; bu gen, aktive olduğunda çekirdeğe güçlü büyüme ve sağkalım sinyalleri gönderen başka bir yüzey molekülünü kodlar. Yazarlar, BCR'leri yüksek riskli, “mutasyonsuz” desen paylaşan hastalardan elde edilen KLL hücrelerini; normal NOTCH1 taşıyan hücrelerle NOTCH1 mutasyonlu hücreleri karşılaştırdı. BCR uyarıldığında NOTCH1 aktivitesinin özellikle mutasyonlu hücrelerde güçlü şekilde arttığını ve lösemik sinyallemenin sürekli açık kalmasını güçlendiren bir geri besleme döngüsünü kuvvetlendirdiğini buldular.
Lösemi hücrelerinin enerji üretimini yeniden kablolama
Gen ifade haritaları ve enerji kullanımı üzerine doğrudan ölçümler, NOTCH1 mutasyonlu KLL hücrelerinin mitokondrilerini mutasyona sahip olmayan hücrelerden çok daha yoğun şekilde çalıştırdığını gösterdi. Bu hücreler hem glikoliz (şeker yıkımı) hem de mitokondriyal solunum yoluyla daha fazla yakıt yaktı, daha fazla hücresel “pil” molekülü (ATP) üretti ve daha fazla reaktif oksijen türü ortaya koydu; bunların hepsi hızlandırılmış bir motorun işaretleri. Mikroskopi, NOTCH1 mutasyonlu hücrelerin daha fazla ve daha büyük mitokondriye sahip olduğunu ve bunların yoğun ağlar oluşturduğunu, bunun da ek mitokondriyal DNA ile desteklendiğini gösterdi. BCR tetiklendiğinde, zaten yüksek olan bu metabolik aktivite daha da yükseldi; bu, hücre dışından gelen sinyallerin önceden hazırlıklı bir enerji sistemini aşırı çalıştırabileceğini gösteriyor.
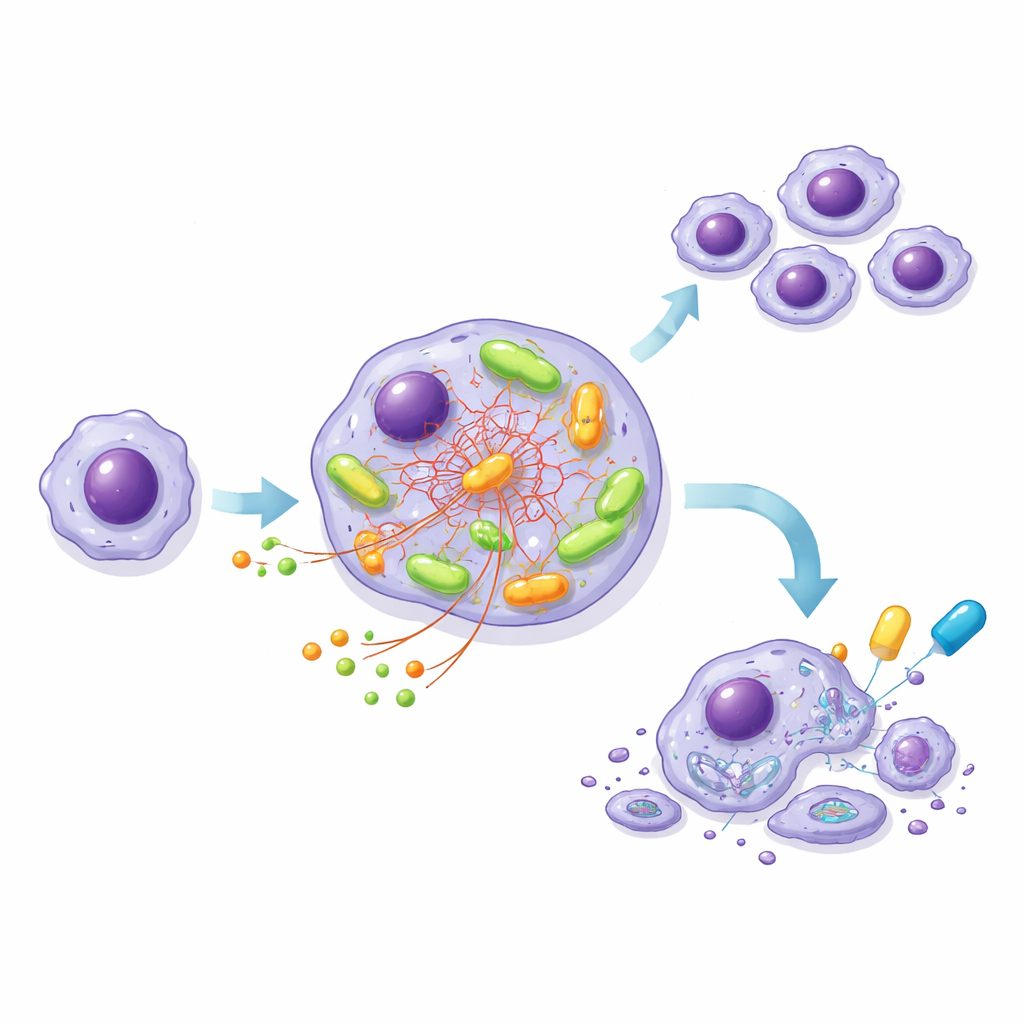
Motoru çözümlemek için bir model hücre hattı kurmak
Hastadan alınan KLL hücreleri laboratuvarda kolayca çoğalmadığı için ekip, MEC-1 adlı lösemi-benzeri bir hücre hattını iki versiyonda mühendislik yaptı: biri normal NOTCH1 ile, diğeri ise kesik ve aşırı aktif bir NOTCH1 ile; her iki versiyon da aynı yüksek riskli BCR'yi taşıyordu. Bu kontrollü sistem, hasta örneklerinde görüleni yansıttı. Mutant hücreler daha fazla glukoz tüketti, daha fazla ATP üretti ve özellikle BCR aktivasyonundan sonra oksijen tüketimleri daha yüksekti. Etiketlenmiş besinlerle yapılan detaylı izleme deneyleri, mutasyonlu hücrelerde glukozun yapı taşları ve koruyucu moleküller yapmak üzere yönlendirildiğini, diğer bir besin olan glutaminin ise mitokondriler içindeki merkezi enerji döngüsünü besleyen ana yakıt haline geldiğini gösterdi.
Mitokondrilerin bir baş kontrolörü ve yakıt bağımlılığı
NOTCH1'in mitokondrileri nasıl yeniden şekillendirdiğini anlamak için araştırmacılar kromatin manzarasını—DNA'nın paketlenme ve etkinlik işaretleme biçimini—incelediler. Mutant hücrelerde, aktif NOTCH1 formunun doğrudan TFAM adlı bir genin yakınında bağlandığını ve bu kilit mitokondriyal DNA ve fonksiyon kontrolörünü artırdığını buldular. TFAM bloke edildiğinde yalnızca NOTCH1 mutasyonlu hücrelerde mitokondriyal kütle azaldı ve bu hücrelerde hücre ölümü tetiklendi; bu durum bu hücrelerin bu mitokondriyal programa benzersiz şekilde bağımlı olduğunu gösterdi. Fonksiyonel olarak, mutant hücreler karışık kültürlerde normal hücrelerden daha hızlı büyüdü. Ekip, glutamin girişini bloke ettiğinde mutant hücrelerin büyüme avantajının ortadan kalktığını ve hem mühendislik yapılmış hücrelerin hem de primer NOTCH1 mutasyonlu KLL hücrelerinin çok daha savunmasız hale geldiğini gördü; bu, güçlü bir glutamin “bağımlılığı”nı ortaya koyuyor.
Bir zayıflığı tedavi stratejisine dönüştürmek
Çalışma daha sonra bu yakıt bağımlılığının mevcut ilaçların etkinliğini artırıp artırmayacağını test etti. Venetoklaks, mitokondriyal yol ile hücre ölümünü tetikleyerek KLL hücrelerini öldüren hedefe yönelik bir ilaç, NOTCH1 mutasyonlu hücrelere karşı normal hücrelerden daha etkiliydi. Dikkat çekici şekilde, glutamin taşımasını bloke etme ile venetoklaksın kombinasyonu lösemi hücresi ölümünü keskin şekilde artırdı ve bu sinerji NOTCH1 mutasyonlu hücrelere özgüydü. Ek genetik hasar taşıyan tipik olarak ilaç dirençli bir model bile bu kombinasyon altında duyarlı hale geldi. Günlük ifadeyle, mutasyona ağır lösemi hücreleri mitokondrilerini glutamin üzerinde yüksek çalıştırarak hayatta kalır; bu yakıt hattı kesilip aynı anda pro-ölüm sinyali uygulandığında, güç sistemleri çöker ve hücreler toparlanamaz.
Bundan sonra ne anlama geliyor
Düz bir dille yazarlar, NOTCH1’deki genetik bir değişikliğin B-hücre reseptörü aracılığıyla alınan sinyallerle birlikte belirli KLL hücrelerini daha büyük, daha yoğun çalışan enerji santralleri kurmaya ve enerji ve büyüme için büyük ölçüde glutamin amino asidine bağımlı hale getirdiğini gösteriyor. Aynı bağımlılık, özellikle venetoklaks gibi mitokondrilere saldıran bir ilaçla birleştirildiğinde, glutamin kullanımının engellenmesi halinde bunları olağanüstü derecede kırılgan kılıyor. Gerçekçi hasta benzeri ortamlarda daha fazla çalışma gerekli olsa da, bu metabolik zayıflık, NOTCH1 mutasyonu taşıyan KLL vakalarına özgü tedaviyi kişiselleştirmek için umut verici bir yol sunuyor; standart hedefe yönelik ilaçların dikkatle seçilmiş metabolik tedavilerle eşleştirilmesiyle sonuçların iyileştirilmesi potansiyeli taşıyor.
Atıf: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Anahtar kelimeler: kronik lenfositik lösemi, NOTCH1 mutasyonu, kanser metabolizması, mitokondri, glutamin bağımlılığı