Clear Sky Science · nl
Functionele samenwerking tussen de B-celreceptor en NOTCH1 bij het reguleren van metabole herschikking in chronische lymfatische leukemie
Waarom dit belangrijk is voor patiënten en families
Chronische lymfatische leukemie (CLL) is de meest voorkomende vorm van leukemie bij volwassenen; veel mensen leven er jaren mee, maar in sommige gevallen wordt de ziekte agressief en moeilijk behandelbaar. Deze studie stelt een eenvoudige maar cruciale vraag: wat maakt dat sommige CLL-cellen sneller groeien en resistent worden tegen behandeling, en kan die kwetsbaarheid tegen hen worden gebruikt? De onderzoekers tonen aan hoe twee belangrijke schakelaars op leukemiecellen samenwerken om het energiegebruik van de cellen ingrijpend te veranderen, wat zowel een groeivoordeel als een verborgen metabool Achillespees creëert die clinici mogelijk kunnen doelwitten.
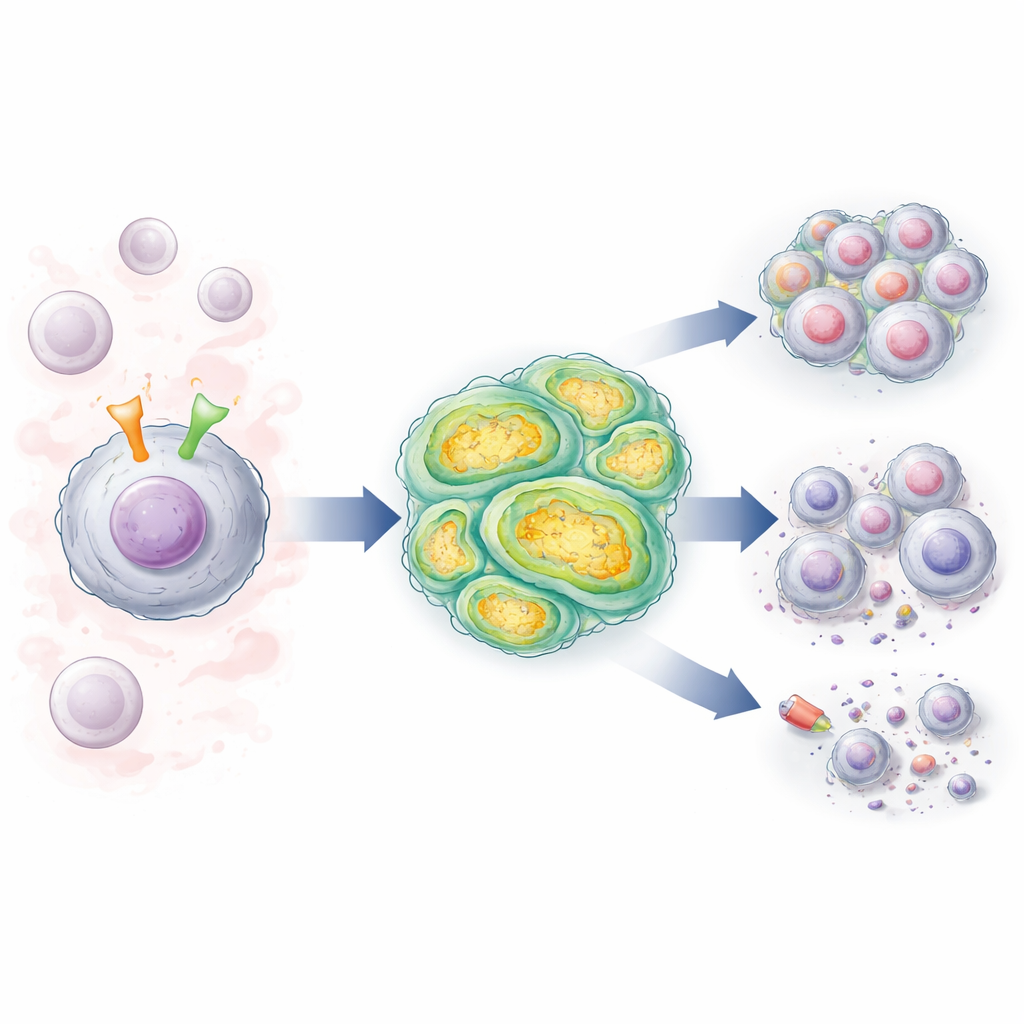
Twee celschakkelaars die met elkaar communiceren
CLL-cellen dragen een oppervlakte-antenne, de B-celreceptor (BCR), die signalen in bloed en lymfeklieren waarneemt en de cellen aanzet tot overleving en deling. Veel patiënten hebben ook veranderingen in het gen NOTCH1, dat een ander oppervlakte-eiwit codeert dat, wanneer geactiveerd, krachtige groeigoedkeuringen en overlevingssignalen naar de celkern stuurt. De auteurs bestudeerden CLL-cellen van patiënten waarvan de BCR een hoog-risico, “onveranderd” (unmutated) patroon heeft, en vergeleken cellen met normale NOTCH1 met cellen met NOTCH1-mutaties. Ze vonden dat wanneer de BCR werd gestimuleerd, dit de NOTCH1-activiteit sterk versterkte, vooral in de gemuteerde cellen, en daarmee een feedbacklus in stand houdt die het leukemische signaal aanhoudt.
Herschakelen van hoe leukemiecellen energie produceren
Genexpressieprofielen en directe metingen van energieverbruik toonden aan dat NOTCH1-gemuteerde CLL-cellen hun energiecentrales—mitochondriën—veel intensiever laten draaien dan cellen zonder de mutatie. Deze cellen verbrandden meer brandstof via zowel glycolyse (suikerafbraak) als mitochondriale ademhaling, produceerden meer cellulaire "batterij"-moleculen (ATP) en genereerden meer reactieve zuurstofsoorten; allemaal tekenen van een opgevoerde motor. Microscopen lieten zien dat NOTCH1-gemuteerde cellen meer en grotere mitochondriën hadden die dichte netwerken vormden, ondersteund door extra mitochondriaal DNA. Wanneer de BCR werd geactiveerd, nam deze al hoge metabole activiteit nog verder toe, wat aangeeft dat signalen van buiten de cel een reeds voorbelast energiesysteem in overdrive kunnen zetten.
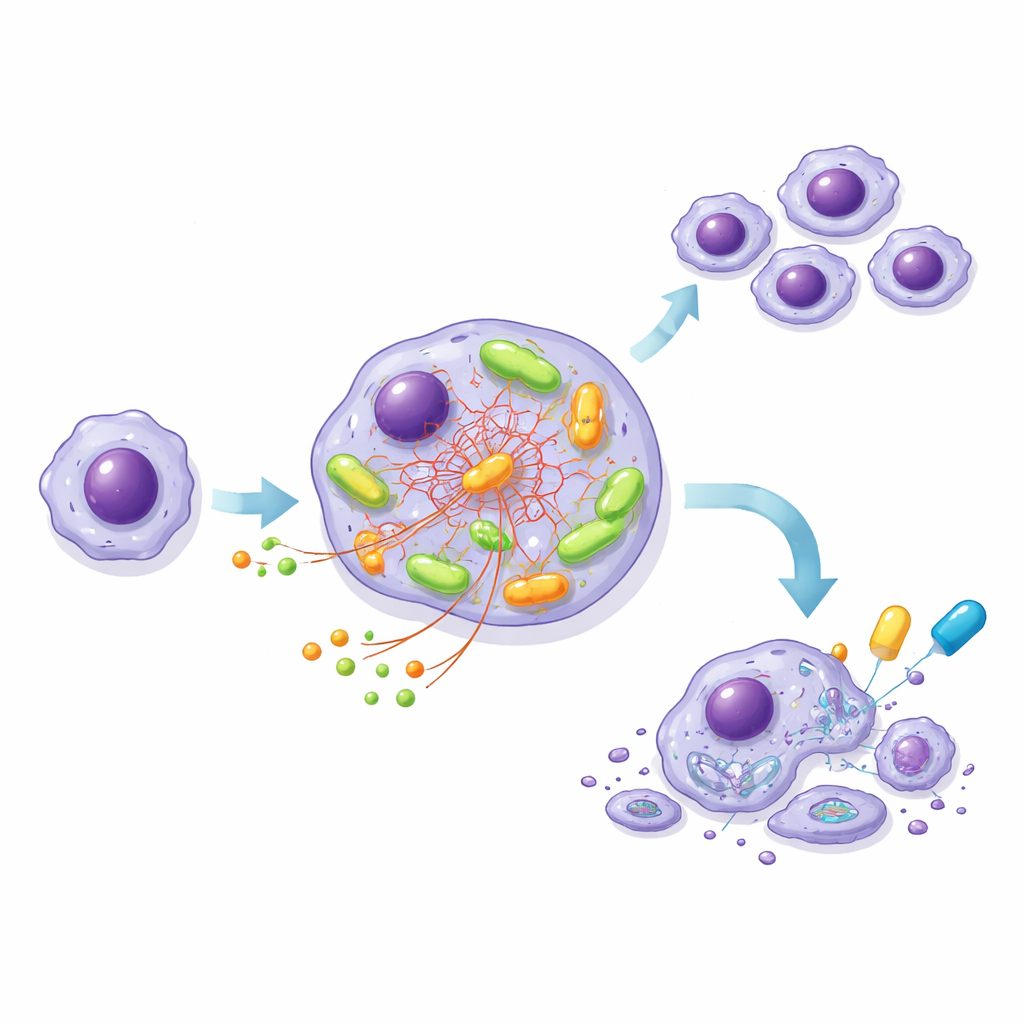
Een modelcelijn bouwen om de motor te analyseren
Aangezien patiënt-CLL-cellen zich niet gemakkelijk in het laboratorium vermenigvuldigen, creëerde het team een leukemie-achtige celijn, MEC-1, in twee versies: één met normale NOTCH1 en één met een getruncateerde, overactieve NOTCH1, beide met dezelfde hoog-risico BCR. Dit gecontroleerde systeem weerspiegelde wat in patiëntmonsters werd gezien. De gemuteerde cellen verbruikten meer glucose, produceerden meer ATP en hadden een hoger zuurstofverbruik dan hun normale tegenhangers, vooral na BCR-activatie. Gedetailleerde tracer-experimenten met gelabelde voedingsstoffen toonden aan dat glucose in gemuteerde cellen werd omgeleid naar bouwstenen en beschermende moleculen, terwijl een andere voedingsstof, glutamine, de belangrijkste brandstof werd die de centrale energieketen in de mitochondriën voedde.
Een hoofdregelaar van mitochondriën en een brandstofverslaving
Om te begrijpen hoe NOTCH1 mitochondriën herprogrammeert, onderzochten de onderzoekers het chromatine-landschap—de manier waarop DNA is verpakt en gemarkeerd voor activiteit. Ze vonden dat in gemuteerde cellen de actieve vorm van NOTCH1 direct nabij een gen genaamd TFAM aanhechtte, een sleutelregelaar van mitochondriaal DNA en functie, en de expressie ervan verhoogde. Het blokkeren van TFAM verminderde de mitochondriale massa alleen in NOTCH1-gemuteerde cellen en leidde tot hun afsterven, wat aantoont dat deze cellen uniek afhankelijk zijn van dit mitochondriale programma. Functioneel groeiden de gemuteerde cellen sneller dan normale cellen in gemengde culturen. Wanneer het team de opname van glutamine in cellen blokkeerde, verdween het groeivoordeel van de gemuteerde cellen, en werden zowel de geconstrueerde cellen als primaire NOTCH1-gemuteerde CLL-cellen veel kwetsbaarder, wat een sterke "verslaving" aan glutamine blootlegde.
Een zwakte omzetten in een behandelstrategie
De studie testte vervolgens of deze brandstofafhankelijkheid bestaande medicijnen effectiever kon maken. Venetoclax, een doelgericht middel dat CLL-cellen doodt door mitochondriaal geprogrammeerde celdood te induceren, was effectiever tegen NOTCH1-gemuteerde cellen dan tegen normale cellen. Opvallend was dat de combinatie van een blokkade van glutaminetransport met venetoclax de leukemieceldood sterk verhoogde, en deze synergie was specifiek voor NOTCH1-gemuteerde cellen. Zelfs een model dat normaal resistent is door extra genetische schade werd gevoelig onder deze combinatie. In eenvoudige bewoordingen: de mutatierijke leukemiecellen overleven door hun mitochondriën op glutamine hoog te laten draaien; wanneer die brandstoftoevoer wordt afgesneden en tegelijk een pro-doodsignaal wordt toegediend, stort hun energiesysteem in en kunnen de cellen niet herstellen.
Wat dit betekent voor de toekomst
Samengevat tonen de auteurs aan dat een genetische verandering in NOTCH1, in samenwerking met signalen via de B-celreceptor, bepaalde CLL-cellen aanzet tot het bouwen van grotere, actievere energiecentrales en tot een sterke afhankelijkheid van het aminozuur glutamine voor energie en groei. Diezelfde afhankelijkheid maakt ze ongewoon kwetsbaar wanneer glutaminegebruik wordt geblokkeerd, zeker in combinatie met een middel als venetoclax dat de mitochondriën aanvalt. Hoewel aanvullend werk in patiëntnabije modellen nodig is, biedt deze metabole kwetsbaarheid een veelbelovende route om behandelingen te personaliseren voor mensen met CLL die NOTCH1-mutaties dragen, met de mogelijkheid om resultaten te verbeteren door standaard doelgerichte middelen te combineren met zorgvuldig gekozen metabole therapieën.
Bronvermelding: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Trefwoorden: chronische lymfatische leukemie, NOTCH1-mutatie, kankermetabolisme, mitochondriën, glutamaatafhankelijkheid