Clear Sky Science · fr
Coopération fonctionnelle entre le récepteur des cellules B et NOTCH1 dans la régulation du reprogrammation métabolique dans la leucémie lymphoïde chronique
Pourquoi cela importe pour les patients et les familles
La leucémie lymphoïde chronique (LLC) est la leucémie la plus fréquente chez l’adulte ; si de nombreuses personnes vivent avec la maladie pendant des années, certains cas deviennent agressifs et difficiles à traiter. Cette étude pose une question simple mais cruciale : qu’est-ce qui fait que certaines cellules de LLC prolifèrent plus vite et résistent aux traitements, et peut-on exploiter cette faiblesse contre elles ? Les chercheurs dévoilent comment deux interrupteurs clés à la surface des cellules leucémiques s’associent pour remodeler l’utilisation d’énergie des cellules, créant à la fois un avantage de croissance et un talon d’Achille métabolique potentiellement exploitable cliniquement.
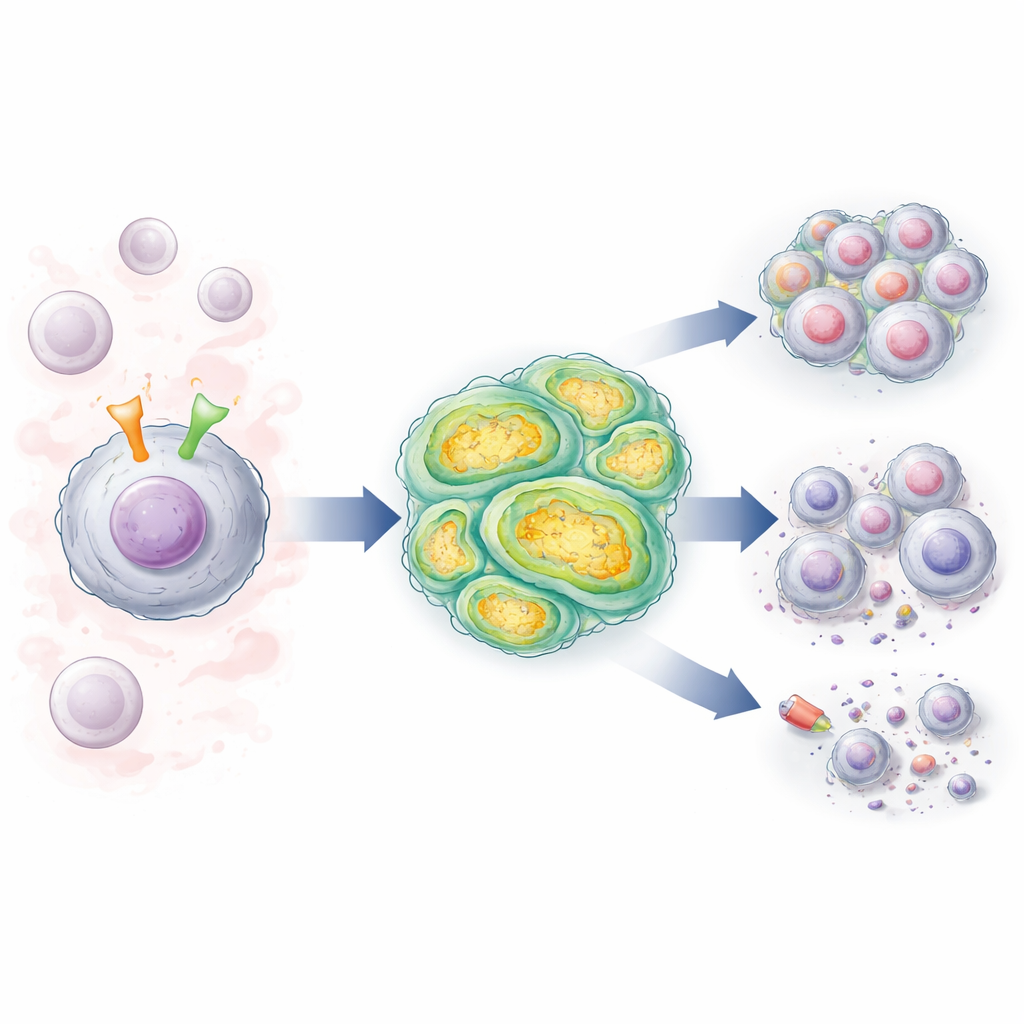
Deux interrupteurs cellulaires qui communiquent
Les cellules de LLC portent une antenne de surface appelée récepteur des cellules B (BCR), qui détecte des signaux dans le sang et les ganglions lymphatiques et stimule la survie et la division des cellules. Chez de nombreux patients, des altérations sont également présentes dans un gène nommé NOTCH1, qui code pour une autre molécule de surface qui, une fois activée, envoie des signaux puissants de croissance et de survie dans le noyau. Les auteurs ont étudié des cellules de LLC de patients dont les BCR partageaient un profil « non muté » à haut risque, et ont comparé des cellules avec un NOTCH1 normal à celles portant des mutations de NOTCH1. Ils ont constaté que lorsque le BCR était stimulé, il renforçait fortement l’activité de NOTCH1, en particulier dans les cellules mutées, alimentant une boucle de rétroaction qui maintient l’activation des voies leucémiques.
Reconfiguration de la production d’énergie des cellules leucémiques
Des cartographies de l’activité génique et des mesures directes de l’utilisation énergétique montrent que les cellules de LLC porteuses d’une mutation de NOTCH1 sollicitent beaucoup plus leurs centrales—les mitochondries—que les cellules sans la mutation. Ces cellules brûlaient davantage de carburant via la glycolyse (dégradation du sucre) et la respiration mitochondriale, produisaient plus de molécules « batterie » (ATP) et généraient davantage d’espèces réactives de l’oxygène, autant d’indicateurs d’un moteur suractivé. La microscopie a révélé que les cellules mutées avaient plus de mitochondries, plus volumineuses et organisées en réseaux denses, soutenues par un surplus d’ADN mitochondrial. Lorsque le BCR était activé, cette activité métabolique déjà élevée augmentait encore, indiquant que des signaux externes peuvent propulser un système énergétique déjà amorcé en surrégime.
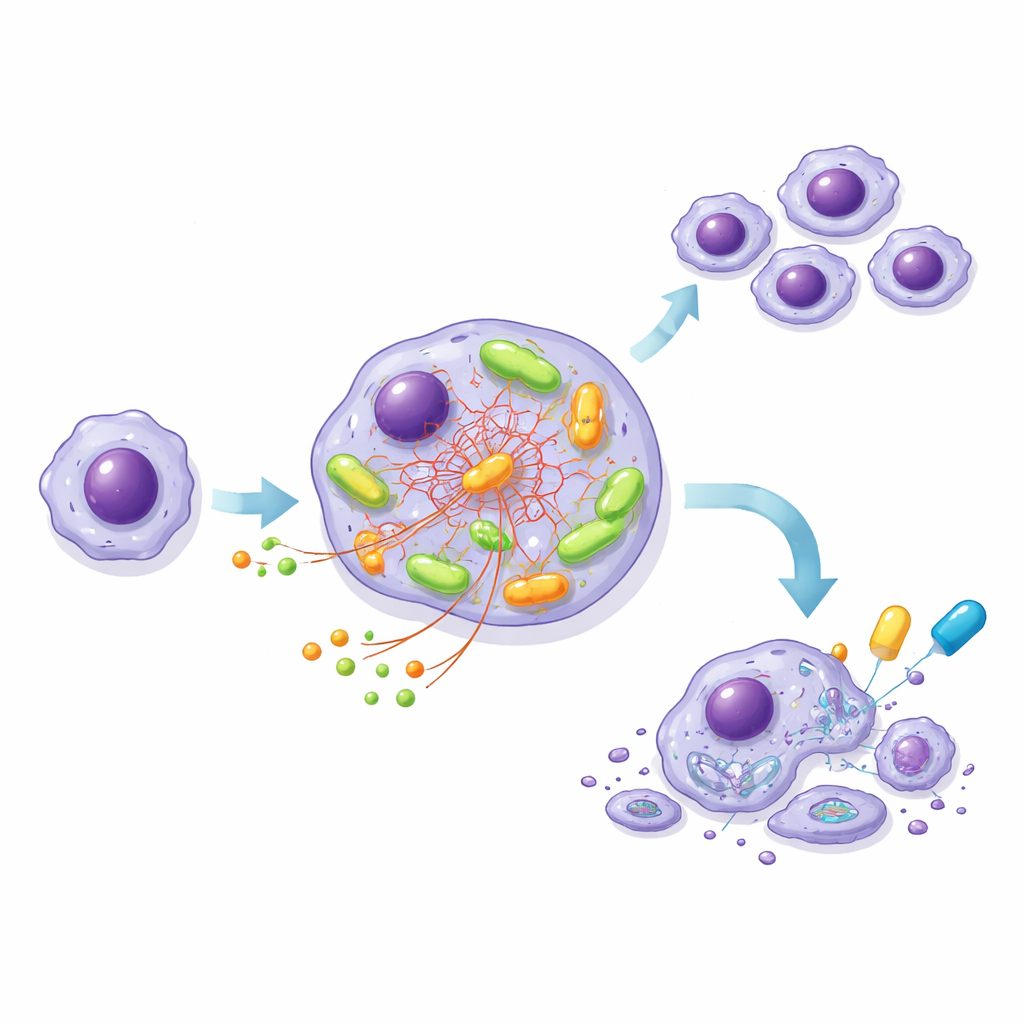
Construction d’une lignée cellulaire modèle pour disséquer le moteur
Parce que les cellules de LLC issues de patients ne prolifèrent pas facilement en laboratoire, l’équipe a modifié une lignée cellulaire de type leucémique, MEC-1, en deux versions : l’une avec NOTCH1 normal et l’autre avec une forme tronquée et hyperactive de NOTCH1, les deux portant le même BCR à haut risque. Ce système contrôlé a reproduit les observations faites sur les échantillons de patients. Les cellules mutantes consommaient plus de glucose, produisaient plus d’ATP et présentaient une consommation d’oxygène plus élevée que leurs homologues normales, surtout après activation du BCR. Des expériences de traçage détaillées utilisant des nutriments marqués ont montré que, dans les cellules mutantes, le glucose était détourné vers la synthèse de composants et de molécules protectrices, tandis qu’un autre nutriment, la glutamine, devenait le principal carburant alimentant le cycle énergétique central au sein des mitochondries.
Un contrôleur maître des mitochondries et une addiction au carburant
Pour comprendre comment NOTCH1 reconfigure les mitochondries, les chercheurs ont examiné le paysage de la chromatine—la manière dont l’ADN est emballé et marqué pour l’activité. Ils ont découvert que, dans les cellules mutées, la forme active de NOTCH1 se liait directement à proximité d’un gène appelé TFAM, un régulateur clé de l’ADN mitochondrial et de la fonction mitochondriale, et l’activait. Bloquer TFAM réduisait la masse mitochondriale uniquement dans les cellules porteuses de la mutation NOTCH1 et déclenchait leur mort, montrant que ces cellules sont particulièrement dépendantes de ce programme mitochondrial. Fonctionnellement, les cellules mutantes proliféraient plus vite que les cellules normales en cultures mixtes. Lorsque l’équipe a bloqué l’entrée de la glutamine dans les cellules, l’avantage de croissance des cellules mutantes a disparu, et aussi bien les cellules modifiées que les cellules primaires de LLC mutées pour NOTCH1 sont devenues beaucoup plus vulnérables, révélant une forte « addiction » à la glutamine.
Transformer une faiblesse en stratégie thérapeutique
L’étude a ensuite testé si cette dépendance au carburant pouvait améliorer l’efficacité de médicaments existants. Le venetoclax, un médicament ciblé qui tue les cellules de LLC en déclenchant la mort mitochondriale, était plus efficace contre les cellules porteuses de la mutation NOTCH1 que contre les cellules normales. De façon frappante, l’association d’un blocage du transport de la glutamine avec le venetoclax augmentait fortement la mortalité des cellules leucémiques, et cette synergie était spécifique aux cellules mutées pour NOTCH1. Même un modèle généralement résistant aux médicaments, porteur de dommages génétiques supplémentaires, devenait sensible sous cette combinaison. En termes simples, les cellules leucémiques riches en mutations survivent en sollicitant fortement leurs mitochondries avec la glutamine ; lorsque cette voie d’alimentation est coupée et qu’un signal pro-apoptotique est appliqué en même temps, leur système énergétique s’effondre et les cellules ne peuvent pas se rétablir.
Ce que cela signifie pour l’avenir
En clair, les auteurs montrent qu’une altération génétique de NOTCH1, en coopération avec les signaux reçus via le récepteur des cellules B, pousse certaines cellules de LLC à construire des centrales énergétiques plus grandes et plus actives et à dépendre fortement de l’acide aminé glutamine pour leur énergie et leur croissance. Cette même dépendance les rend exceptionnellement fragiles lorsque l’utilisation de la glutamine est bloquée, en particulier si elle est combinée à un médicament comme le venetoclax qui attaque les mitochondries. Bien que des travaux supplémentaires dans des modèles proches du patient soient nécessaires, cette vulnérabilité métabolique offre une piste prometteuse pour personnaliser le traitement des personnes dont la LLC porte des mutations de NOTCH1, améliorant potentiellement les résultats en associant des thérapies métaboliques ciblées à des médicaments standard.»}
Citation: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Mots-clés: leucémie lymphoïde chronique, mutation NOTCH1, métabolisme du cancer, mitochondries, dépendance au glutamine