Clear Sky Science · pt
Cooperação funcional entre o receptor de células B e NOTCH1 na regulação do reprogramamento metabólico na leucemia linfocítica crônica
Por que isto importa para pacientes e suas famílias
A leucemia linfocítica crônica (LLC) é a leucemia adulta mais comum e, embora muitas pessoas convivam com ela por anos, alguns casos tornam-se agressivos e difíceis de tratar. Este estudo faz uma pergunta simples, porém crucial: o que faz algumas células da LLC crescerem mais rápido e resistirem ao tratamento, e essa fraqueza pode ser explorada contra elas? Os pesquisadores descrevem como dois interruptores chave nas células leucêmicas atuam em conjunto para reformular o uso de energia das células, criando tanto uma vantagem de crescimento quanto um calcanhar de Aquiles metabólico que os médicos podem vir a direcionar.
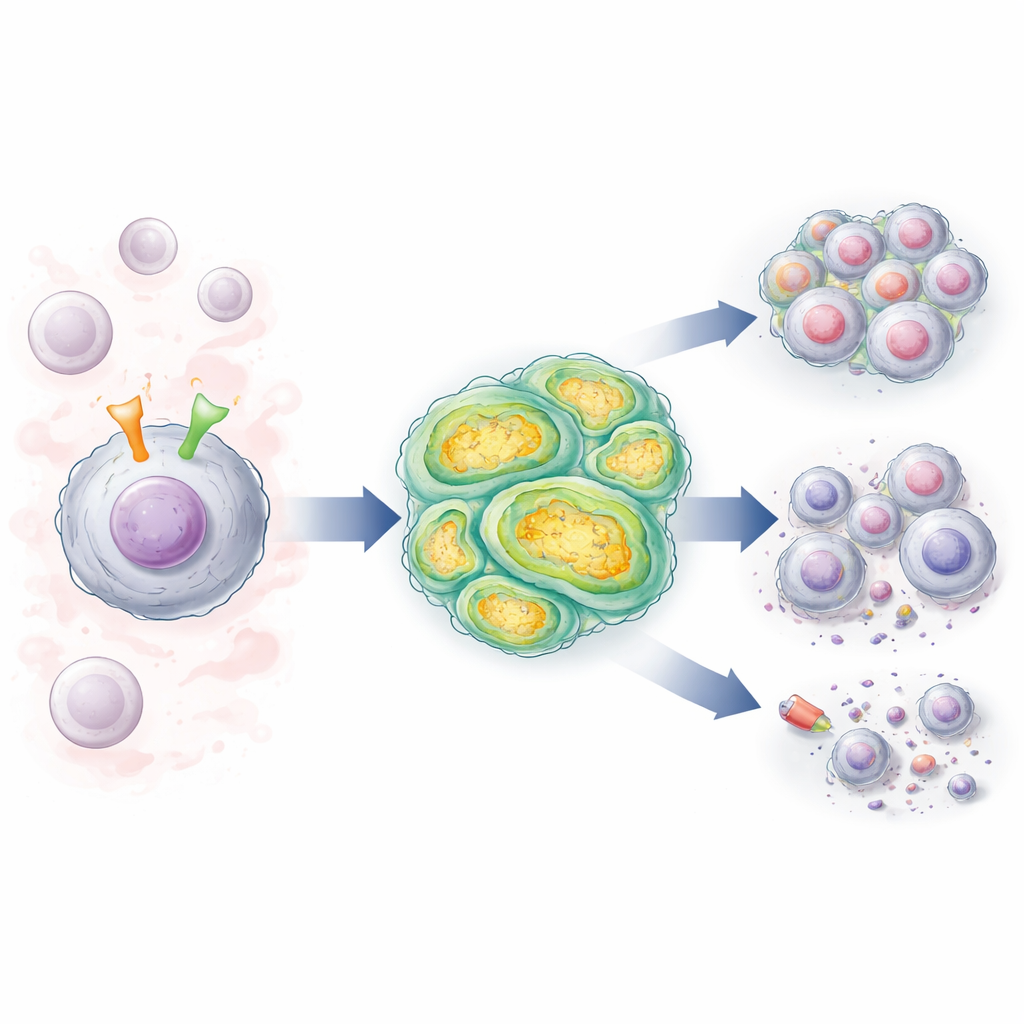
Dois interruptores celulares que conversam entre si
As células da LLC carregam uma antena de superfície chamada receptor de células B (BCR), que detecta sinais no sangue e nos linfonodos e impulsiona as células a sobreviver e se dividir. Muitos pacientes também apresentam alterações em um gene chamado NOTCH1, que codifica outra molécula de superfície que, quando ativada, envia sinais poderosos de crescimento e sobrevivência ao núcleo. Os autores estudaram células de LLC de pacientes cujos BCRs compartilhavam um padrão de alto risco “não mutado”, e compararam células com NOTCH1 normal às com mutações em NOTCH1. Eles descobriram que, quando o BCR era estimulado, ele aumentava fortemente a atividade de NOTCH1, especialmente nas células mutadas, reforçando um ciclo de realimentação que mantém a sinalização leucêmica ligada.
Reconectando como as células leucêmicas produzem energia
Mapeamentos de atividade gênica e medições diretas do uso de energia mostraram que células de LLC com mutação em NOTCH1 fazem suas usinas — as mitocôndrias — funcionarem muito mais intensamente do que células sem a mutação. Essas células queimavam mais combustível tanto pela glicólise (quebra de açúcares) quanto pela respiração mitocondrial, produziam mais moléculas “baterias” (ATP) e geravam mais espécies reativas de oxigênio, todos sinais de um motor acelerado. A microscopia revelou que células com mutação em NOTCH1 tinham mitocôndrias mais numerosas e maiores formando redes densas, sustentadas por DNA mitocondrial extra. Quando o BCR era ativado, essa já alta atividade metabólica aumentava ainda mais, indicando que sinais externos podem empurrar um sistema energético já preparado a entrar em sobredrive.
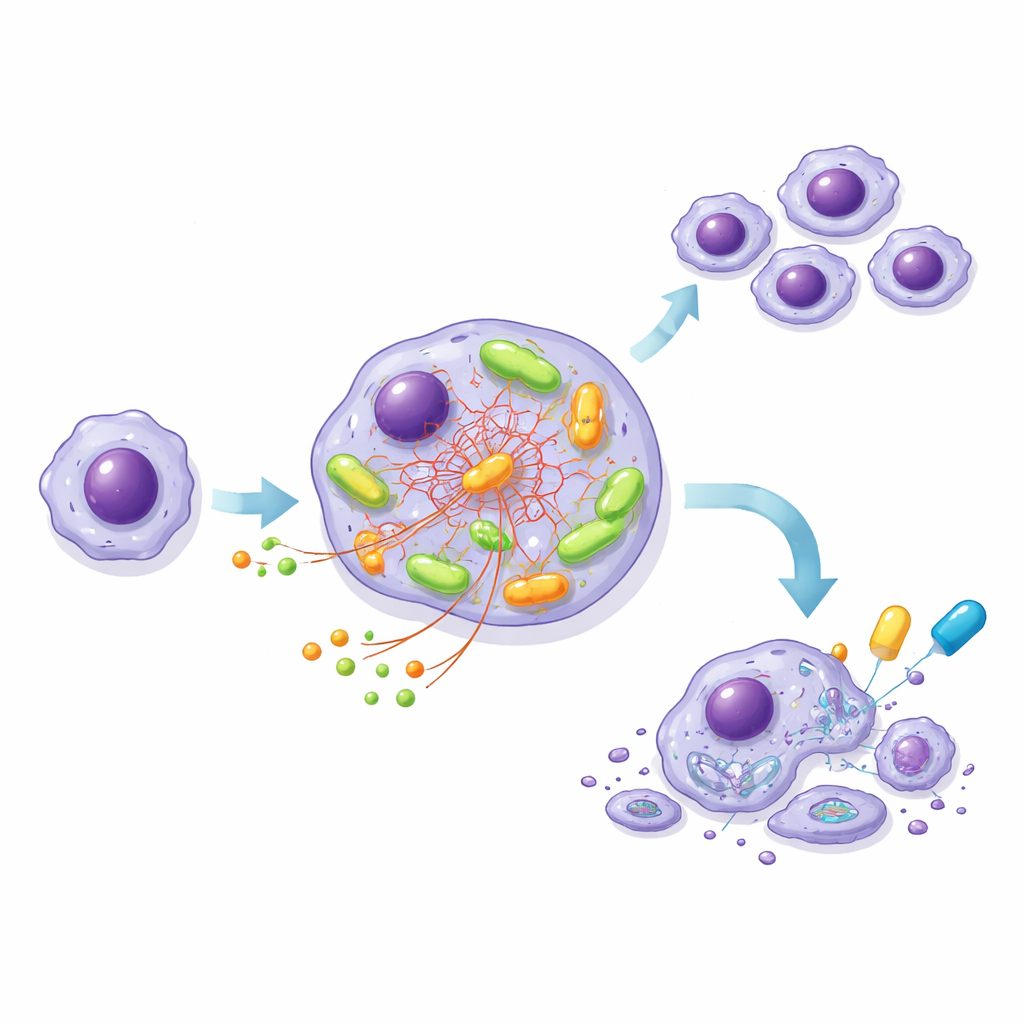
Construindo uma linhagem celular modelo para dissecar o motor
Como células de LLC de pacientes não crescem facilmente em laboratório, a equipe engenheirou uma linha celular tipo leucemia, MEC-1, em duas versões: uma com NOTCH1 normal e outra com uma forma truncada e hiperativa de NOTCH1, ambas portando o mesmo BCR de alto risco. Esse sistema controlado espelhou o observado nas amostras de pacientes. As células mutantes consumiram mais glicose, produziram mais ATP e apresentaram maior consumo de oxigênio do que as contrapartes normais, especialmente após ativação do BCR. Experimentos detalhados de rastreamento usando nutrientes marcados mostraram que, nas células mutantes, a glicose era desviada para blocos de construção e moléculas protetoras, enquanto outro nutriente, a glutamina, tornava-se o combustível principal alimentando o ciclo energético central dentro das mitocôndrias.
Um controlador mestre das mitocôndrias e uma dependência de combustível
Para entender como NOTCH1 remodela as mitocôndrias, os pesquisadores examinaram o paisagismo da cromatina — a forma como o DNA é empacotado e marcado para atividade. Eles descobriram que, nas células mutantes, a forma ativa de NOTCH1 ligava-se diretamente perto de um gene chamado TFAM, um controlador-chave do DNA mitocondrial e da função mitocondrial, e o ativava. Bloquear o TFAM reduziu a massa mitocondrial apenas nas células com mutação em NOTCH1 e desencadeou sua morte, mostrando que essas células são singularmente dependentes desse programa mitocondrial. Funcionalmente, as células mutantes cresceram mais rápido do que as normais em culturas mistas. Quando a equipe bloqueou a entrada de glutamina nas células, a vantagem de crescimento das células mutantes desapareceu, e tanto as células manipuladas quanto as células primárias de LLC com mutação em NOTCH1 ficaram muito mais vulneráveis, revelando uma forte “dependência” de glutamina.
Transformando uma fraqueza em estratégia de tratamento
O estudo testou então se essa dependência de combustível poderia melhorar a eficácia de medicamentos existentes. Venetoclax, um fármaco direcionado que mata células de LLC ao desencadear a morte mitocondrial, foi mais eficaz contra células com mutação em NOTCH1 do que contra as normais. De forma marcante, a combinação do bloqueio do transporte de glutamina com venetoclax aumentou fortemente a morte das células leucêmicas, e essa sinergia foi específica para células com mutação em NOTCH1. Mesmo um modelo tipicamente resistente a drogas, carregando danos genéticos adicionais, tornou-se sensível sob essa combinação. Em termos cotidianos, as células leucêmicas com muitas mutações sobrevivem mantendo suas mitocôndrias aceleradas usando glutamina; quando essa linha de combustível é cortada e um sinal pró-morte é aplicado ao mesmo tempo, seu sistema de energia colapsa e as células não se recuperam.
O que isso significa para o futuro
Em linguagem direta, os autores mostram que uma alteração genética em NOTCH1, atuando em conjunto com sinais recebidos pelo receptor de células B, empurra certas células de LLC a construírem usinas energéticas maiores e mais ativas e a dependerem fortemente do aminoácido glutamina para energia e crescimento. Essa mesma dependência os torna incomumente frágeis quando o uso de glutamina é bloqueado, especialmente se combinado com um fármaco como o venetoclax que ataca as mitocôndrias. Embora sejam necessários mais estudos em modelos que reproduzam fielmente o contexto dos pacientes, essa vulnerabilidade metabólica oferece uma rota promissora para personalizar o tratamento de pessoas cuja LLC carrega mutações em NOTCH1, potencialmente melhorando os desfechos ao combinar drogas alvo padrão com terapias metabólicas cuidadosamente escolhidas.
Citação: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Palavras-chave: leucemia linfocítica crônica, mutação em NOTCH1, metabolismo do câncer, mitocôndrias, dependência de glutamina