Clear Sky Science · es
Cooperación funcional entre el receptor de células B y NOTCH1 en la regulación del reprogramamiento metabólico en la leucemia linfocítica crónica
Por qué importa esto para pacientes y familias
La leucemia linfocítica crónica (LLC) es la leucemia adulta más frecuente y, aunque muchas personas conviven con ella durante años, algunos casos se vuelven agresivos y difíciles de tratar. Este estudio plantea una pregunta sencilla pero crucial: ¿qué hace que algunas células de LLC crezcan más rápido y resistan el tratamiento, y se puede convertir esa debilidad en un punto vulnerable? Los investigadores revelan cómo dos interruptores claves en las células leucémicas colaboran para rehacer el uso de la energía de las células, creando tanto una ventaja de crecimiento como un talón de Aquiles metabólico que los médicos podrían aprovechar.
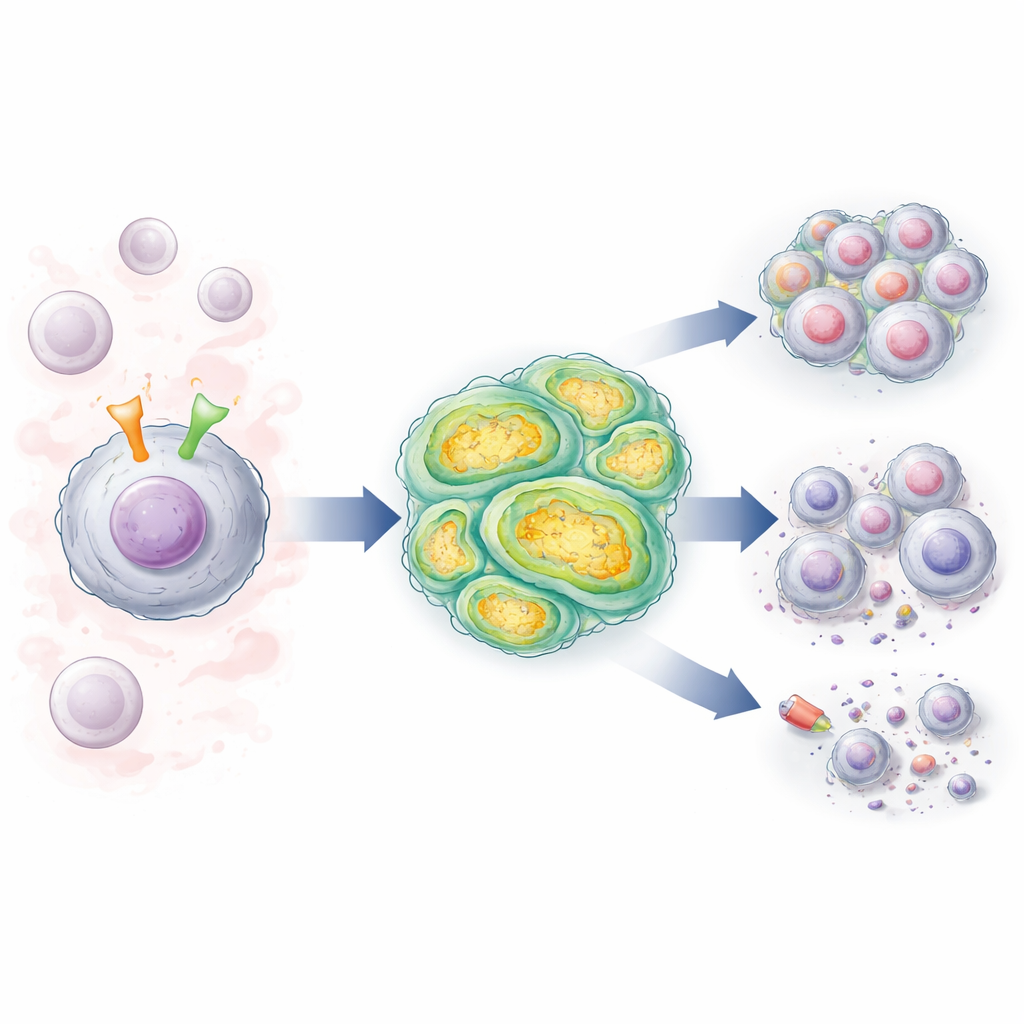
Dos interruptores celulares que se comunican
Las células de LLC llevan una antena en la superficie llamada receptor de células B (BCR), que detecta señales en la sangre y en los ganglios linfáticos y empuja a las células a sobrevivir y dividirse. Muchos pacientes también presentan alteraciones en un gen llamado NOTCH1, que codifica otra molécula de superficie que, cuando se activa, envía potentes señales de crecimiento y supervivencia al núcleo. Los autores estudiaron células de LLC de pacientes cuyos BCR compartían un patrón de alto riesgo «no mutado», y compararon células con NOTCH1 normal frente a células con mutaciones en NOTCH1. Encontraron que cuando se estimulaba el BCR, se aumentaba fuertemente la actividad de NOTCH1, especialmente en las células mutadas, reforzando un circuito de retroalimentación que mantiene la señalización leucémica activada.
Reconfiguración de cómo las células leucémicas generan energía
Los mapas de actividad génica y las mediciones directas del uso de energía mostraron que las células de LLC con mutación en NOTCH1 hacen trabajar mucho más sus centrales eléctricas —las mitocondrias— que las células sin la mutación. Estas células quemaban más combustible tanto por glicólisis (descomposición de azúcares) como por respiración mitocondrial, producían más moléculas “batería” (ATP) y generaban más especies reactivas de oxígeno, todas señales de un motor acelerado. La microscopía reveló que las células con NOTCH1 mutado tenían más mitocondrias de mayor tamaño formando redes densas, apoyadas por un exceso de ADN mitocondrial. Cuando se activaba el BCR, esta ya alta actividad metabólica aumentaba aún más, lo que indica que las señales externas pueden empujar a un sistema energético ya cebado a un estado de sobreexcitamiento.
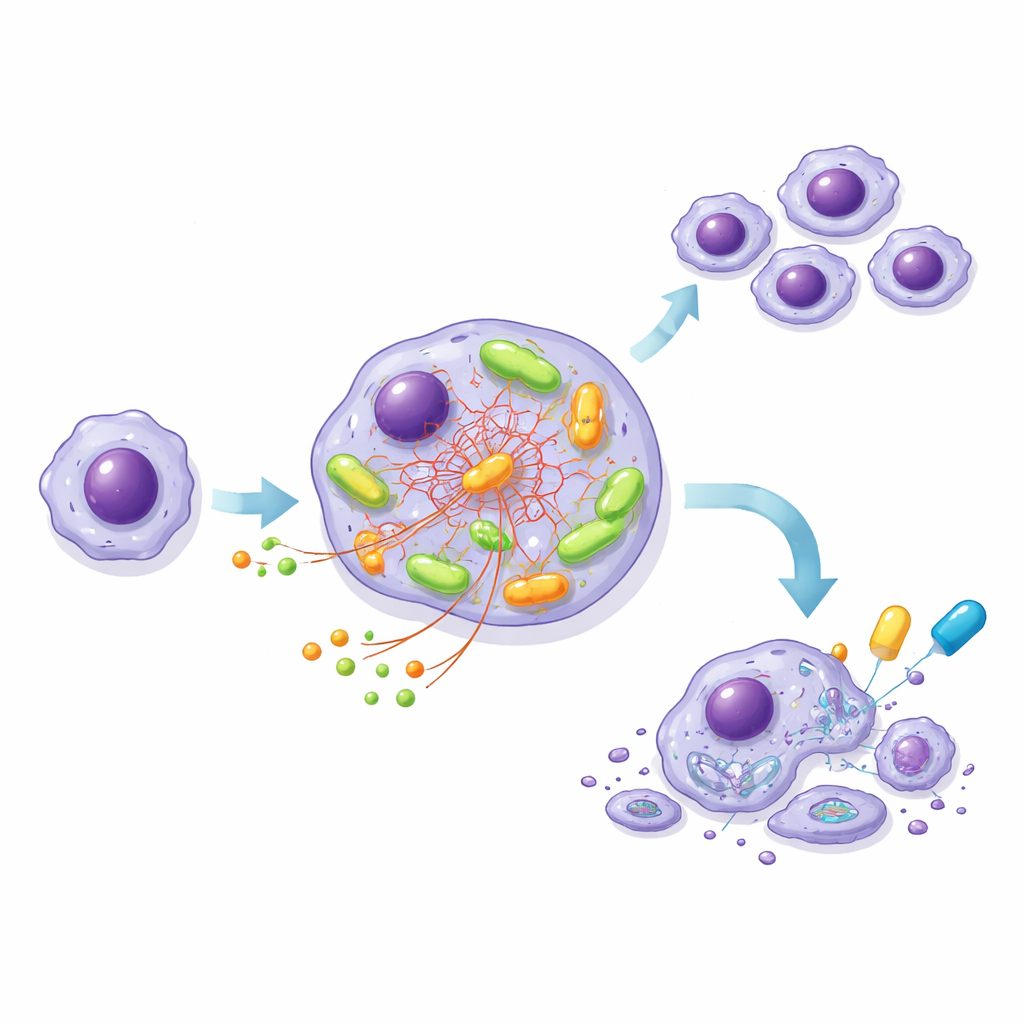
Construcción de una línea celular modelo para diseccionar el motor
Dado que las células de LLC de pacientes no proliferan con facilidad en el laboratorio, el equipo diseñó una línea celular tipo leucemia, MEC-1, en dos versiones: una con NOTCH1 normal y otra con un NOTCH1 truncado y sobreactivado, ambas con el mismo BCR de alto riesgo. Este sistema controlado reflejó lo observado en las muestras de pacientes. Las células mutantes consumieron más glucosa, produjeron más ATP y presentaron mayor consumo de oxígeno que sus contrapartes normales, especialmente tras la activación del BCR. Experimentos de trazado detallados con nutrientes marcados mostraron que, en las células mutantes, la glucosa se desviaba hacia la síntesis de bloques de construcción y moléculas protectoras, mientras que otro nutriente, la glutamina, se convertía en el combustible principal que alimenta el ciclo energético central dentro de las mitocondrias.
Un regulador maestro de las mitocondrias y una adicción al combustible
Para entender cómo NOTCH1 remodela las mitocondrias, los investigadores examinaron el paisaje de la cromatina —la forma en que el ADN está empaquetado y marcado para la actividad. Encontraron que en las células mutantes, la forma activa de NOTCH1 se unía directamente cerca de un gen llamado TFAM, un controlador clave del ADN mitocondrial y de la función mitocondrial, y lo activaba. Bloquear TFAM redujo la masa mitocondrial solo en las células con NOTCH1 mutado y desencadenó su muerte, mostrando que estas células dependen de forma única de este programa mitocondrial. Funcionalmente, las células mutantes crecían más rápido que las normales en cultivos mixtos. Cuando el equipo bloqueó la entrada de glutamina en las células, la ventaja de crecimiento de las mutantes desapareció, y tanto las células diseñadas como las células primarias de LLC con NOTCH1 mutado se volvieron mucho más vulnerables, revelando una fuerte «adicción» a la glutamina.
Convertir una debilidad en una estrategia terapéutica
El estudio probó luego si esta dependencia del combustible podía potenciar fármacos existentes. Venetoclax, un fármaco dirigido que mata células de LLC al activar la muerte mitocondrial, fue más eficaz contra células con NOTCH1 mutado que contra las normales. De forma notable, la combinación de bloqueo del transporte de glutamina con venetoclax aumentó drásticamente la muerte de las células leucémicas, y esta sinergia fue específica de las células con NOTCH1 mutado. Incluso un modelo típicamente resistente a fármacos que portaba daños genéticos adicionales se volvió sensible con esta combinación. En términos sencillos, las células leucémicas con muchas mutaciones sobreviven manteniendo sus mitocondrias trabajando a alta temperatura con glutamina; cuando se corta ese suministro de combustible y al mismo tiempo se aplica una señal pro-muerte, su sistema energético colapsa y las células no se recuperan.
Qué significa esto de cara al futuro
En lenguaje llano, los autores muestran que un cambio genético en NOTCH1, en conjunto con las señales recibidas a través del receptor de células B, empuja a ciertas células de LLC a construir centrales eléctricas más grandes y activas y a depender en gran medida del aminoácido glutamina para obtener energía y crecer. Esa misma dependencia las hace inusualmente frágiles cuando se bloquea el uso de glutamina, especialmente si se combina con un fármaco como venetoclax que ataca las mitocondrias. Aunque se necesitan más estudios en contextos clínicos realistas, esta vulnerabilidad metabólica ofrece una vía prometedora para personalizar el tratamiento de personas cuya LLC porta mutaciones en NOTCH1, mejorando potencialmente los resultados al combinar fármacos dirigidos estándar con terapias metabólicas seleccionadas.
Cita: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Palabras clave: leucemia linfocítica crónica, mutación NOTCH1, metabolismo del cáncer, mitocondrias, dependencia de la glutamina