Clear Sky Science · it
Cooperazione funzionale tra il recettore delle cellule B e NOTCH1 nella regolazione del riprogrammamento metabolico nella leucemia linfatica cronica
Perché questo è importante per pazienti e famiglie
La leucemia linfatica cronica (LLC) è la forma di leucemia più comune negli adulti e, sebbene molte persone convivano con la malattia per anni, in alcuni casi la malattia diventa aggressiva e difficile da trattare. Questo studio pone una domanda semplice ma cruciale: cosa rende alcune cellule di LLC più proliferative e resistenti alle terapie, e può questa vulnerabilità essere sfruttata contro di loro? I ricercatori svelano come due interruttori chiave sulle cellule leucemiche collaborino per riorganizzare l’uso energetico delle cellule, creando sia un vantaggio proliferativo sia un’achillea metabolica nascosta che i clinici potrebbero essere in grado di colpire.
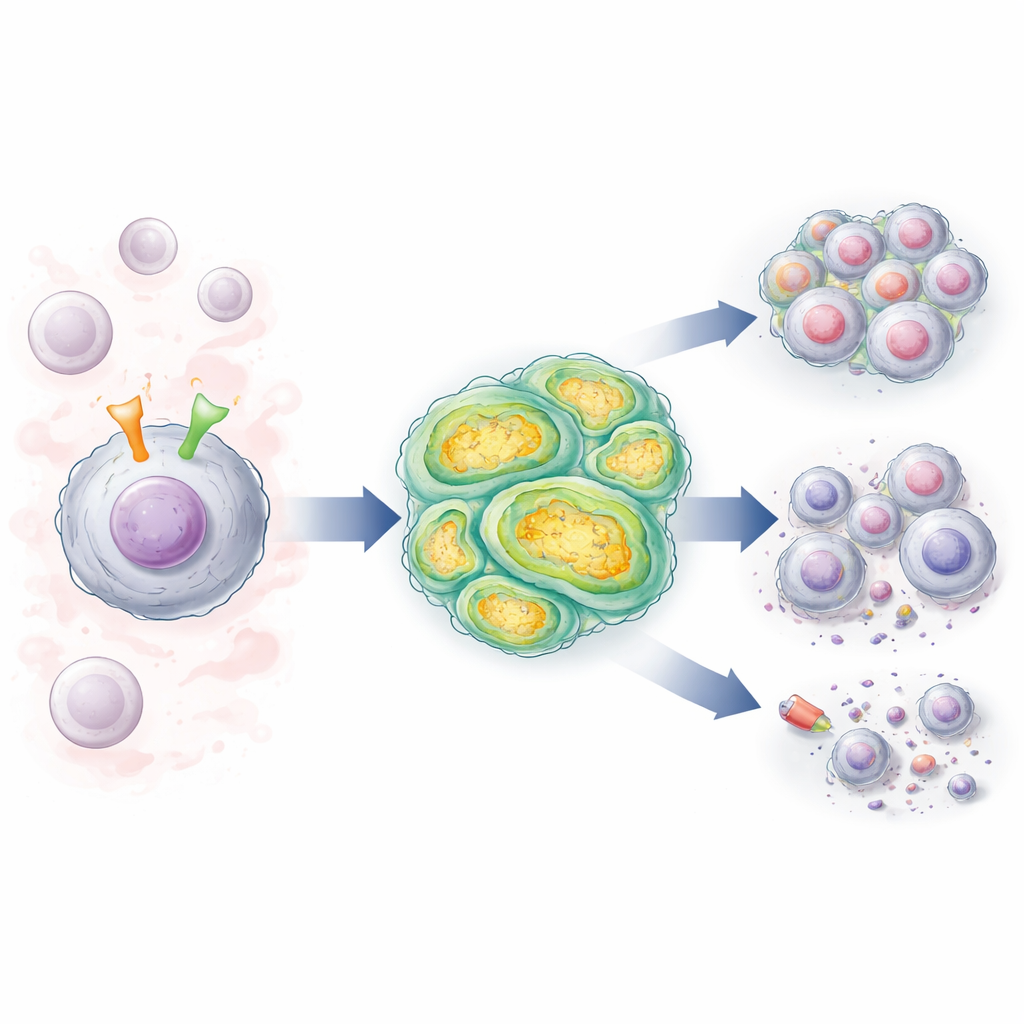
Due interruttori cellulari che comunicano tra loro
Le cellule di LLC portano un’antenna di superficie chiamata recettore delle cellule B (BCR), che rileva segnali nel sangue e nei linfonodi e spinge le cellule a sopravvivere e dividersi. Molti pazienti presentano inoltre alterazioni in un gene chiamato NOTCH1, che codifica per un’altra molecola di superficie che, una volta attivata, invia potenti segnali di crescita e sopravvivenza al nucleo. Gli autori hanno studiato cellule di LLC di pazienti i cui BCR condividevano un profilo ad alto rischio, “non mutato”, e hanno confrontato cellule con NOTCH1 normale e con NOTCH1 mutato. Hanno trovato che quando il BCR veniva stimolato, aumentava fortemente l’attività di NOTCH1, specialmente nelle cellule mutate, rafforzando un circuito di feedback che mantiene acceso il segnale leucemico.
Rimodellamento del modo in cui le cellule leucemiche producono energia
Mappe dell’attività genica e misure dirette dell’uso energetico hanno mostrato che le cellule di LLC con NOTCH1 mutato fanno funzionare i loro motori—i mitocondri—molto più intensamente rispetto alle cellule senza la mutazione. Queste cellule bruciavano più combustibile sia tramite la glicolisi (degradazione degli zuccheri) sia tramite la respirazione mitocondriale, producevano più molecole “batteria” (ATP) e generavano più specie reattive dell’ossigeno, tutti segnali di un motore rivitalizzato. La microscopia ha rivelato che le cellule mutate presentavano più mitocondri, di dimensioni maggiori, che formavano reti dense, supportate da un eccesso di DNA mitocondriale. Quando il BCR veniva attivato, questa già elevata attività metabolica aumentava ulteriormente, indicando che segnali esterni possono spingere un sistema energetico già predisposto a sovraccaricarsi.
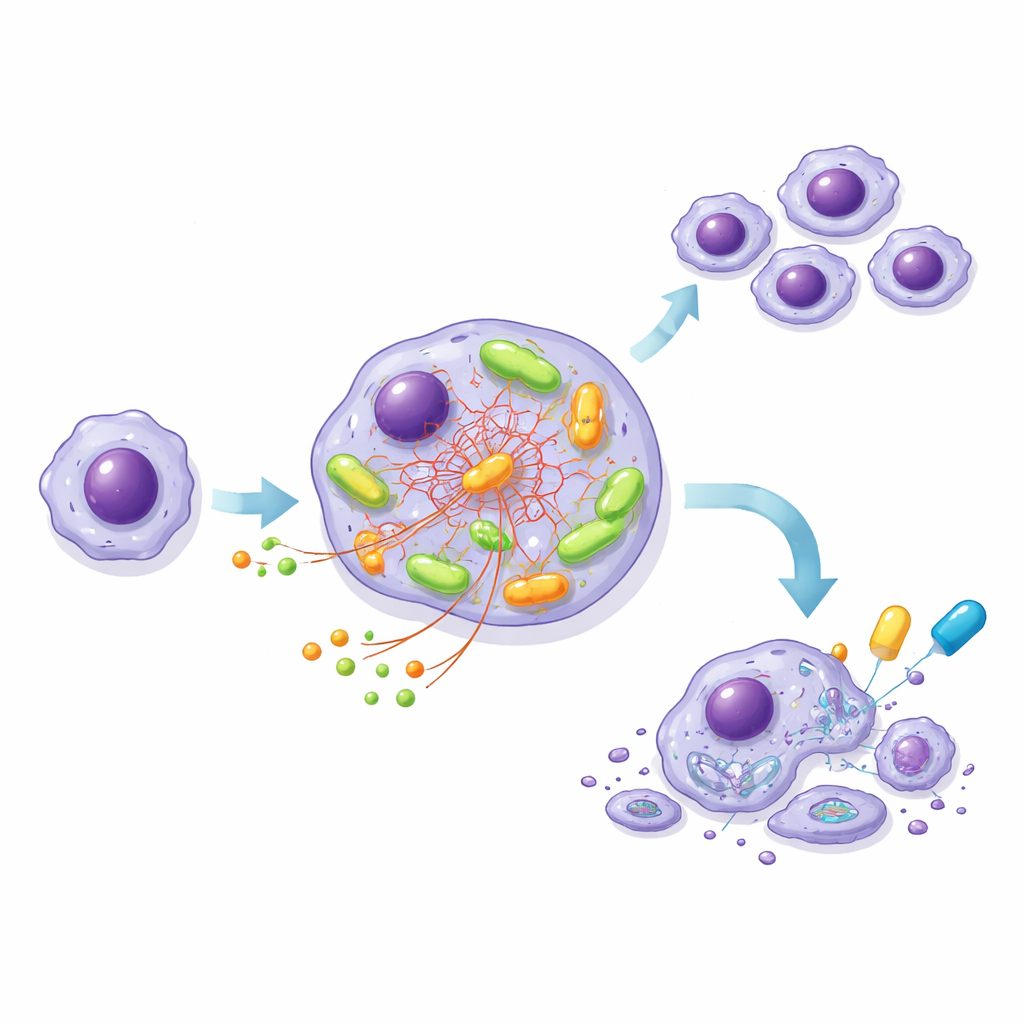
Costruire una linea cellulare modello per analizzare il motore
Poiché le cellule di LLC dei pazienti non crescono facilmente in laboratorio, il team ha ingegnerizzato una linea cellulare simile alla leucemia, MEC-1, in due versioni: una con NOTCH1 normale e una con NOTCH1 troncato e iperattivo, entrambe con lo stesso BCR ad alto rischio. Questo sistema controllato ha rispecchiato ciò che si osservava nei campioni dei pazienti. Le cellule mutate consumavano più glucosio, producevano più ATP e avevano un’ossigenazione maggiore rispetto alle controparti normali, specialmente dopo l’attivazione del BCR. Esperimenti di tracciamento dettagliati usando nutrienti marcati hanno mostrato che, nelle cellule mutate, il glucosio veniva indirizzato verso mattoni costitutivi e molecole protettive, mentre un altro nutriente, il glutamine, diventava il carburante principale che alimentava il ciclo energetico centrale all’interno dei mitocondri.
Un controllore maestro dei mitocondri e una dipendenza dal carburante
Per comprendere come NOTCH1 rimodella i mitocondri, i ricercatori hanno esaminato il paesaggio della cromatina—il modo in cui il DNA è impacchettato e segnato per l’attività. Hanno trovato che nelle cellule mutate la forma attiva di NOTCH1 si legava direttamente vicino a un gene chiamato TFAM, un regolatore chiave del DNA mitocondriale e della funzione mitocondriale, aumentando la sua espressione. Bloccare TFAM riduceva la massa mitocondriale solo nelle cellule con NOTCH1 mutato e ne induceva la morte, dimostrando che queste cellule dipendono in modo univoco da questo programma mitocondriale. Sul piano funzionale, le cellule mutate crescevano più velocemente rispetto a quelle normali in colture miste. Quando il team bloccava l’ingresso del glutamine nelle cellule, il vantaggio proliferativo delle cellule mutate scompariva e sia le cellule ingegnerizzate sia le cellule primarie di LLC con NOTCH1 mutato diventavano molto più vulnerabili, rivelando una forte “dipendenza” dal glutamine.
Trasformare una debolezza in una strategia terapeutica
Lo studio ha quindi testato se questa dipendenza dal carburante potesse migliorare l’efficacia dei farmaci esistenti. Il venetoclax, un farmaco mirato che uccide le cellule di LLC innescando la morte mitocondriale, era più efficace contro le cellule con NOTCH1 mutato rispetto a quelle normali. Colpisce notevolmente che la combinazione del blocco del trasporto del glutamine con il venetoclax aumentava drasticamente la morte delle cellule leucemiche, e questa sinergia era specifica per le cellule con NOTCH1 mutato. Anche un modello tipicamente resistente ai farmaci, portatore di danni genetici aggiuntivi, diventava sensibile con questa combinazione. In termini pratici, le cellule leucemiche ricche di mutazioni sopravvivono facendo funzionare a pieno regime i mitocondri usando il glutamine; quando quella linea di carburante viene tagliata e contemporaneamente viene applicato un segnale pro-morte, il loro sistema energetico collassa e le cellule non riescono a riprendersi.
Cosa significa per il futuro
In parole semplici, gli autori mostrano che una variazione genetica in NOTCH1, in collaborazione con i segnali ricevuti tramite il recettore delle cellule B, spinge alcune cellule di LLC a costruire centrali energetiche più grandi e attive e a dipendere fortemente dall’amminoacido glutamine per energia e crescita. Questa stessa dipendenza le rende particolarmente fragili quando l’uso del glutamine è bloccato, soprattutto se combinato con un farmaco come il venetoclax che attacca i mitocondri. Sebbene siano necessari ulteriori studi in contesti più vicini al paziente, questa vulnerabilità metabolica offre una strada promettente per personalizzare il trattamento per le persone la cui LLC porta mutazioni di NOTCH1, potenzialmente migliorando gli esiti accoppiando farmaci mirati standard con terapie metaboliche selezionate.
Citazione: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Parole chiave: leucemia linfatica cronica, mutazione NOTCH1, metabolismo del cancro, mitocondri, dipendenza dal glutamine