Clear Sky Science · ja
慢性リンパ性白血病における代謝リプログラミングの制御においてB細胞受容体とNOTCH1が機能的に協調する
患者と家族にとってなぜ重要か
慢性リンパ性白血病(CLL)は成人で最も一般的な白血病で、多くの人は長年共存しますが、一部は急速に進行して治療が困難になります。本研究は単純だが重要な問いを投げかけます:なぜ一部のCLL細胞は速く増殖し治療に抵抗するのか、そしてその脆弱性を逆手に取れるのか。研究者らは、白血病細胞上の二つの重要なスイッチがどのように協調して細胞のエネルギー利用を一新し、増殖上の利点と医師が狙える代謝上のアキレス腱の両方を生み出しているかを明らかにしました。
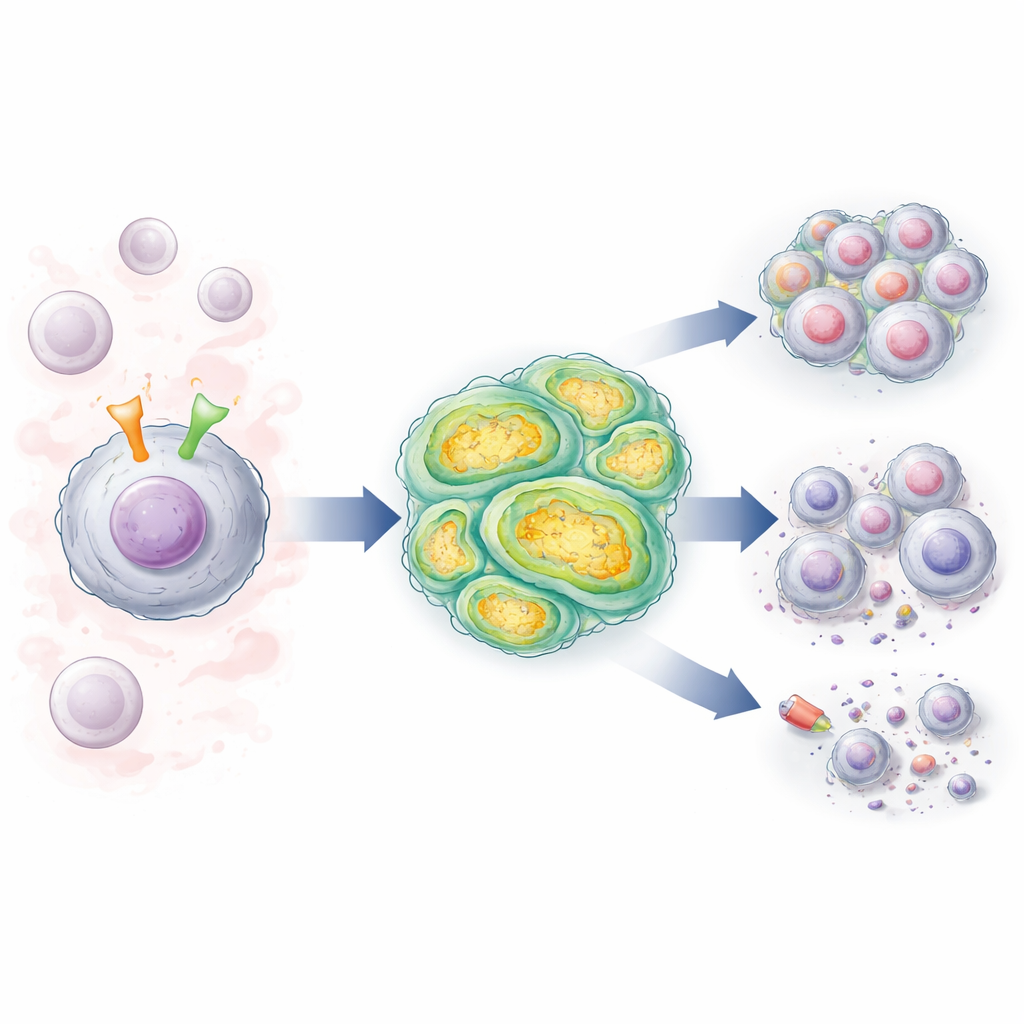
互いにやり取りする二つの細胞スイッチ
CLL細胞はB細胞受容体(BCR)と呼ばれる細胞表面のアンテナを持ち、血液やリンパ節のシグナルを感知して生存と分裂を促します。多くの患者はまたNOTCH1という遺伝子に変化を抱えており、これは活性化されると核内へ強力な増殖・生存シグナルを送る別の表面分子をコードします。著者らはBCRがハイリスクな“非変異型”パターンを共有する患者由来のCLL細胞を調べ、正常なNOTCH1を持つ細胞とNOTCH1変異を持つ細胞とを比較しました。その結果、BCRが刺激されるとNOTCH1活性が強く増強され、特に変異細胞で顕著に起こり、白血病シグナルを維持するフィードバックループを強化していることが分かりました。
白血病細胞のエネルギー産生を配線し直す
遺伝子発現マップとエネルギー使用の直接測定により、NOTCH1変異を持つCLL細胞は変異を持たない細胞よりもミトコンドリアをずっと激しく稼働させていることが示されました。これらの細胞は糖分解(グリコリシス)とミトコンドリア呼吸の双方でより多くの燃料を消費し、より多くの細胞内“バッテリー”分子(ATP)を産生し、活性酸素種を多く発生させており、いずれもエンジンが過回転している印です。顕微鏡観察では、NOTCH1変異細胞はより多く大きなミトコンドリアを有し、濃密なネットワークを形成しており、追加のミトコンドリアDNAによって支えられていました。BCRが作動すると、このすでに高い代謝活動はさらに上昇し、外部からのシグナルが既に準備されたエネルギー系を過負荷に追いやることを示していました。
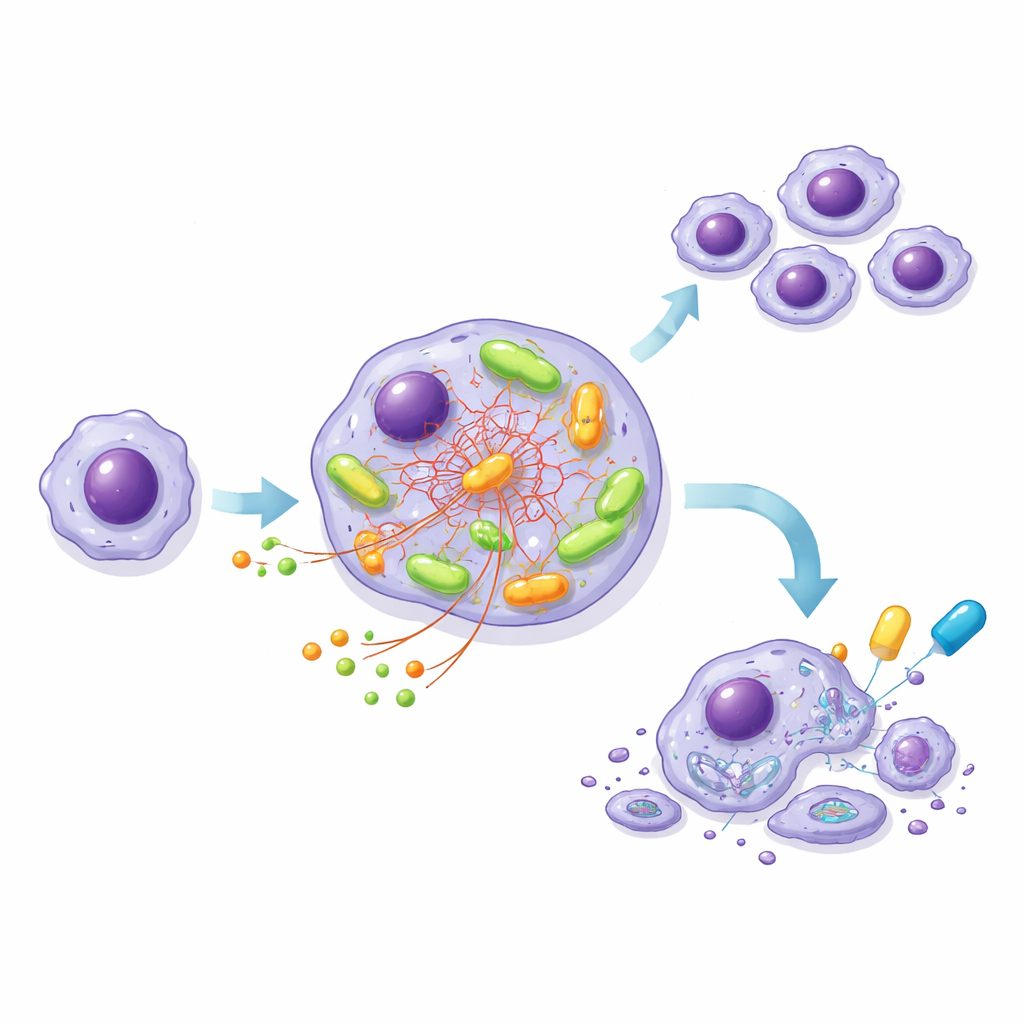
エンジンを解剖するためのモデル細胞株の構築
患者由来CLL細胞は培養で増殖しにくいため、研究チームは白血病様の細胞株MEC-1を二つのバージョンで作製しました:正常なNOTCH1を持つものと切り詰められて過剰活性化したNOTCH1を持つもの、どちらも同じハイリスクBCRを保持するという構成です。この管理された系は患者サンプルで観察された現象を反映していました。変異細胞はより多くのグルコースを消費し、より多くのATPを産生し、酸素消費も高く、特にBCR活性化後にその差が顕著でした。標識栄養素を用いた詳細なトレーシング実験は、変異細胞ではグルコースが構成要素や保護分子の合成へ向けられる一方で、別の栄養素であるグルタミンがミトコンドリア内の中心的なエネルギー回路に燃料として供給される主要経路になっていることを示しました。
ミトコンドリアの司令塔と燃料依存
NOTCH1がミトコンドリアをどのように再編するかを理解するため、研究者らはクロマチンの状態—DNAがどのように梱包され活動に印を付けられているか—を調べました。変異細胞では、活性化型NOTCH1がTFAMと呼ばれるミトコンドリアDNAと機能の主要な制御因子の近傍に直接結合し、その発現を上げていることが分かりました。TFAMを阻害するとNOTCH1変異細胞のみでミトコンドリア量が減少し、細胞死が引き起こされ、これらの細胞がこのミトコンドリアプログラムに特有の依存性を持つことが示されました。機能的には、変異細胞は混合培養で正常細胞より速く増殖しました。チームがグルタミンの細胞内取り込みを遮断すると、変異細胞の増殖優位は消え、作製した細胞株と一次のNOTCH1変異CLL細胞の両方がはるかに脆弱になり、強い“グルタミン依存”が明らかになりました。
脆弱性を治療戦略に変える
研究は次に、この燃料依存が既存薬の効果を高め得るかを検証しました。ベネトクラクス(venetoclax)はミトコンドリア由来の細胞死を誘導してCLL細胞を殺す標的薬ですが、NOTCH1変異細胞に対しては正常細胞より効果的でした。注目すべきは、グルタミン輸送の阻害とベネトクラクスの併用が白血病細胞の死を著しく増加させ、その相乗効果がNOTCH1変異細胞に特異的であったことです。通常は薬剤抵抗性を示す追加の遺伝的損傷を持つモデルでさえ、この併用で感受性を示しました。平たく言えば、変異多めの白血病細胞はグルタミンを燃料にミトコンドリアを熱く回すことで生き延びており、その燃料供給を絶ち、同時にプロ・デス(細胞死促進)シグナルを加えると、エネルギーシステムが崩壊して細胞は回復できなくなるのです。
今後の意味
簡潔に言えば、著者らはNOTCH1の遺伝的変化がB細胞受容体を介して受け取るシグナルと協働し、特定のCLL細胞により大きく活発な“発電所”を構築させ、エネルギーと増殖にアミノ酸グルタミンを強く依存させることを示しました。その同じ依存性が、特にベネトクラクスのようにミトコンドリアを標的とする薬剤と組み合わせると、グルタミン利用を遮断したときにこれらの細胞を異常に脆弱にします。より現実的な患者相当の設定でのさらなる検証は必要ですが、この代謝上の脆弱性はNOTCH1変異を有するCLL患者に治療を合わせる有望な道を提供し、標準的な標的薬と慎重に選ばれた代謝療法の組み合わせで転帰を改善する可能性があります。
引用: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
キーワード: 慢性リンパ性白血病, NOTCH1変異, がん代謝, ミトコンドリア, グルタミン依存