Clear Sky Science · ru
Функциональное взаимодействие между В-клеточным рецептором и NOTCH1 в регулировании метаболического перепрограммирования при хроническом лимфолейкозе
Почему это важно для пациентов и их семей
Хронический лимфоцитарный лейкоз (ХЛЛ) — самый распространённый лейкоз у взрослых: многие живут с ним годами, но у части пациентов заболевание становится агрессивным и плохо поддаётся лечению. Это исследование задаёт простой, но ключевой вопрос: что заставляет некоторые клетки ХЛЛ быстрее расти и сопротивляться терапии, и можно ли обратить это слабое место против них? Авторы раскрывают, как два важных «переключателя» на лейкозных клетках взаимодействуют, перестраивая их энергетический метаболизм — одновременно давая преимущество в росте и создавая скрытую метаболическую ахиллесову пяту, на которую врачи могут нацелиться.
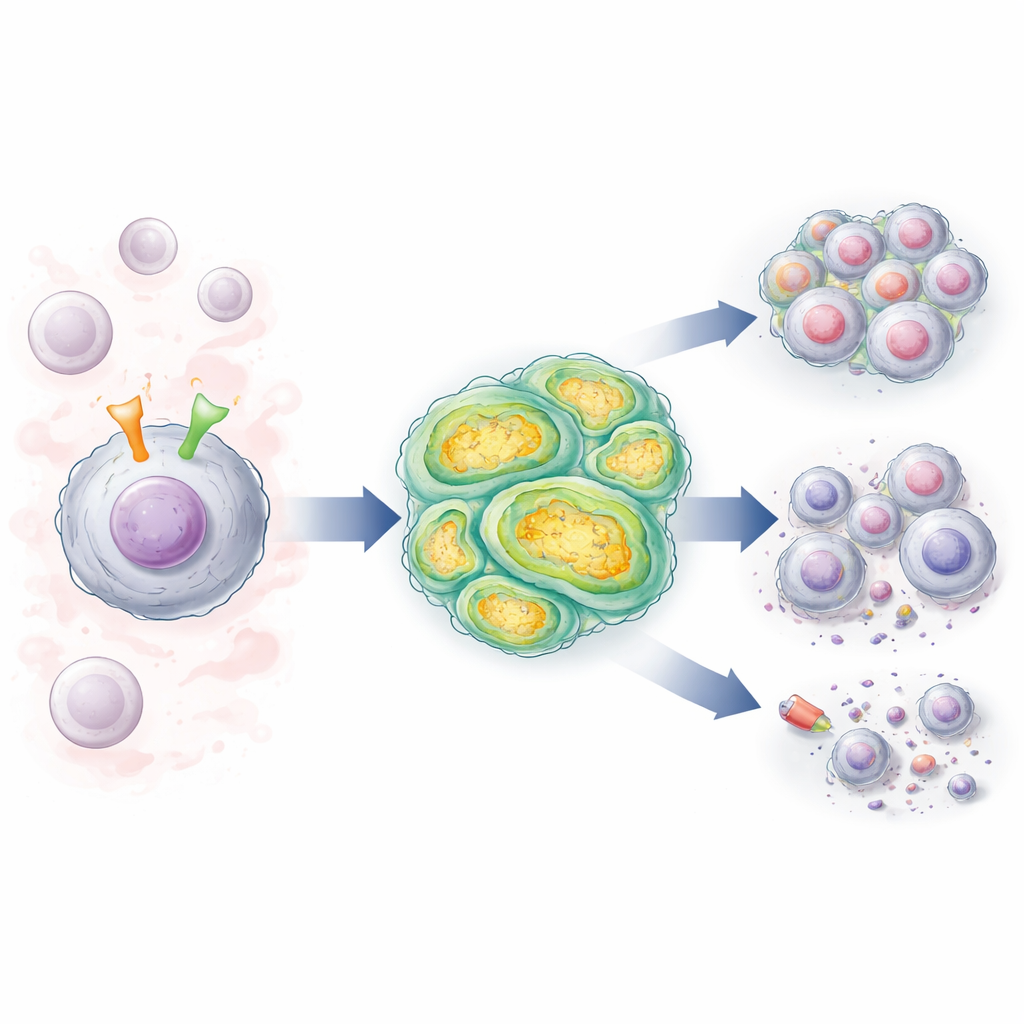
Два клеточных переключателя, которые общаются друг с другом
Клетки ХЛЛ несут на поверхности антенну, называемую В-клеточным рецептором (ВКР), который улавливает сигналы в крови и лимфе и стимулирует клетки выживать и делиться. У многих пациентов также встречаются изменения в гене NOTCH1, кодирующем ещё одну поверхностную молекулу, которая при активации посылает мощные сигналы роста и выживания в ядро. Авторы изучали клетки ХЛЛ от пациентов с высокорискованным «немутированным» паттерном ВКР и сравнивали клетки с нормальным NOTCH1 и с мутированным NOTCH1. Они обнаружили, что при стимуляции ВКР активность NOTCH1 резко возрастала, особенно в клетках с мутацией, усиливая петлю положительной обратной связи, которая поддерживает включённый лейкемический сигнальный режим.
Перенастройка способов производства энергии в лейкозных клетках
Карты активности генов и прямые измерения энергопотребления показали, что клетки ХЛЛ с мутацией NOTCH1 гораздо сильнее нагружают свои энергетические станции — митохондрии — по сравнению с клетками без мутации. Эти клетки использовали больше топлива как через гликолиз (разложение сахаров), так и через митохондриальное дыхание, производили больше «батарейных» молекул (АТФ) и генерировали больше реактивных форм кислорода — всё это признаки «раскрученного двигателя». Микроскопия показала, что у клеток с мутацией NOTCH1 митохондрий было больше, они крупнее и образовывали плотные сети, поддерживаемые увеличенным количеством митохондриальной ДНК. При активации ВКР эта и без того высокая метаболическая активность ещё больше усиливалась, что указывает на то, что внешние сигналы могут доводить уже подготовленную энергетическую систему до сверхрежима.
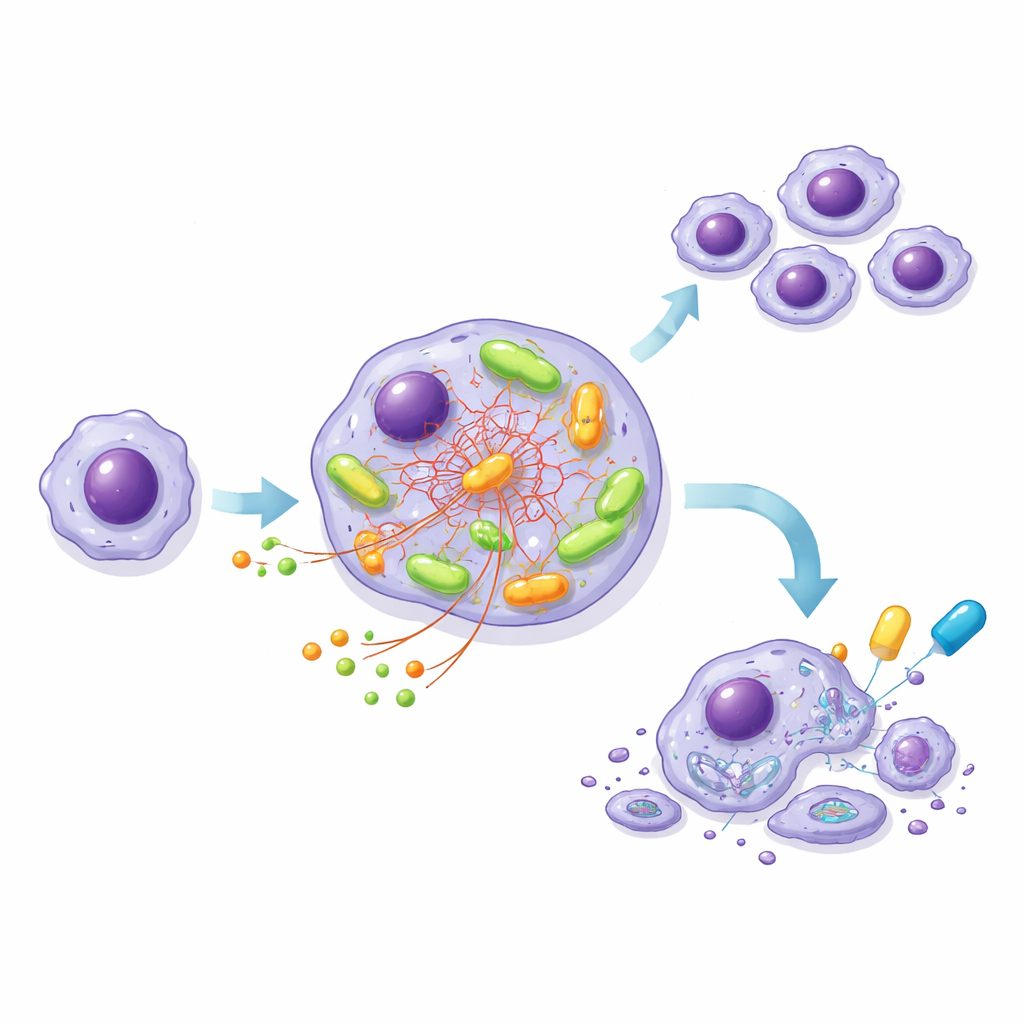
Создание модельной клеточной линии для изучения «двигателя»
Поскольку клетки пациентов с ХЛЛ плохо растут в лаборатории, команда создала похожую на лейкоз клеточную линию MEC-1 в двух вариантах: с нормальным NOTCH1 и с усечённым, гиперактивным NOTCH1; обе линии несли одинаковый высокорискованный ВКР. Эта контролируемая модель воспроизвела наблюдения в образцах пациентов. Мутантные клетки потребляли больше глюкозы, вырабатывали больше АТФ и имели более высокий уровень потребления кислорода, чем нормальные клетки, особенно после активации ВКР. Точные эксперименты с мечеными нутриентами показали, что в мутантных клетках глюкоза шла преимущественно на синтез строительных и защитных молекул, тогда как другой нутриент — глутамин — становился основным топливом, питающим центральный энергетический цикл в митохондриях.
Главный регулятор митохондрий и «наркотик» в виде топлива
Чтобы понять, как NOTCH1 перестраивает митохондрии, исследователи изучили хроматиновый ландшафт — то есть упаковку ДНК и маркеры активности генов. Они обнаружили, что в мутантных клетках активная форма NOTCH1 связывалась непосредственно рядом с геном TFAM, ключевым регулятором митохондриальной ДНК и функции, и усиливала его экспрессию. Блокада TFAM уменьшала митохондриальную массу только в клетках с мутацией NOTCH1 и вызывала их гибель, показывая, что эти клетки уникально зависят от данной митохондриальной программы. Функционально мутантные клетки росли быстрее, чем нормальные, в смешанных культурах. Когда команда блокировала вход глутамина в клетки, преимущество в росте мутантных клеток исчезало, а и модельные клетки, и первичные клетки ХЛЛ с мутацией NOTCH1 становились существенно более уязвимыми — это выявило сильную «зависимость» от глутамина.
Обращение слабости в лечебную стратегию
Далее исследование проверило, можно ли использовать эту топливную зависимость, чтобы повысить эффективность существующих препаратов. Венетоклакс, таргетный препарат, убивающий клетки ХЛЛ путём индукции митохондриальной программы гибели, оказался более эффективным в отношении клеток с мутацией NOTCH1 по сравнению с нормальными. Поразительно, что сочетание блокады транспорта глутамина с венетоклаксом резко увеличивало гибель лейкозных клеток, и этот синергизм был специфичен для клеток с мутантным NOTCH1. Даже модель, обычно резистентная из‑за дополнительного генетического поражения, становилась чувствительной при таком сочетании. Проще говоря, клетки лейкемии с множественными мутациями выживают, поддерживая митохондрии в «горячем» режиме на глутамине; когда этот канал питания перекрывают и одновременно вводят про‑смертный сигнал по митохондриям, их энергетическая система рушится, и клетки не способны восстановиться.
Что это значит для дальнейших исследований
Проще говоря, авторы показывают, что генетическое изменение NOTCH1 в сочетании с сигналами через В-клеточный рецептор заставляет часть клеток ХЛЛ строить большие и более активные энергетические станции и сильно зависеть от аминокислоты глутамина для энергии и роста. Эта же зависимость делает их необычно уязвимыми при блокаде использования глутамина, особенно в комбинации с препаратом вроде венетоклакса, атакующим митохондрии. Хотя требуются дополнительные исследования в моделях, максимально приближённых к пациентам, эта метаболическая уязвимость открывает перспективный путь для персонализации терапии пациентов с мутациями NOTCH1, потенциально улучшая исходы за счёт сочетания стандартных таргетных препаратов с тщательно подобранными метаболическими вмешательствами.
Цитирование: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Ключевые слова: хронический лимфоцитарный лейкоз, мутация NOTCH1, метаболизм рака, митохондрии, зависимость от глутамина