Clear Sky Science · de
Funktionelle Zusammenarbeit zwischen B-Zell-Rezeptor und NOTCH1 bei der Regulation des metabolischen Umschaltens beim chronischen lymphatischen Leukämie
Warum das für Patienten und Familien wichtig ist
Die chronische lymphatische Leukämie (CLL) ist die häufigste Leukämie im Erwachsenenalter. Viele Betroffene leben jahrelang mit der Erkrankung, doch manche Verläufe werden aggressiv und schwer behandelbar. Diese Studie stellt eine einfache, aber entscheidende Frage: Was macht manche CLL-Zellen schneller wachsend und therapieresistent, und lässt sich diese Schwäche therapeutisch ausnutzen? Die Forschenden zeigen, wie zwei zentrale Schalter auf Leukämiezellen zusammenwirken, um deren Energiehaushalt umzubauen – das verschafft den Zellen einen Wachstumsvorteil, schafft aber gleichzeitig eine versteckte metabolische Achillesferse, die klinisch angegriffen werden könnte.
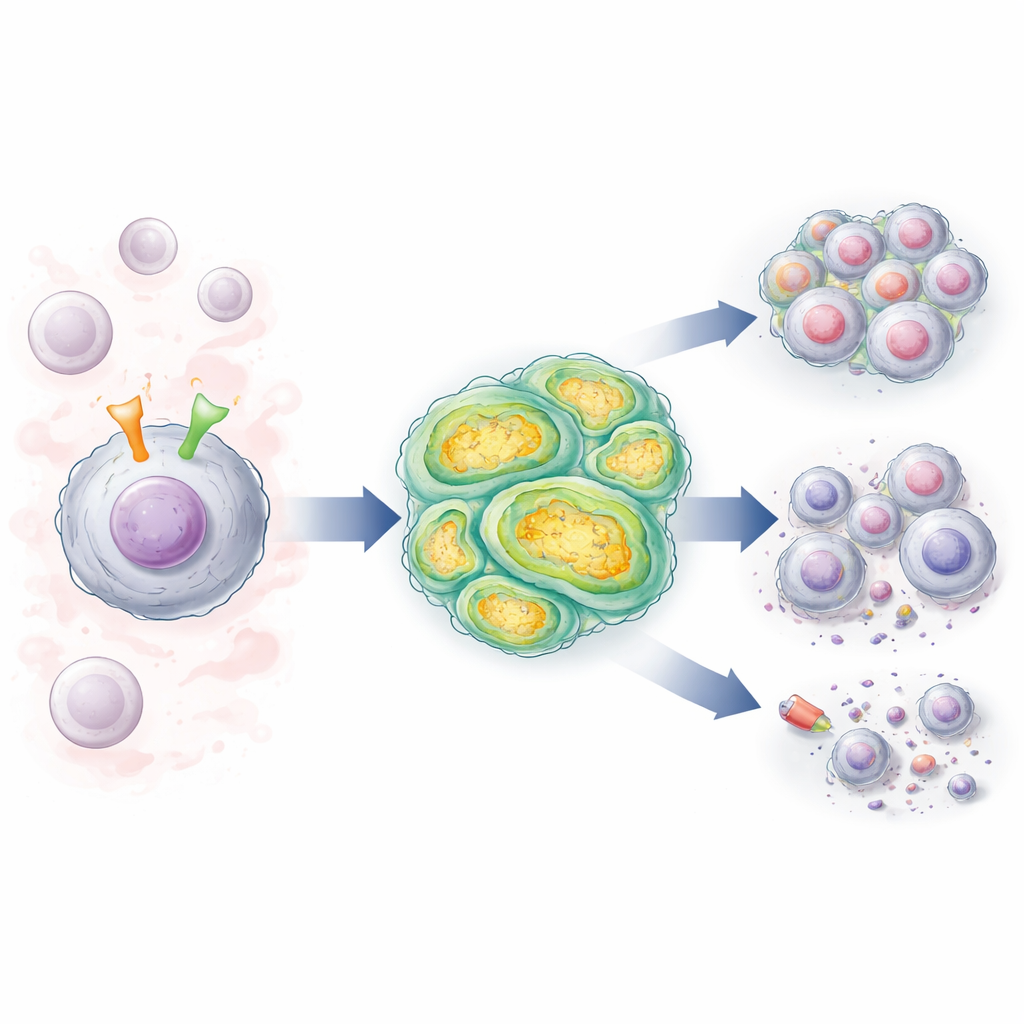
Zwei Zellschalter, die miteinander kommunizieren
CLL-Zellen tragen einen Oberflächenempfänger, den B-Zell-Rezeptor (BCR), der Signale im Blut und in Lymphknoten wahrnimmt und die Zellen zum Überleben und zur Teilung antreibt. Bei vielen Patientinnen und Patienten liegen zudem Veränderungen im Gen NOTCH1 vor; dieses kodiert ein weiteres Oberflächenmolekül, das nach Aktivierung starke Wachstums- und Überlebenssignale in den Zellkern weitergibt. Die Autorinnen und Autoren untersuchten CLL-Zellen von Patientinnen und Patienten mit einem hochriskanten, „unmutierten“ BCR-Muster und verglichen Zellen mit normalem NOTCH1 mit solchen, die NOTCH1-Mutationen tragen. Sie fanden heraus, dass BCR-Stimulation die NOTCH1‑Aktivität kräftig erhöht — besonders in den mutierten Zellen — und so eine Rückkopplungsschleife stärkt, die das leukämische Signaling dauerhaft aufrechterhält.
Umschaltung der Energieerzeugung in Leukämiezellen
Genexpressionsprofile und direkte Messungen des Energieverbrauchs zeigten, dass NOTCH1-mutierte CLL-Zellen ihre Kraftwerke, die Mitochondrien, deutlich intensiver betreiben als Zellen ohne Mutation. Diese Zellen verbrauchten mehr Brennstoff sowohl über die Glykolyse (Zuckerabbau) als auch über die mitochondriale Atmung, produzierten mehr zelluläre „Batteriemoleküle“ (ATP) und erzeugten mehr reaktive Sauerstoffspezies – alles Anzeichen eines hochgefahrenen Motors. Die Mikroskopie enthüllte, dass NOTCH1-mutierte Zellen mehr und größere Mitochondrien in dichten Netzwerken besitzen, unterstützt durch zusätzliche mitochondriale DNA. Bei BCR-Aktivierung stieg diese bereits hohe metabolische Aktivität weiter an, was darauf hinweist, dass extrazelluläre Signale ein bereits vorgespultes Energiesystem noch weiter hochfahren können.
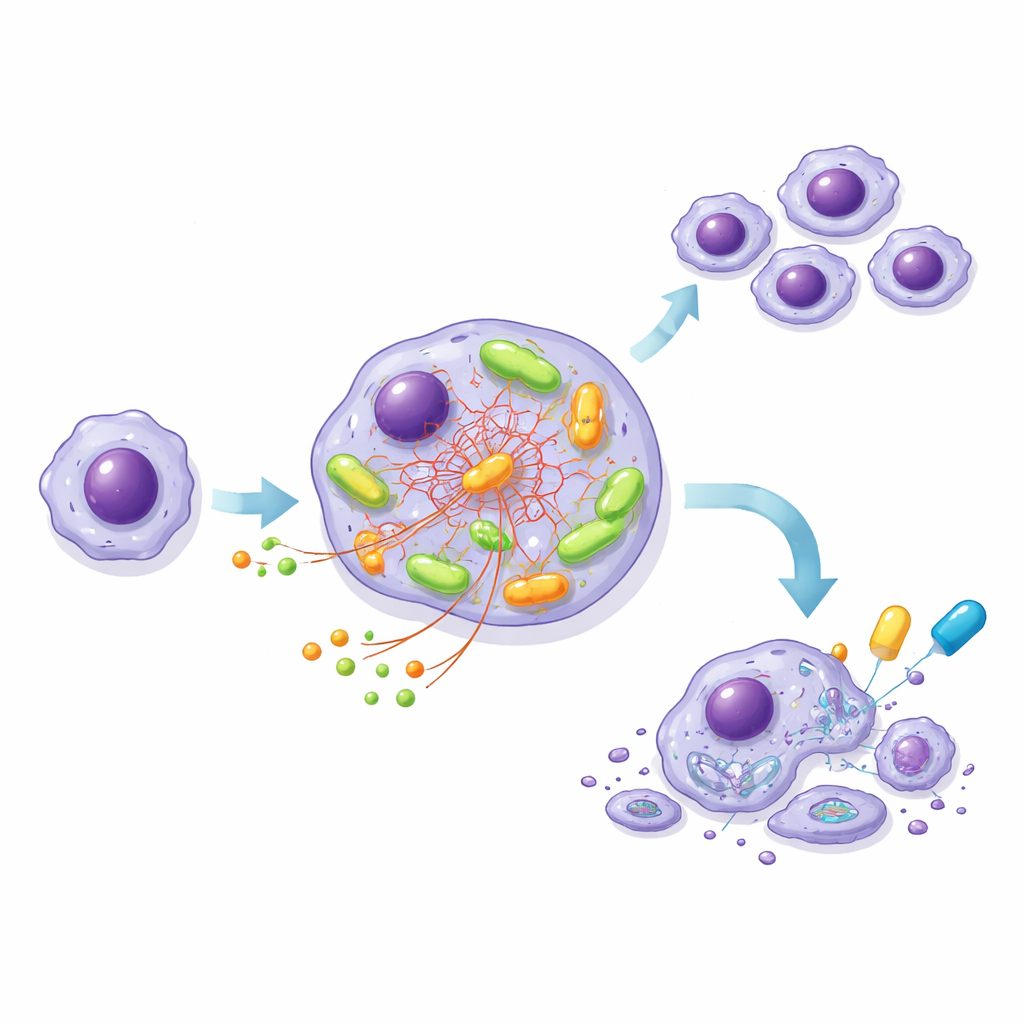
Ein Modellzelllinien-System zum Entschlüsseln des Motors
Da primäre CLL-Zellen im Labor schwer zu kultivieren sind, erzeugte das Team eine leukämieähnliche Zelllinie, MEC-1, in zwei Versionen: eine mit normalem NOTCH1 und eine mit einer verkürzten, überaktiven NOTCH1‑Form, jeweils mit demselben hochriskanten BCR. Dieses kontrollierte System spiegelte die Beobachtungen aus Patientenproben wider. Die mutierten Zellen nahmen mehr Glukose auf, produzierten mehr ATP und zeigten eine höhere Sauerstoffverwendung als die normalen Zellen, insbesondere nach BCR‑Aktivierung. Detaillierte Tracing‑Experimente mit markierten Nährstoffen zeigten, dass in den mutierten Zellen Glukose vermehrt in Baustoffe und Schutzmoleküle gelenkt wurde, während ein anderes Nährstoffsubstrat, Glutamin, zur Haupttreibstoffquelle für den zentralen mitochondrialen Energiestoffwechsel wurde.
Ein Master‑Regulator der Mitochondrien und eine Brennstoff‑Sucht
Um zu verstehen, wie NOTCH1 die Mitochondrien umgestaltet, untersuchten die Forschenden die Chromatinlandschaft — also die Verpackung und Markierung der DNA für Aktivität. Sie fanden heraus, dass in den mutierten Zellen die aktive Form von NOTCH1 direkt in der Nähe des Gens TFAM gebunden war, eines Schlüsselregulators der mitochondrialen DNA und Funktion, und dessen Expression hochregulierte. Das Blockieren von TFAM reduzierte die mitochondriale Masse nur in NOTCH1‑mutierten Zellen und löste in ihnen den Zelltod aus, was zeigt, dass diese Zellen eindeutig von diesem mitochondrialen Programm abhängig sind. Funktionell wuchsen die mutierten Zellen in Durchmischungskulturen schneller als normale Zellen. Wenn der Eintritt von Glutamin in die Zellen blockiert wurde, verschwand der Wachstumsvorteil der mutierten Zellen, und sowohl die konstruierten Zellen als auch primäre NOTCH1‑mutierte CLL‑Zellen wurden deutlich verwundbarer — ein starker Hinweis auf eine „Sucht“ nach Glutamin.
Eine Schwäche in eine Behandlungsstrategie verwandeln
Die Studie testete anschließend, ob diese Brennstoffabhängigkeit vorhandene Medikamente verstärken kann. Venetoclax, ein zielgerichtetes Mittel, das CLL‑Zellen durch Auslösen mitochondrialer Zelltodwege tötet, war wirksamer gegen NOTCH1‑mutierte Zellen als gegen normale. Bemerkenswert war, dass die Kombination aus Blockade des Glutamintransports und Venetoclax die Leukämiezellsterblichkeit stark erhöhte; diese Synergie war spezifisch für NOTCH1‑mutierte Zellen. Sogar ein normalerweise medikamentenresistentes Modell mit zusätzlichen genetischen Schäden wurde unter dieser Kombination empfindlich. Vereinfacht gesagt: Die mutierten Leukämiezellen überleben, indem sie ihre Mitochondrien mit Glutamin auf Hochtouren betreiben; kappt man diese Brennstoffzufuhr und setzt gleichzeitig ein pro‑apoptotisches Signal, bricht ihr Energiesystem zusammen und die Zellen erholen sich nicht.
Was das für die Zukunft bedeutet
Kurz gefasst zeigen die Autorinnen und Autoren, dass eine genetische Veränderung in NOTCH1 zusammen mit Signalen über den B‑Zell‑Rezeptor bestimmte CLL‑Zellen dazu bringt, größere und aktivere Energiewerke aufzubauen und sich stark auf die Aminosäure Glutamin für Energie und Wachstum zu stützen. Diese Abhängigkeit macht sie besonders verwundbar, wenn die Glutaminnutzung blockiert wird, insbesondere in Kombination mit einem Medikament wie Venetoclax, das auf Mitochondrien abzielt. Zwar sind weitere Untersuchungen in realistischen, patientennahen Modellen nötig, doch bietet diese metabolische Verwundbarkeit einen vielversprechenden Ansatz, die Therapie für Menschen mit NOTCH1‑mutierter CLL zu individualisieren und die Behandlungsergebnisse durch die Kombination standardisierter Zieltherapien mit gezielten metabolischen Interventionen zu verbessern.
Zitation: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Schlüsselwörter: chronische lymphatische Leukämie, NOTCH1-Mutation, Krebsstoffwechsel, Mitochondrien, Glutaminabhängigkeit