Clear Sky Science · sv
Funktionellt samarbete mellan B-cellsreceptorn och NOTCH1 i reglering av metabolisk ominställning vid kronisk lymfatisk leukemi
Varför detta spelar roll för patienter och familjer
Kronisk lymfatisk leukemi (KLL) är den vanligaste leukemin hos vuxna, och även om många lever med sjukdomen i åratal blir vissa fall aggressiva och svåra att behandla. Denna studie ställer en enkel men avgörande fråga: vad får vissa KLL-celler att växa snabbare och stå emot behandling, och kan den svagheten vändas mot dem? Forskarna avslöjar hur två viktiga reglage på leukemicellerna samarbetar för att omprogrammera cellernas energianvändning, vilket skapar både en tillväxtfördel och en dold metabolisk akilleshäl som läkare kan kunna rikta in sig på.
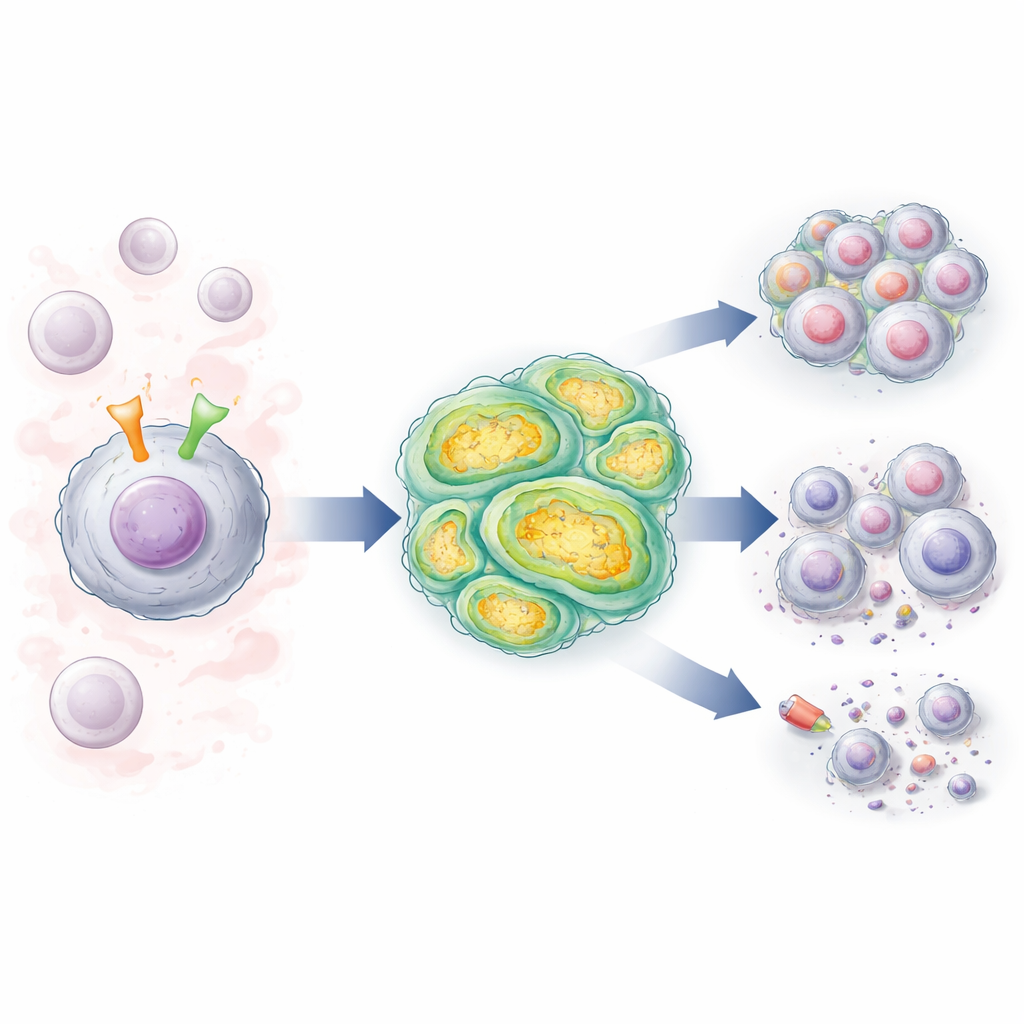
Två cellreglage som kommunicerar
KLL-celler bär en ytantenn kallad B-cellsreceptorn (BCR), som känner av signaler i blod och lymfnoder och driver cellerna att överleva och dela sig. Många patienter har också förändringar i en gen som heter NOTCH1, som kodar för en annan ytmolekyl som, när den aktiveras, skickar starka tillväxt- och överlevnadssignaler in i kärnan. Författarna studerade KLL-celler från patienter vars BCR:er delade ett hög-risk, “omuterat” mönster, och jämförde celler med normal NOTCH1 med celler med NOTCH1-mutationer. De fann att när BCR stimulerades ökade NOTCH1-aktiviteten kraftigt, särskilt i de muterade cellerna, vilket förstärkte en återkopplingsslinga som håller den leukemiska signaleringen påslagen.
Omkoppling av hur leukemiceller skaffar energi
Kartor över genaktivitet och direkta mätningar av energianvändning visade att NOTCH1-mutanta KLL-celler driver sina kraftverk—mitokondrierna—mycket hårdare än celler utan mutationen. Dessa celler förbrukade mer bränsle via både glykolys (sockerbrytning) och mitokondriell respiration, producerade mer av cellens “batterimolekyler” (ATP) och genererade fler reaktiva syreföreningar, alla tecken på en varvad motor. Mikroskopi visade att NOTCH1-mutanta celler hade fler och större mitokondrier som bildade täta nätverk, stödda av extra mitokondrie-DNA. När BCR aktiverades steg denna redan höga metaboliska aktivitet ännu mer, vilket tyder på att signaler utifrån kan skjuta ett redan förberett energisystem i övervarv.
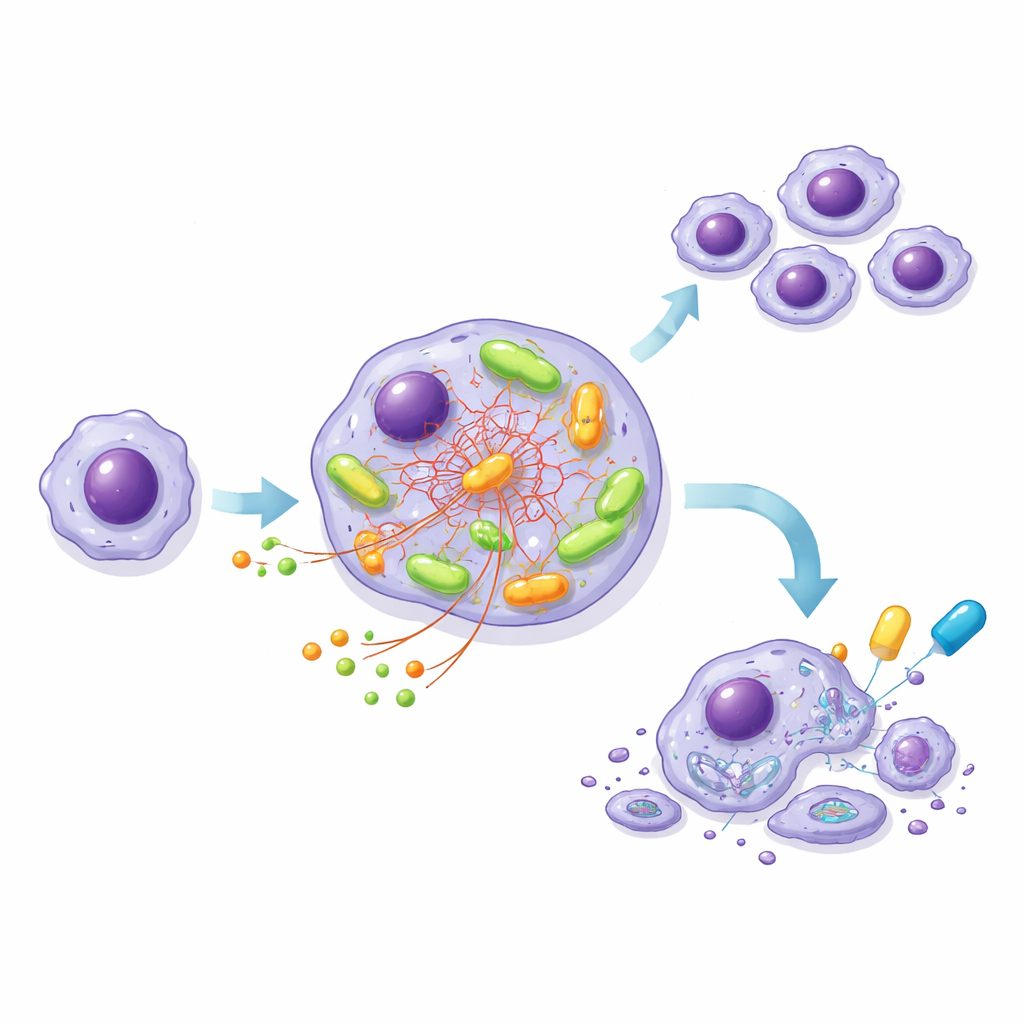
Bygga en modellcellinje för att dissekera motorn
Eftersom patientens KLL-celler inte växer lätt i labbet konstruerade teamet en leukemilik cellinje, MEC-1, i två versioner: en med normal NOTCH1 och en med en trunkerad, överaktiv NOTCH1, båda med samma hög-risk BCR. Detta kontrollerade system speglade det som sågs i patientprover. De mutanta cellerna förbrukade mer glukos, producerade mer ATP och hade högre syreförbrukning än sina normala motsvarigheter, särskilt efter BCR-aktivering. Detaljerade spårningsexperiment med märkta näringsämnen visade att i mutanta celler gick glukos åt till byggstenar och skyddande molekyler, medan ett annat näringsämne, glutamin, blev huvudbränslet som matade det centrala energicykeln inne i mitokondrierna.
En mästarkontroller för mitokondrier och ett bränsleberoende
För att förstå hur NOTCH1 omformar mitokondrierna undersökte forskarna kromatinlandskapet—hur DNA paketeras och markeras för aktivitet. De fann att i mutanta celler bund den aktiva formen av NOTCH1 direkt nära en gen kallad TFAM, en nyckelkontrollant för mitokondrie-DNA och funktion, och uppreglerade den. Att blockera TFAM minskade mitokondriemassan endast i NOTCH1-mutanta celler och utlöste deras död, vilket visar att dessa celler är unikt beroende av detta mitokondriella program. Funktionellt växte mutanta celler snabbare än normala celler i blandade kulturer. När teamet blockerade glutamintransport in i cellerna försvann den mutanta cellernas tillväxtfördel, och både de konstruerade cellerna och primära NOTCH1-mutanta KLL-celler blev mycket mer sårbara, vilket avslöjar ett starkt ”beroende” av glutamin.
Att vända en svaghet till en behandlingsstrategi
Studien testade sedan om detta bränsleberoende kunde hjälpa befintliga läkemedel att fungera bättre. Venetoclax, ett riktat läkemedel som dödar KLL-celler genom att utlösa mitokondriell celldöd, var mer effektivt mot NOTCH1-mutanta celler än mot normala. Slående nog ökade kombinationen av glutamintransportblockad och venetoclax kraftigt leukemicelldöd, och denna synergi var specifik för NOTCH1-mutanta celler. Även en modell som vanligtvis är läkemedelsresistent på grund av ytterligare genetiska skador blev känslig under denna kombination. I vardagliga termer överlever de mutantrika leukemicellerna genom att köra sina mitokondrier varma på glutamin; när den bränsleledningen klipps av och en pro-död-signal appliceras samtidigt fallerar deras energisystem och cellerna kan inte återhämta sig.
Vad detta betyder framöver
Enkelt uttryckt visar författarna att en genetisk förändring i NOTCH1, i samverkan med signaler som tas emot via B-cellsreceptorn, driver vissa KLL-celler att bygga större, mer aktiva kraftverk och att i hög grad förlita sig på aminosyran glutamin för energi och tillväxt. Samma beroende gör dem ovanligt skörare när glutaminanvändningen blockeras, särskilt i kombination med ett läkemedel som venetoclax som angriper mitokondrierna. Även om mer arbete i patientlika, kliniska sammanhang behövs, erbjuder denna metaboliska sårbarhet en lovande väg för att skräddarsy behandling för personer vars KLL bär NOTCH1-mutationer, med potential att förbättra utfall genom att para standardiserade riktade läkemedel med noggrant utvalda metaboliska terapier.
Citering: Fascì, A., Vallone, F.E., Nabelsi, N. et al. Functional cooperation between the B-cell receptor and NOTCH1 in regulating metabolic reprogramming in chronic lymphocytic leukemia. Leukemia 40, 982–995 (2026). https://doi.org/10.1038/s41375-026-02912-7
Nyckelord: kronisk lymfatisk leukemi, NOTCH1-mutation, cancermetabolism, mitokondrier, glutaminberoende