Clear Sky Science · sv
Homogena bildbaserade digitala immunoassayer med hög felförtålighet
Varför små partiklar och smarta kameror spelar roll
Många av dagens medicinska tester kräver antingen ett fullskaligt laboratorium med utbildad personal eller ger snabba men grova svar på en enkel remsa. Denna artikel presenterar ett sätt att kombinera fördelarna hos båda: laboratoriekvalitet från ett litet blodprov med enkel hårdvara, där det mesta av jobbet utförs av avancerad bildanalys. Genom att observera hur små guldpartiklar beter sig i en bloddroppe och låta maskininlärningsprogram tolka bilderna visar författarna en väg mot hemmatest och kliniska tester som både är lätta att använda och svåra att vilseleda.
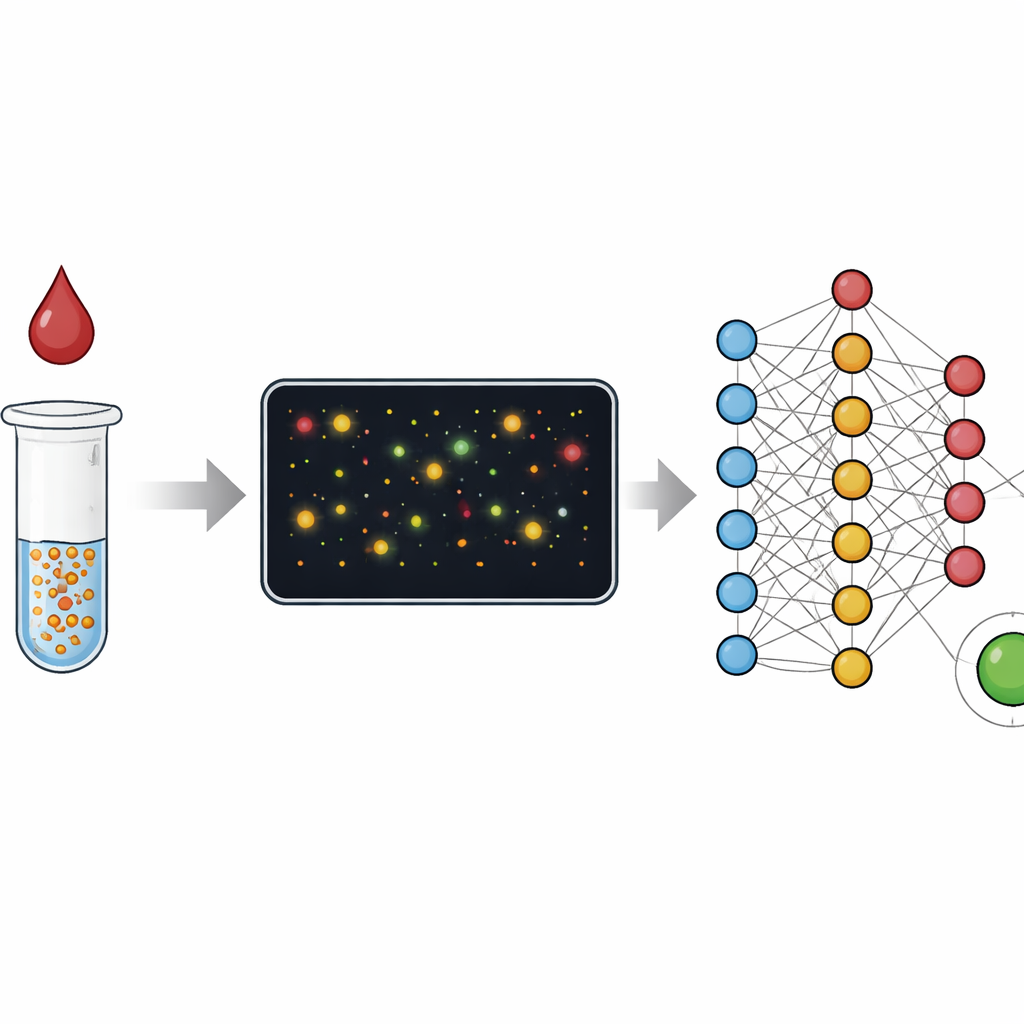
Från färgförändringar till partikelräkning
Traditionella blodtester som ELISA läser av en genomsnittlig färgförändring från miljontals molekyler i en brunn, ungefär som att bedöma en publik utifrån dess totala ljudnivå. Snabba remstester, så kallade lateral flow-assays, bygger på en liknande idé och byter noggrannhet mot snabbhet och enkelhet. I denna studie fokuserar forskarna istället på enskilda guldförsedda nanopartiklar som klumpar ihop sig när de hittar sitt mål i ett prov, till exempel C-reaktivt protein som är kopplat till inflammation eller antikroppar mot viruset som orsakar COVID-19. Istället för att mäta endast lösningens bulkfärg använder de mörkfältsmikroskopi för att avbilda små fält fulla av dessa partiklar och kluster, och analyserar sedan varje enskild partikel. Denna övergång från "analog" färg till "digital" räkning vidgar drastiskt det dynamiska området testet kan mäta och gör det lättare att upptäcka när något gått fel.
Se igenom röran i verkliga prover
Riktiga blodprov är röriga: de innehåller röda blodkroppar, partiklar, bubblor och andra källor till visuellt brus som kan förvirra enkla bildbehandlingsregler. Gruppen visar först att även med finjusterade konventionella algoritmer kan de extrahera ett rent, nästan linjärt samband mellan klusterstorlek och nivåer av C-reaktivt protein, och att detta kan göras direkt i helblod utan att skilja ut cellerna. För att hantera artefakter mer systematiskt tränar de sedan en segmenteringsmodell som märker varje pixel i en bild som nanopartikel, cell, damm eller bakgrund. Efter att ha filtrerat bort allt utom de verkliga partiklarna använder de återigen klusterstorlek som avläsning. Med detta hybrida tillvägagångssätt klassificerar de korrekt COVID-19-antikroppsstatus i lagrade patientsera med 96 % specificitet och 90 % sensitivitet, även om bilderna samlades in under medvetet felfyllda förhållanden.
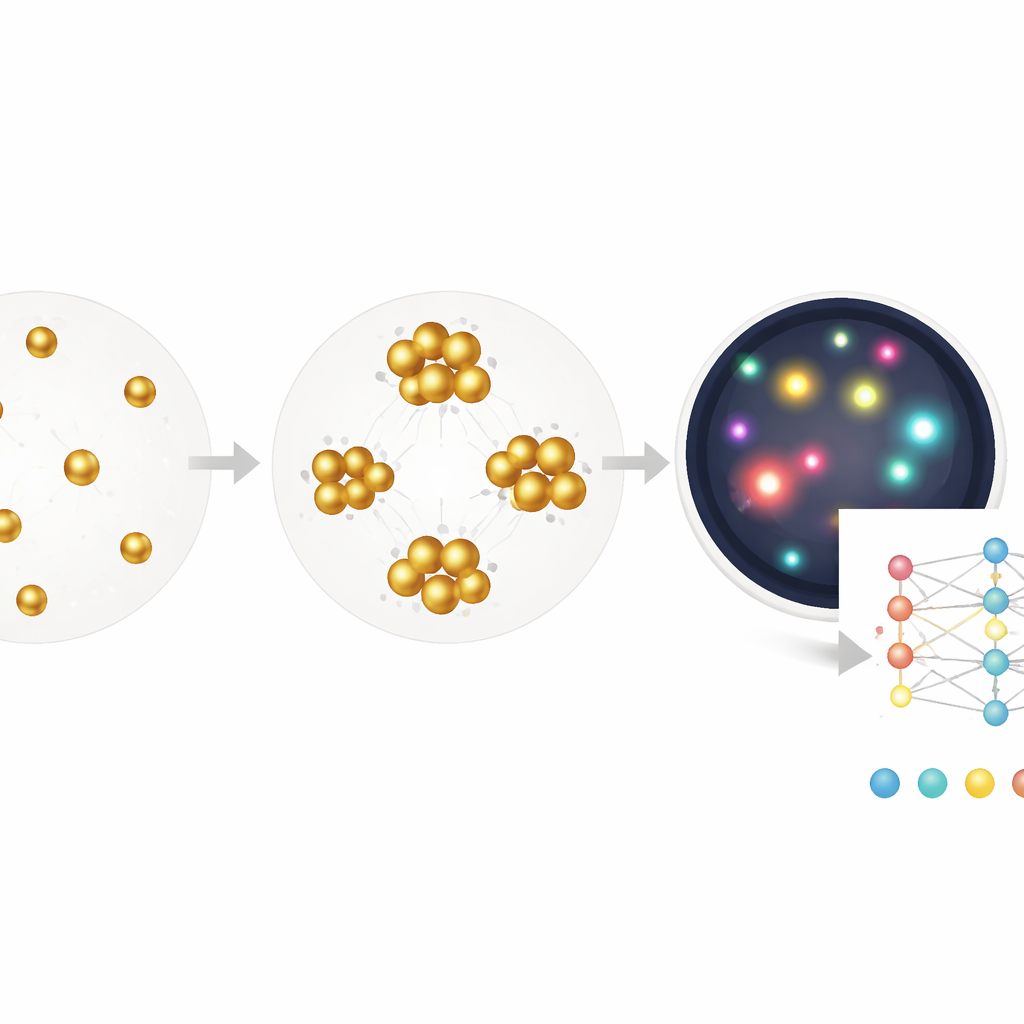
Låta datorn upptäcka vad som är viktigt
Även om segmenteringsmetoden hjälper förlitar den sig fortfarande på mänskliga val om vilka egenskaper som ska mätas—till exempel hur stort eller ljust ett kluster måste vara. Författarna går längre genom att träna ett djupt neuralt nätverk som går direkt från en rå bild till koncentrationen av antivirala antikroppar, med enbart den kända koncentrationen som etikett och utan pixelnivå-annoteringar. Denna end-to-end-modell, byggd på en standard ResNet-arkitektur, lär sig effektivt sin egen kombination av ledtrådar: subtila färgskiftningar, densitet, klusterform, tomrum och mer. Vid test på nya prover uppskattar den antikroppsnivåer över ett intervall på mer än tre och en halv storleksordning, med en detektionsgräns som närmar sig den hos ett kliniskt ELISA-kit, samtidigt som den kräver endast en enda 30-minuters inkubation och fungerar med mycket små volymer.
Designa tester som kan finjusteras som ett mikroskop
Utöver att demonstrera fungerande analyser frågar studien också hur långt denna typ av digital partikelräkning i princip kan drivas. Med en matematisk och simuleringsmässig ram visar författarna att känsligheten hos sådana tester inte är fast; den beror på hur många partiklar som används, hur lika de är och hur väl enstaka respektive parade partiklar kan särskiljas utifrån ljusstyrka. Genom att justera dessa reglage—särskilt antalet partiklar och deras kvalitet—argumenterar de för att man i teorin kan nå extremt låga detekterbara koncentrationer, begränsade främst av grundläggande räknestatistik. Maskininlärning ger ytterligare vinster genom att öka hur många partiklar som med hög säkerhet kan användas och genom att förbättra diskrimineringen mellan verkliga bindningsevenemang och slumpmässigt brus.
Mot smartare, mer förlåtande blodtester
Sammantaget tyder arbetet på att kombinera enkel optik med avancerad bildanalys kan leverera tester som kan mäta i nivå med guldstandarder i labbet samtidigt som de tål variationer i verklig användning. Istället för att bygga ständigt mer precis hårdvara förlitar sig tillvägagångssättet på den rika information som redan finns i bilder och låter programvara skilja signal från brus. För patienter och vårdsystem kan detta innebära mer tillförlitliga point-of-care- och självtester för vanliga blodmarkörer och infektionssjukdomar, utan behov av komplexa instrument eller expertoperatörer.
Citering: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Nyckelord: digital immunoassay, nanopartikelavbildning, maskininlärningsdiagnostik, point-of-care-testning, SARS-CoV-2-antikroppar