Clear Sky Science · ru
Однородные иммуноассайи на основе изображений с высокой устойчивостью к ошибкам
Почему важны крошечные частицы и умные камеры
Многие современные медицинские тесты либо требуют полноценной лаборатории с квалифицированным персоналом, либо дают быстрые, но грубые ответы на простых полосках. В этой работе предложен способ получить лучшее из обоих миров: лабораторную точность по небольшому образцу крови при помощи простого оборудования, где основная работа выполняется с помощью продуманного анализа изображений. Наблюдая за поведением крошечных золотых наночастиц в капле крови и позволяя программам машинного обучения интерпретировать эти снимки, авторы демонстрируют путь к домашним и клиническим тестам, которые одновременно просты в использовании и трудны для подделки.
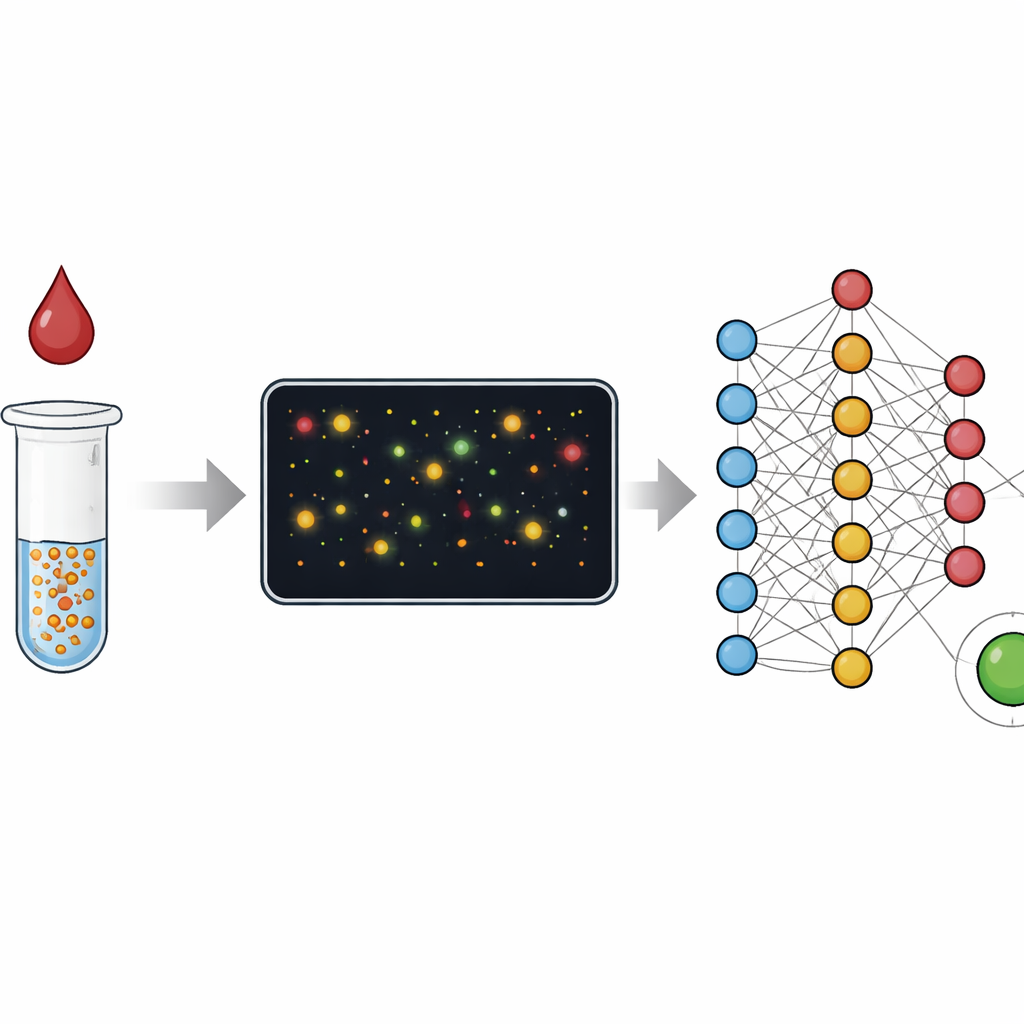
От цветовых изменений к подсчёту частиц
Традиционные лабораторные тесты, такие как ELISA, читают усреднённое изменение цвета от миллионов молекул в лунке — как судить о толпе по общему уровню шума. Быстрые тест‑полоски, или латеральные иммунологические тесты, опираются на похожую идею и жертвуют точностью ради скорости и простоты. В этом исследовании учёные сосредотачиваются на отдельных золотых наночастицах, которые объединяются в кластеры при обнаружении своей мишени в образце, например С‑реактивного белка, связанного с воспалением, или антител к вирусу, вызывающему COVID‑19. Вместо измерения только общей окраски раствора они используют темнопольную микроскопию для съёмки небольших полей, заполненных этими частицами и сгустками, а затем анализируют каждую из них. Переход от «аналоговой» оценки цвета к «цифровому» подсчёту существенно расширяет диапазон концентраций, которые тест может измерить, и облегчает обнаружение сбоев.
Видеть сквозь беспорядок в реальных образцах
Настоящие образцы крови сложны: они содержат эритроциты, фрагменты, пузыри и другие источники визуального шума, которые могут ввести в заблуждение простые алгоритмы обработки изображений. Сначала команда показывает, что даже при настроенных традиционных алгоритмах можно выделить чистую, почти линейную зависимость между размером кластера и уровнем С‑реактивного белка, причём это достигается прямо в цельной крови без центрифугирования клеток. Чтобы систематически справляться с артефактами, они обучают модель сегментации, которая помечает каждый пиксель изображения как наночастицу, клетку, пыль или фон. Отфильтровав всё, кроме настоящих частиц, они снова используют размер кластера в качестве показателя. С таким гибридным подходом они корректно классифицируют статус антител к COVID‑19 в хранящихся сыворотках пациентов с 96% специфичностью и 90% чувствительностью, даже несмотря на то, что изображения собирались в целенаправленно ошибкоопасных условиях.
Дать компьютеру возможность обнаружить важное
Хотя метод сегментации помогает, он всё ещё опирается на человеческие решения о том, какие признаки измерять — например, насколько большим или ярким должен быть кластер. Авторы идут дальше и обучают глубокую нейронную сеть напрямую переводить необработанное изображение в концентрацию антивирусных антител, используя в качестве метки только известную концентрацию и без покадровых аннотаций. Эта модель «от конца до конца», основанная на стандартной архитектуре ResNet, эффективно находит собственную комбинацию признаков: тонкие сдвиги цвета, плотность, форму кластеров, пустые пространства и другие детали. При проверке на новых образцах она оценивает уровни антител в диапазоне более чем в три с половиной порядка величин, с порогом обнаружения, приближающимся к клиническому набору ELISA, при этом требуя всего одной 30‑минутной инкубации и работая на крошечных объёмах.
Проектирование тестов, настраиваемых как микроскоп
Помимо демонстрации работоспособных анализов, исследование также рассматривает, насколько в принципе можно улучшить цифровой подсчёт частиц. Используя математическую и симуляционную модель, авторы показывают, что чувствительность таких тестов не является фиксированной; она зависит от числа используемых частиц, их однородности и того, насколько хорошо одиночные и парные частицы можно различить по яркости. Регулируя эти параметры — особенно количество частиц и их качество — можно теоретически достичь чрезвычайно низких обнаруживаемых концентраций, ограниченных главным образом фундаментальной статистикой подсчёта. Машинное обучение даёт дополнительный эффект, позволяя надёжно использовать больше частиц и улучшая различение между истинными событиями связывания и случайным шумом.
К более умным, более толерантным тестам крови
В целом работа показывает, что сочетание простой оптики и продвинутого анализа изображений может дать тесты, сопоставимые с лабораторными методами эталонного уровня, при этом устойчивые к вариабельности реального применения. Вместо того чтобы создавать всё более точное оборудование, подход опирается на богатую информацию, уже содержащуюся в изображениях, и позволяет программному обеспечению отделять сигнал от помех. Для пациентов и систем здравоохранения это может означать более надёжные экспресс‑тесты у постели больного и самопроводимые тесты на распространённые маркеры крови и инфекционные заболевания, без необходимости в сложных приборах или экспертных операторах.
Цитирование: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Ключевые слова: цифровой иммуноассай, визуализация наночастиц, диагностика с помощью машинного обучения, экспресс‑тестирование у пациента, антитела к SARS‑CoV‑2