Clear Sky Science · it
Immunoassay digitali omogenei basati su immagini con alta tolleranza agli errori
Perché le particelle minuscole e le fotocamere intelligenti contano
Molti dei test medici odierni richiedono un laboratorio completo con personale specializzato oppure offrono risposte rapide ma approssimative su una striscia semplice. Questo articolo presenta un modo per ottenere il meglio di entrambi i mondi: precisione da laboratorio da un piccolo campione di sangue usando hardware semplice, con la maggior parte del lavoro svolto da un’analisi intelligente delle immagini. Osservando come si comportano minuscole particelle d’oro in una goccia di sangue e lasciando che software di apprendimento automatico interpreti quelle immagini, gli autori mostrano una strada verso test domestici e clinici facili da usare e difficili da ingannare.
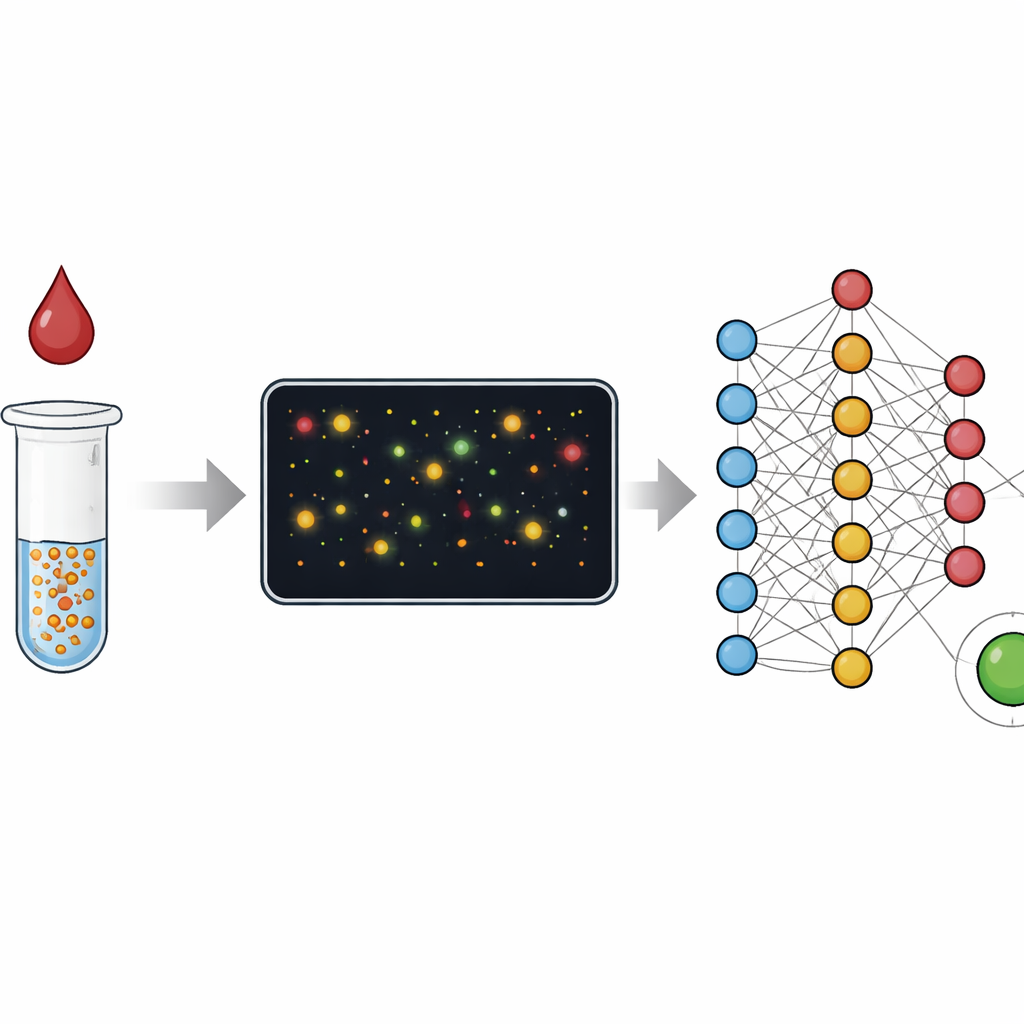
Dai cambiamenti di colore al conteggio delle particelle
I test tradizionali del sangue come l’ELISA registrano un cambiamento di colore medio da milioni di molecole in una provetta, un po’ come giudicare una folla dal livello generale di rumore. I test rapidi su striscia, o saggi a flusso laterale, funzionano su un’idea simile e sacrificano precisione in favore di velocità e semplicità. In questo studio i ricercatori si concentrano invece su singole nanoparticelle d’oro che si agglomerano quando rilevano il loro bersaglio nel campione, ad esempio la proteina C-reattiva legata all’infiammazione o anticorpi contro il virus che causa il COVID-19. Anziché misurare solo il colore complessivo della soluzione, usano microscopia a campo scuro per acquisire immagini di piccoli campi pieni di particelle e ammassi, poi analizzano ciascuno di essi. Questo passaggio dal conteggio “analogico” del colore al conteggio “digitale” amplia notevolmente la gamma di concentrazioni misurabili e rende più semplice individuare quando qualcosa è andato storto.
Vedere attraverso il caos dei campioni reali
I campioni di sangue reali sono disordinati: contengono globuli rossi, detriti, bolle e altre fonti di confusione visiva che possono ingannare regole semplici di elaborazione delle immagini. Il team mostra innanzitutto che anche con algoritmi convenzionali tarati è possibile estrarre una relazione pulita e quasi lineare tra la dimensione degli ammassi e i livelli di proteina C-reattiva, e che ciò si può fare direttamente nel sangue intero senza separare i globuli. Per affrontare in modo più sistematico gli artefatti, addestrano poi un modello di segmentazione che etichetta ogni pixel dell’immagine come nanoparticella, cellula, polvere o sfondo. Dopo aver filtrato tutto tranne le vere particelle, usano di nuovo la dimensione degli ammassi come lettura. Con questo approccio ibrido, classificano correttamente lo stato degli anticorpi COVID-19 in sieri di pazienti conservati con il 96% di specificità e il 90% di sensibilità, nonostante le immagini siano state raccolte in condizioni intenzionalmente predisposte a errori.
Lasciare che il computer scopra ciò che conta
Sebbene il metodo di segmentazione aiuti, dipende ancora da scelte umane su quali caratteristiche misurare—per esempio quanto grande o luminosa debba essere una massa. Gli autori spingono oltre addestrando una rete neurale profonda a passare direttamente da un’immagine grezza alla concentrazione di anticorpi antivirali, usando solo la concentrazione nota come etichetta e senza annotazioni a livello di pixel. Questo modello end-to-end, basato su un’architettura ResNet standard, impara efficacemente la propria combinazione di indizi: sottili variazioni di colore, densità, forma degli ammassi, spazi vuoti e altro. Testato su nuovi campioni, stima i livelli di anticorpi su un intervallo superiore a tre ordini di grandezza e mezzo, con un limite di rilevamento prossimo a quello di un kit ELISA clinico, pur richiedendo una singola incubazione di 30 minuti e funzionando su volumi minimi.
Progettare test che si possono regolare come un microscopio
Oltre a dimostrare saggi funzionanti, lo studio indaga anche fino a che punto questo tipo di conteggio digitale delle particelle possa essere spinto in principio. Utilizzando un quadro matematico e di simulazione, gli autori mostrano che la sensibilità di tali test non è fissa; dipende da quante particelle vengono usate, quanto sono uniformi e quanto bene particelle singole e coppie possono essere distinte per luminosità. Regolando queste manopole—soprattutto il numero di particelle e la loro qualità—sostengono che si può, in teoria, raggiungere concentrazioni rilevabili estremamente basse, limitate principalmente dalla statistica del conteggio fondamentale. Il machine learning aggiunge un ulteriore vantaggio aumentando il numero di particelle che possono essere usate con fiducia e migliorando la discriminazione tra veri eventi di legame e rumore casuale.
Verso test del sangue più intelligenti e più indulgenti
Nel complesso, il lavoro suggerisce che abbinare ottiche semplici ad analisi d’immagine avanzata può offrire test che rivaleggiano con i metodi di laboratorio standard, pur tollerando la variabilità dell’uso nel mondo reale. Invece di costruire hardware sempre più preciso, l’approccio fa affidamento sulle ricche informazioni già presenti nelle immagini e lascia al software il compito di separare il segnale dal disordine. Per i pazienti e i sistemi sanitari, questo potrebbe significare test point-of-care e autogestiti più affidabili per marker ematici comuni e malattie infettive, senza la necessità di strumenti complessi o operatori esperti.
Citazione: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Parole chiave: immunoassay digitale, imaging di nanoparticelle, diagnostica con machine learning, test point-of-care, anticorpi SARS-CoV-2