Clear Sky Science · fr
Immunodosages numériques homogènes basés sur l'imagerie avec grande tolérance aux erreurs
Pourquoi de minuscules particules et des caméras intelligentes comptent
Beaucoup des analyses médicales actuelles exigent soit un laboratoire complet avec du personnel qualifié, soit des réponses rapides mais approximatives sur une bandelette simple. Cet article présente une manière d’obtenir le meilleur des deux mondes : une précision de niveau laboratoire à partir d’un petit prélèvement sanguin avec du matériel simple, la majeure partie du traitement étant réalisée par une analyse d’image astucieuse. En observant le comportement de minuscules particules d’or dans une goutte de sang et en laissant un logiciel d’apprentissage automatique interpréter ces images, les auteurs montrent une voie vers des tests à domicile et en clinique à la fois faciles d’utilisation et difficiles à tromper.
Du changement de couleur au comptage de particules
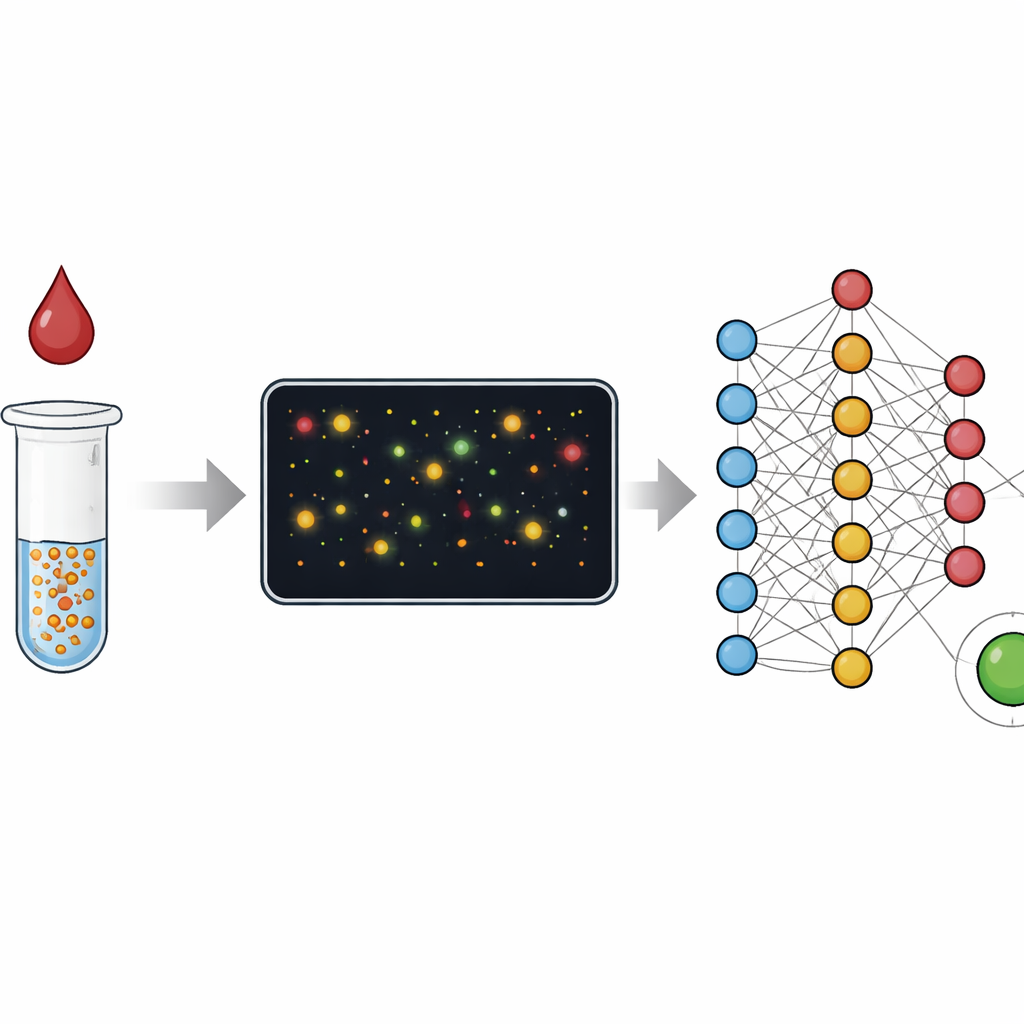
Les tests sanguins traditionnels comme l’ELISA mesurent un changement de couleur moyen provenant de millions de molécules dans un puits, un peu comme juger une foule d’après son niveau sonore global. Les tests rapides sur bandelette, ou dosages par flux latéral, reposent sur une idée similaire et sacrifient la précision pour la rapidité et la simplicité. Dans cette étude, les chercheurs se concentrent plutôt sur des nanoparticules d’or individuelles qui s’agrègent lorsqu’elles rencontrent leur cible dans un échantillon, comme la protéine C‑réactive liée à l’inflammation ou des anticorps dirigés contre le virus responsable de la COVID‑19. Plutôt que de ne mesurer que la couleur d’ensemble de la solution, ils utilisent la microscopie en champ sombre pour imager de petits champs remplis de ces particules et d’agrégats, puis analysent chaque élément. Ce passage de la mesure « analogique » de couleur au comptage « numérique » élargit fortement la gamme de concentrations mesurables et facilite la détection des anomalies.
Voir à travers le désordre des échantillons réels
Les échantillons sanguins réels sont complexes : ils contiennent des globules rouges, des débris, des bulles et d’autres sources d’encombrement visuel qui peuvent tromper des règles simples de traitement d’image. L’équipe montre d’abord que, même avec des algorithmes conventionnels optimisés, ils peuvent extraire une relation nette et presque linéaire entre la taille des agrégats et les niveaux de protéine C‑réactive, et ce directement dans le sang total sans centrifuger les cellules. Pour traiter plus systématiquement les artefacts, ils entraînent ensuite un modèle de segmentation qui étiquette chaque pixel d’une image comme nanoparticule, cellule, poussière ou fond. Après avoir filtré tout ce qui n’est pas une vraie particule, ils utilisent à nouveau la taille des agrégats comme signal de lecture. Avec cette approche hybride, ils classifient correctement le statut anticorps COVID‑19 dans des sérums de patients conservés avec 96 % de spécificité et 90 % de sensibilité, bien que les images aient été acquises dans des conditions volontairement propices aux erreurs.
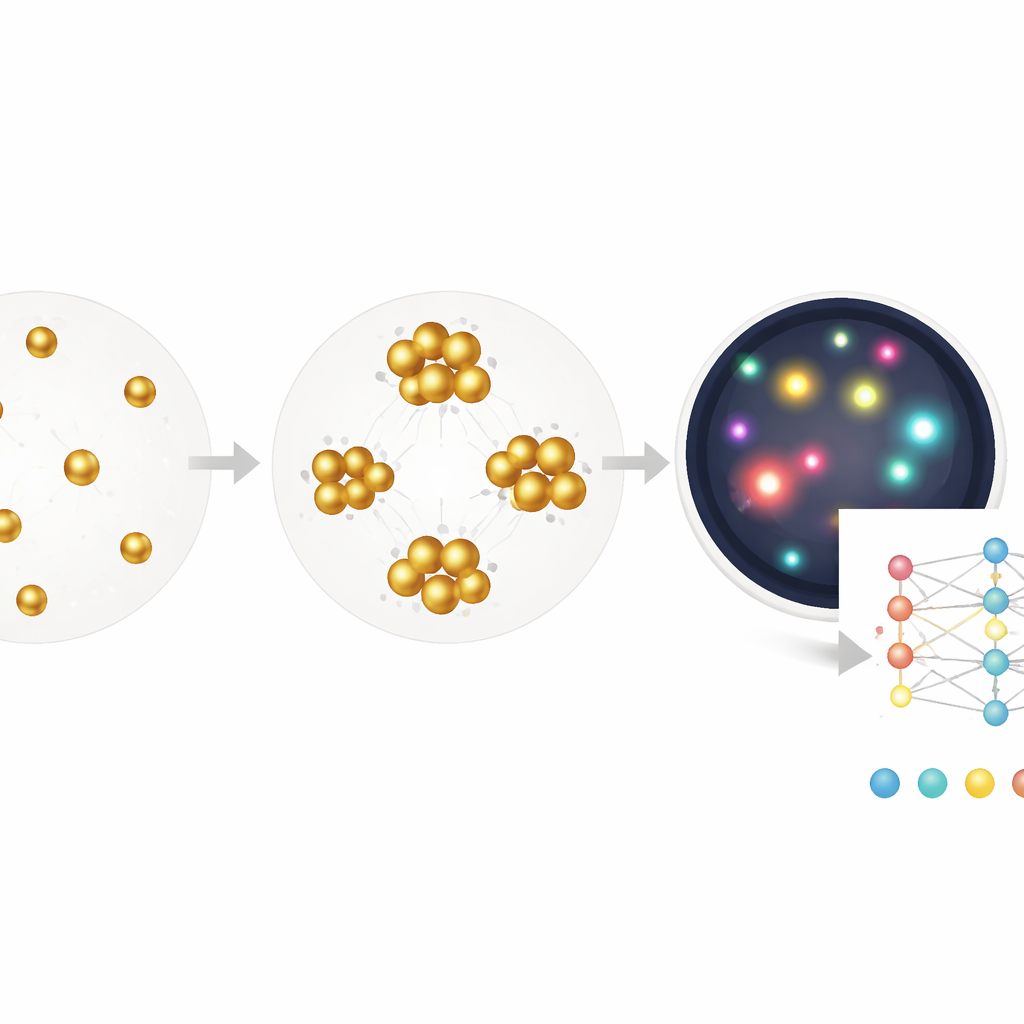
Laisser l’ordinateur découvrir ce qui compte
Si la segmentation aide, elle repose encore sur des choix humains concernant les caractéristiques à mesurer — par exemple la taille ou la luminosité qu’un agrégat doit atteindre. Les auteurs vont plus loin en entraînant un réseau neuronal profond pour passer directement d’une image brute à la concentration d’anticorps antiviraux, en n’utilisant comme étiquette que la concentration connue et sans annotations au niveau du pixel. Ce modèle de bout en bout, construit sur une architecture ResNet standard, apprend en pratique sa propre combinaison d’indices : légers changements de couleur, densité, forme des agrégats, espaces vides, et plus encore. Testé sur de nouveaux échantillons, il estime les niveaux d’anticorps sur une plage de plus de trois ordres de grandeur et demi, avec une limite de détection approchant celle d’un kit ELISA clinique, tout en ne nécessitant qu’une incubation unique de 30 minutes et des volumes minimes.
Concevoir des tests réglables comme un microscope
Au‑delà de la démonstration d’essais fonctionnels, l’étude examine aussi jusqu’où ce type de comptage numérique de particules peut être poussé en principe. À l’aide d’un cadre mathématique et de simulations, les auteurs montrent que la sensibilité de tels tests n’est pas fixe ; elle dépend du nombre de particules utilisées, de leur uniformité et de la capacité à distinguer des particules seules et appariées par leur luminosité. En ajustant ces paramètres — en particulier le nombre de particules et leur qualité — ils soutiennent qu’on peut en théorie atteindre des concentrations détectables extrêmement faibles, limitées principalement par les statistiques fondamentales du comptage. L’apprentissage automatique apporte un gain supplémentaire en augmentant le nombre de particules utilisables avec confiance et en améliorant la discrimination entre événements de liaison réels et bruit aléatoire.
Vers des tests sanguins plus intelligents et plus tolérants
Dans l’ensemble, ce travail suggère que l’association d’une optique simple et d’une analyse d’image avancée peut fournir des tests qui rivalisent avec les méthodes de référence en laboratoire tout en tolérant la variabilité de l’usage en conditions réelles. Plutôt que de construire du matériel toujours plus précis, l’approche exploite l’information riche déjà présente dans les images et laisse le logiciel séparer le signal du désordre. Pour les patients et les systèmes de santé, cela pourrait signifier des tests au point de soins et auto‑administrés plus fiables pour les marqueurs sanguins courants et les maladies infectieuses, sans besoin d’instruments complexes ni d’opérateurs experts.
Citation: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Mots-clés: immunodosage numérique, imagerie de nanoparticules, dépistage par apprentissage automatique, tests au point de soins, anticorps SARS-CoV-2