Clear Sky Science · es
Inmunoensayos digitales homogéneos basados en imágenes con alta tolerancia a errores
Por qué importan las partículas diminutas y las cámaras inteligentes
Muchas de las pruebas médicas actuales exigen un laboratorio completo con personal especializado o bien ofrecen respuestas rápidas pero aproximadas en una tira sencilla. Este artículo presenta una forma de obtener lo mejor de ambos mundos: precisión de laboratorio a partir de una pequeña muestra de sangre usando hardware simple, con la mayor parte del trabajo pesado realizado por un análisis de imagen inteligente. Observando cómo se comportan diminutas partículas de oro en una gota de sangre y dejando que el software de aprendizaje automático interprete esas imágenes, los autores muestran un camino hacia pruebas domésticas y clínicas que son tanto fáciles de usar como difíciles de engañar.
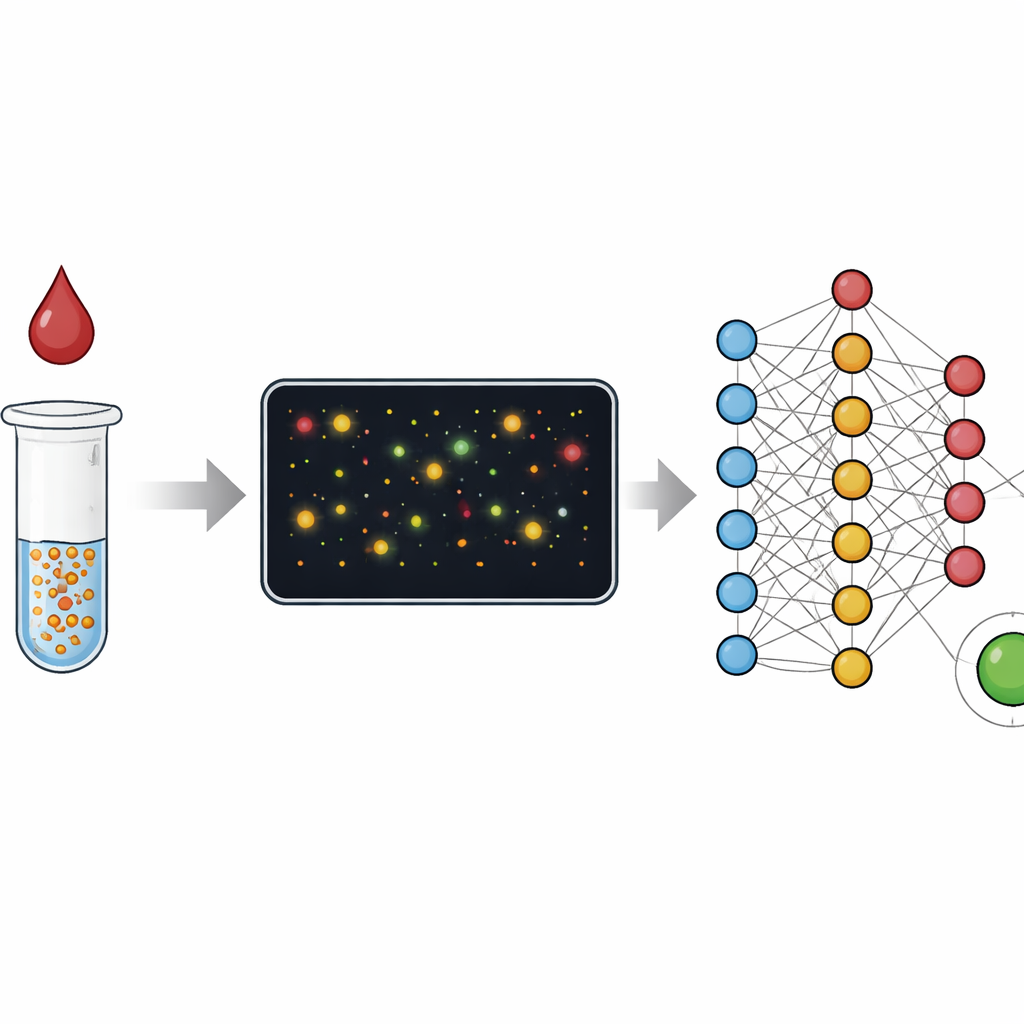
De cambios de color a contar partículas
Las pruebas tradicionales de sangre, como ELISA, leen un cambio de color medio procedente de millones de moléculas en un pocillo, de forma análoga a juzgar a una multitud por su nivel de ruido global. Las pruebas rápidas de tira, o inmunoensayos de flujo lateral, funcionan con una idea similar y sacrifican precisión por velocidad y sencillez. En este estudio, los investigadores en cambio se concentran en nanopartículas de oro individuales que se agrupan cuando encuentran su diana en una muestra, por ejemplo proteína C reactiva ligada a la inflamación o anticuerpos contra el virus que causa la COVID-19. En lugar de medir solo el color global de la solución, usan microscopía en campo oscuro para capturar imágenes de pequeños campos repletos de estas partículas y racimos, y luego analizan cada uno. Este cambio de un enfoque “analógico” de color a uno “digital” de conteo ensancha considerablemente el rango de concentraciones que la prueba puede medir y facilita detectar cuando algo ha salido mal.
Ver a través del desorden en muestras del mundo real
Las muestras de sangre reales son desordenadas: contienen glóbulos rojos, restos, burbujas y otras fuentes de ruido visual que pueden confundir reglas simples de procesamiento de imagen. El equipo muestra primero que incluso con algoritmos convencionales ajustados pueden extraer una relación limpia y casi lineal entre el tamaño del racimo y los niveles de proteína C reactiva, y que pueden hacerlo directamente en sangre entera sin centrifugar las células. Para tratar más sistemáticamente los artefactos, luego entrenan un modelo de segmentación que etiqueta cada píxel de una imagen como nanopartícula, célula, polvo o fondo. Tras filtrar todo excepto las partículas verdaderas, vuelven a usar el tamaño del racimo como lectura. Con este enfoque híbrido, clasifican correctamente el estado de anticuerpos contra COVID-19 en sueros de pacientes almacenados con un 96 % de especificidad y un 90 % de sensibilidad, aunque las imágenes se recopilaron en condiciones deliberadamente propensas a errores.
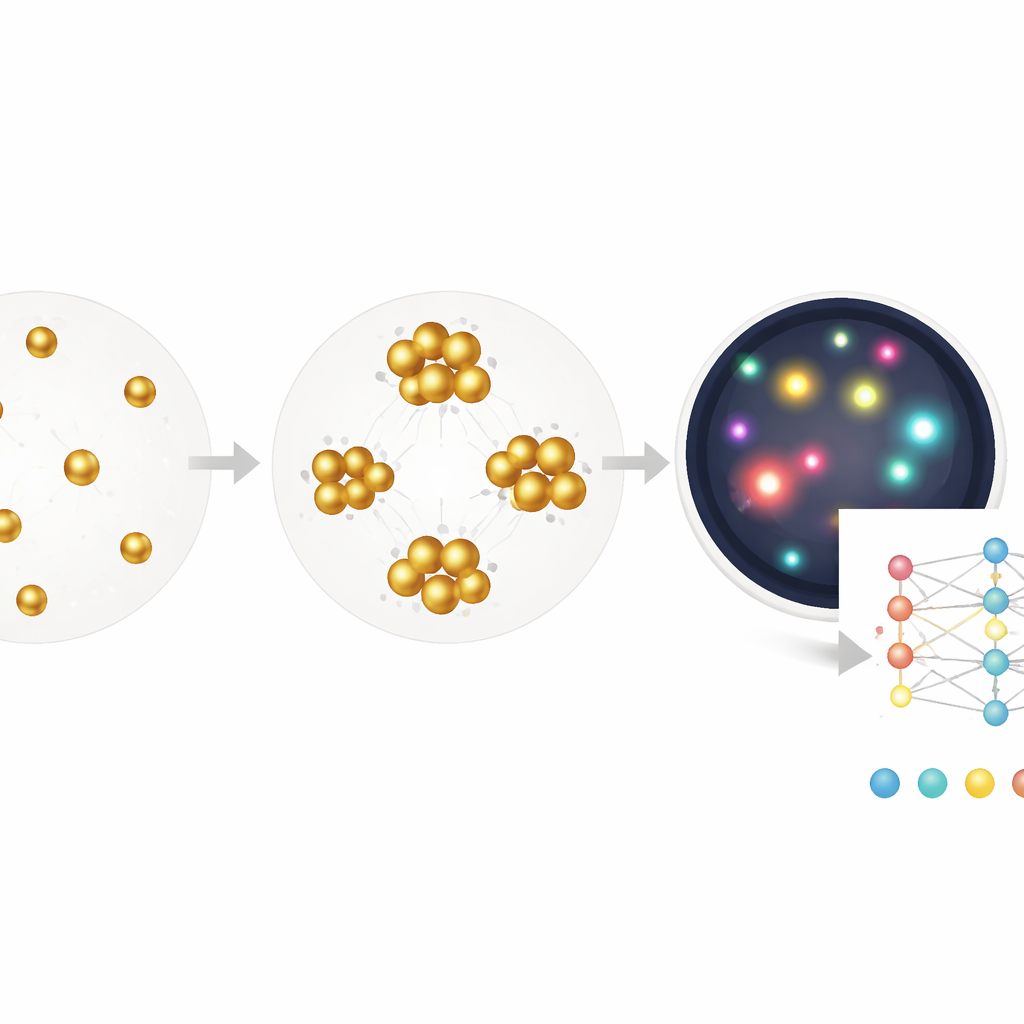
Dejar que el ordenador descubra lo que importa
Si bien el método de segmentación ayuda, todavía depende de decisiones humanas sobre qué características medir—por ejemplo, qué tan grande o brillante debe ser un racimo. Los autores van más allá entrenando una red neuronal profunda para pasar directamente de una imagen sin procesar a la concentración de anticuerpos antivirales, usando únicamente la concentración conocida como etiqueta y sin anotaciones a nivel de píxel. Este modelo de extremo a extremo, basado en una arquitectura ResNet estándar, aprende de forma efectiva su propia combinación de pistas: sutiles cambios de color, densidad, forma de los racimos, espacios vacíos y más. Al evaluarlo en muestras nuevas, estima niveles de anticuerpos en un rango de más de tres órdenes y medio de magnitud, con un límite de detección que se aproxima al de un kit ELISA clínico, pero requiere solo una incubación de 30 minutos y funciona con volúmenes diminutos.
Diseñar pruebas que se puedan ajustar como un microscopio
Más allá de demostrar ensayos operativos, el estudio también pregunta hasta dónde podría empujarse en principio este tipo de conteo digital de partículas. Usando un marco matemático y de simulación, los autores muestran que la sensibilidad de tales pruebas no es fija; depende de cuántas partículas se usen, cuán uniformes sean y de qué tan bien se puedan distinguir partículas individuales y parejas por brillo. Al ajustar estas perillas—especialmente el número de partículas y su calidad—sostienen que, en teoría, se pueden alcanzar concentraciones detectables extremadamente bajas, limitadas principalmente por la estadística de conteo fundamental. El aprendizaje automático añade un impulso adicional al aumentar cuántas partículas pueden usarse con confianza y al mejorar la discriminación entre eventos de unión reales y ruido aleatorio.
Hacia pruebas de sangre más inteligentes y tolerantes
En conjunto, el trabajo sugiere que emparejar óptica simple con análisis avanzado de imágenes puede ofrecer pruebas que rivalizan con métodos de referencia de laboratorio mientras toleran la variabilidad del uso en el mundo real. En lugar de construir hardware cada vez más preciso, el enfoque se apoya en la información rica ya presente en las imágenes y deja que el software separe la señal del desorden. Para pacientes y sistemas de salud, esto podría significar pruebas en el punto de atención y autoadministradas más fiables para marcadores sanguíneos comunes y enfermedades infecciosas, sin la necesidad de instrumentos complejos u operadores expertos.
Cita: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Palabras clave: inmunoensayo digital, imagen de nanopartículas, diagnóstico con aprendizaje automático, pruebas en el punto de atención, anticuerpos SARS-CoV-2