Clear Sky Science · pl
Jednorodne obrazowe immunotesty cyfrowe o wysokiej tolerancji błędów
Dlaczego malutkie cząstki i inteligentne kamery mają znaczenie
Wiele współczesnych badań medycznych wymaga albo pełnego laboratorium z wykwalifikowanym personelem, albo daje szybkie, lecz przybliżone odpowiedzi na prostej kasetce. Artykuł przedstawia sposób na pogodzenie obu podejść: dokładność na poziomie laboratoryjnym uzyskaną z małej próbki krwi przy użyciu prostego sprzętu, gdzie większość pracy wykonuje sprytna analiza obrazów. Obserwując zachowanie maleńkich cząstek złota w kropli krwi i pozwalając oprogramowaniu uczącemu się maszynowo interpretować te obrazy, autorzy pokazują drogę do testów domowych i gabinetowych, które są jednocześnie łatwe w użyciu i trudne do oszukania.
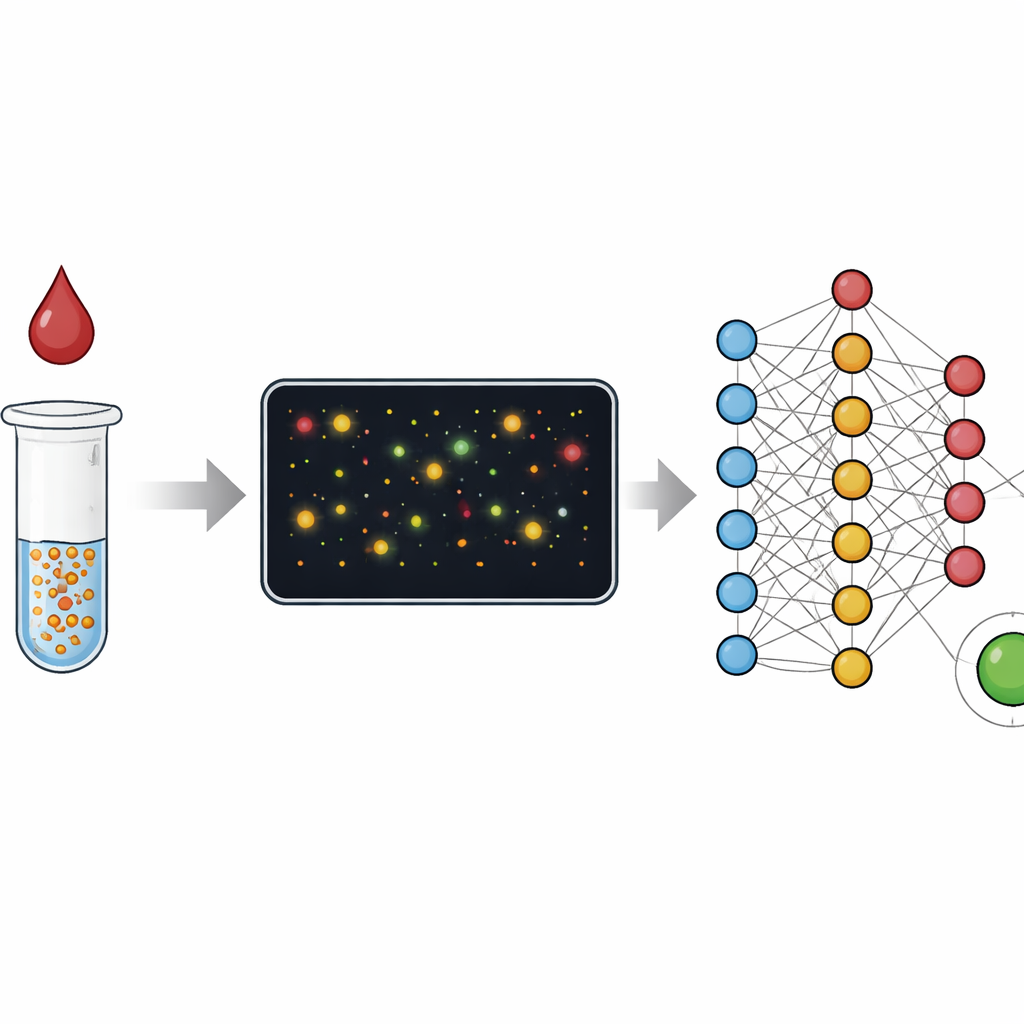
Od zmian koloru do liczenia cząstek
Tradycyjne testy krwi, takie jak ELISA, odczytują średnią zmianę koloru pochodzącą od milionów cząsteczek w studzience — podobnie jak ocenianie tłumu po jego ogólnym poziomie hałasu. Szybkie testy paskowe, czyli testy immunochromatograficzne, opierają się na podobnej idei i kosztem szybkości i prostoty rezygnują z dokładności. W tej pracy badacze skupiają się zamiast tego na pojedynczych nanocząstkach złota, które zlepiają się w obecności docelowej molekuły w próbce, na przykład białka C‑reaktywnego związanego z zapaleniem lub przeciwciał przeciw wirusowi wywołującemu COVID‑19. Zamiast mierzyć jedynie ogólny kolor roztworu, używają ciemnego pola mikroskopowego, aby obrazować drobne pola pełne tych cząstek i klastrów, a następnie analizują każdy z nich. Ta zamiana z „analogowego” pomiaru koloru na „cyfrowe” liczenie znacznie rozszerza zakres stężeń, które test potrafi zmierzyć, i ułatwia wykrywanie, gdy coś poszło nie tak.
Widzenie przez bałagan w próbkach z prawdziwego świata
Rzeczywiste próbki krwi są nieuporządkowane: zawierają czerwone krwinki, fragmenty komórek, pęcherzyki i inne źródła wizualnego zakłócenia, które mogą zmylić proste reguły przetwarzania obrazu. Zespół najpierw pokazuje, że nawet przy dopracowanych konwencjonalnych algorytmach można wydobyć czysty, niemal liniowy związek między rozmiarem klastra a poziomem białka C‑reaktywnego, i to bez separacji komórek — bezpośrednio w pełnej krwi. Aby systematyczniej radzić sobie z artefaktami, następnie trenują model segmentacji, który oznacza każdy piksel na obrazie jako nanopartykułę, komórkę, kurz lub tło. Po odfiltrowaniu wszystkiego poza prawdziwymi cząstkami ponownie używają rozmiaru klastra jako odczytu. Dzięki temu hybrydowemu podejściu poprawnie klasyfikują status przeciwciał COVID‑19 w przechowywanych surowicach pacjentów z 96% swoistością i 90% czułością, nawet gdy obrazy zbierano w warunkach celowo obciążonych błędami.
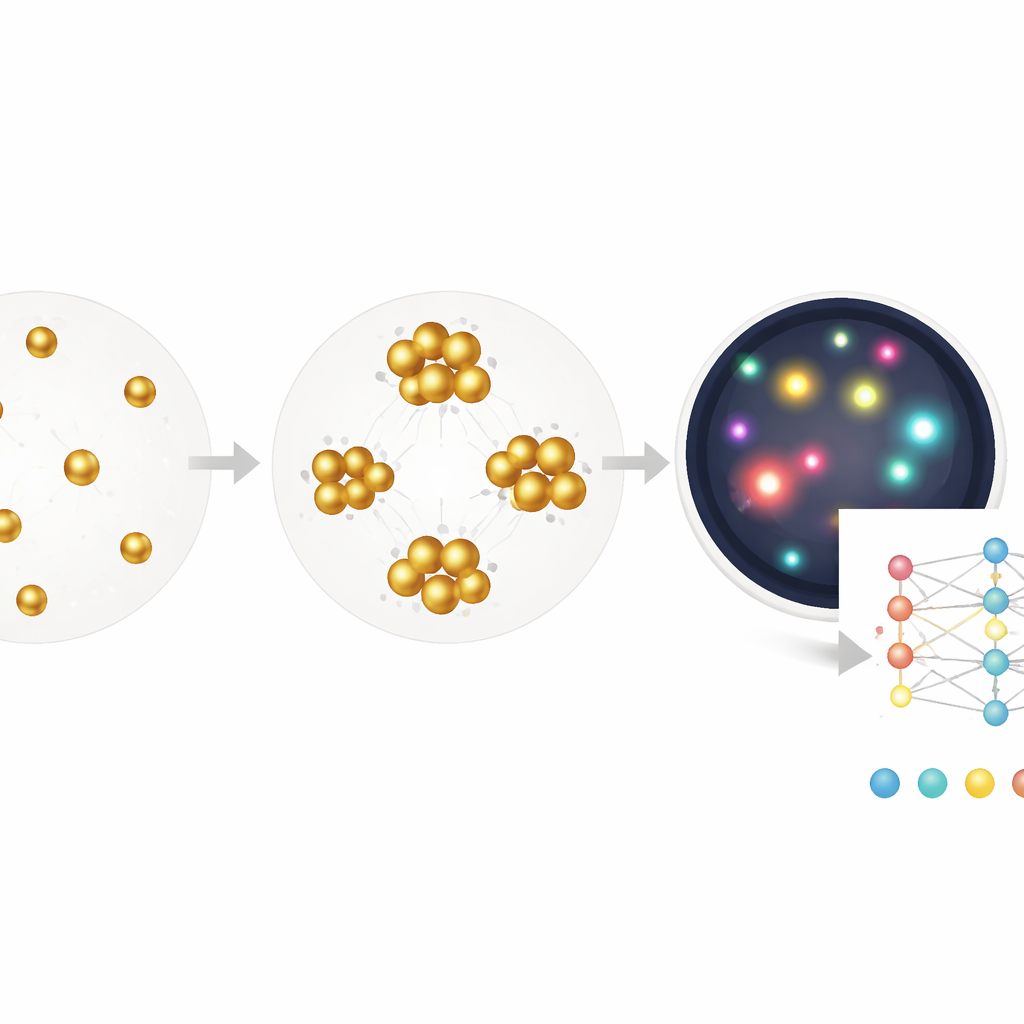
Pozwalając komputerowi odkryć, co ma znaczenie
Choć metoda segmentacji pomaga, wciąż opiera się na ludzkich wyborach dotyczących tego, które cechy mierzyć — na przykład jak duży lub jak jasny musi być klaster. Autorzy idą dalej, trenując głęboką sieć neuronową, która przechodzi bezpośrednio od surowego obrazu do stężenia przeciwciał przeciwwirusowych, używając jedynie znanego stężenia jako etykiety i bez adnotacji na poziomie piksela. Ten model end‑to‑end, oparty na standardowej architekturze ResNet, efektywnie uczy się własnej kombinacji wskazówek: subtelnych przesunięć koloru, gęstości, kształtu klastrów, pustych przestrzeni i innych. Testowany na nowych próbkach estymuje poziomy przeciwciał w zakresie przekraczającym trzy i pół rzędu wielkości, z granicą detekcji zbliżoną do klinicznego zestawu ELISA, a jednocześnie wymaga tylko pojedynczej 30‑minutowej inkubacji i działa na bardzo małych objętościach.
Projektowanie testów, które można dostroić jak mikroskop
Poza demonstracją działających testów, badanie pyta też, jak daleko teoretycznie można posunąć liczenie cząstek w trybie cyfrowym. Korzystając z ram matematycznych i symulacyjnych, autorzy pokazują, że czułość takich testów nie jest stała; zależy od liczby użytych cząstek, ich jednorodności oraz tego, jak dobrze można rozróżnić pojedyncze i pary cząstek po jasności. Poprzez regulację tych parametrów — zwłaszcza liczby cząstek i ich jakości — argumentują, że w teorii można osiągnąć wyjątkowo niskie wykrywalne stężenia, ograniczone głównie przez fundamentalne statystyki zliczeń. Uczenie maszynowe dodaje kolejny impuls, zwiększając liczbę cząstek, które można pewnie wykorzystać, oraz poprawiając rozróżnianie między prawdziwymi zdarzeniami wiązania a losowym szumem.
W kierunku mądrzejszych, bardziej wybaczających testów krwi
Podsumowując, praca sugeruje, że połączenie prostych układów optycznych z zaawansowaną analizą obrazów może dostarczyć testy dorównujące złotym standardom laboratoryjnym, jednocześnie tolerujące zmienność rzeczywistego użycia. Zamiast budować coraz precyzyjniejszy sprzęt, podejście opiera się na bogactwie informacji już obecnych w obrazach i pozwala oprogramowaniu oddzielić sygnał od zakłóceń. Dla pacjentów i systemów opieki zdrowotnej może to oznaczać bardziej niezawodne testy przyłóżkowe i samodzielne badania dla powszechnych markerów krwi i chorób zakaźnych, bez potrzeby skomplikowanych instrumentów czy ekspertów obsługi.
Cytowanie: McAffee, D.B., Hu, Q., Arnob, A. et al. Homogeneous image-based digital immunoassays with high error tolerance. npj Imaging 4, 30 (2026). https://doi.org/10.1038/s44303-026-00164-9
Słowa kluczowe: immunotest cyfrowy, obrazowanie nanopartykuł, diagnostyka z uczeniem maszynowym, badania przy łóżku pacjenta, przeciwciała SARS-CoV-2